新加坡国立大学赵宇教授课题组在JACS发表桥联轴手性联芳化合物研究成果
轴手性化合物是一类非常重要的手性化合物,存在于许多天然产物中,在金属催化剂配体和有机催化剂得到广泛应用,但是其不对称催化合成至今仍是一项极具挑战的工作。新加坡国立大学(NUS)的赵宇课题组在该领域做出了原创性的研究工作(Angew. Chem. Int. Ed., 2014, 53, 11041 –11045; Nat. Commun., 2019, 10, 3061.; Org. Lett., 2019, 21, 6169-6172)。桥联轴手性联芳基骨架是一类比较特殊的结构单元,广泛存在于药物分子以及天然产物中,例如异五味子素(isoschizandrin)、五加前胡素(steganacin) 、天然产物rhazinilam等。

最近,西北工业大学黄维院士团队鲁神赐教授与新加坡国立大学的赵宇(Zhao Yu)教授以及Richard Wong教授报道了通过串联反应同时生成苯并呋喃或吲哚并八元环内酯的方法,得到光学纯桥联轴手性化合物。该方法利用商业化的氮杂环卡宾作为催化剂,反应条件温和,具有良好的选择性,同时产物也可以发生开环反应转化为轴手性化合物,这种新方法为合成手性的阻转异构材料提供了一条新的途径。相关结果发表在Journal of the American Chemical Society 上。
首先,作者使用对称的二酚基炔丙醇底物,通过去对称化的方法,得到苯并呋喃并八元环的轴手性化合物。该反应的底物适用性良好(15个底物)。对于富电子和缺电子底物均能获得优秀的对映选择性(高达99% ee)和非对映选择性(大于98:2 dr)。
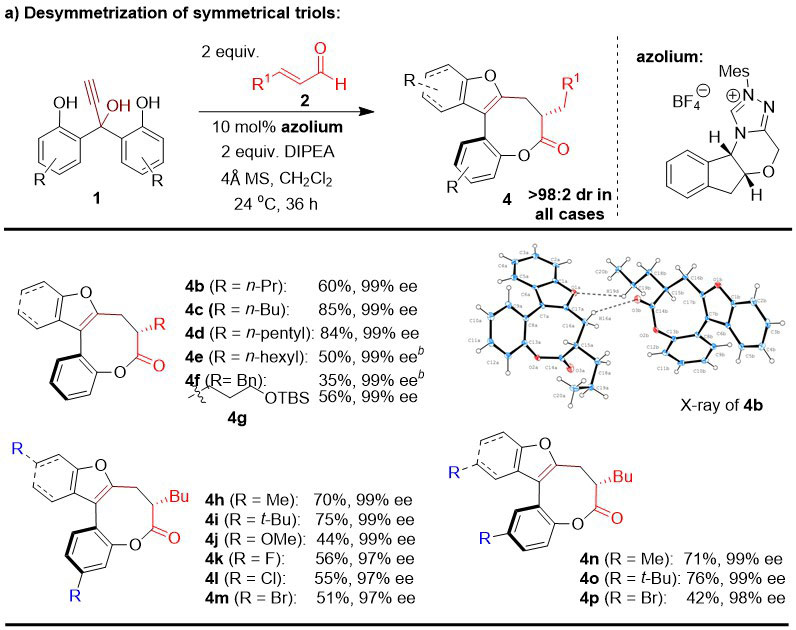
其次,作者把底物中的一个苯酚换成苯胺,在类似的条件下,外消旋的底物通过较高的化学选择性仅仅生成吲哚并八元环内酯的桥联轴手性化合物。该反应的底物适用性良好(14个底物),均能获得良好的对映选择性(高达99% ee)和非对映选择性(大于98:2 dr)。稠环吲哚类化合物是当今新药研发领域高度关注的一类化合物,广泛存在于具有生物活性的天然产物和药物分子中。
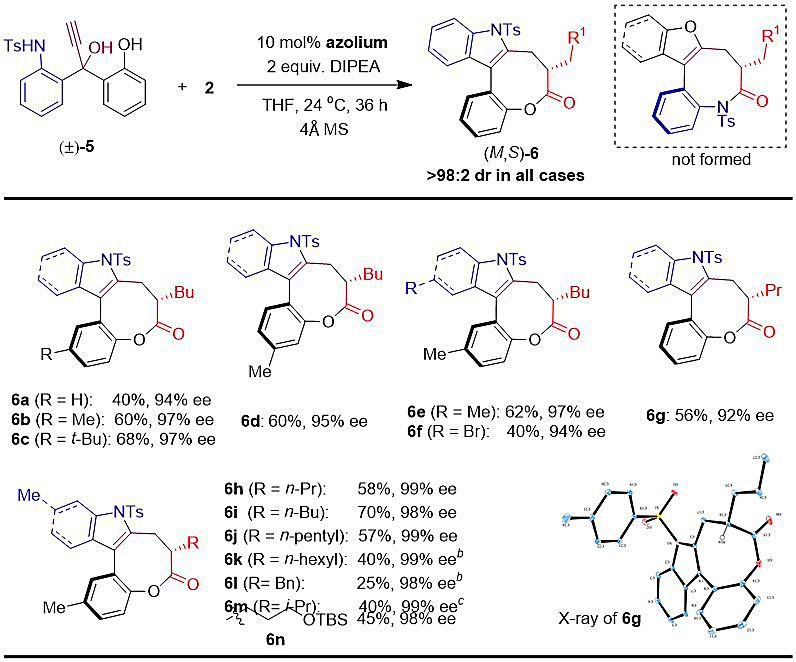
最后,作者对反应机理进行了推测,反应机理一:脱水生成共轭炔基醌酮化合物(o-QM)接着发生1,6-加成反应生成联烯中间体INT-2;反应机理二:发生SN2'亲核取代反应生成相同的中间体INT-2,它再发生串联环化反应生成桥联轴手性化合物。作者通过DFT计算对反应的机理进行了深入的研究,亲核取代反应路径(TS1)的能量是26.7 kcal/mol,它比生成共轭炔基醌酮化合物(o-QM)反应路径(TS2)的能量32.6 kcal/mol低。值得一提的是,目前非金属参与的炔丙基取代反应的成功案例只有少数几例报道。
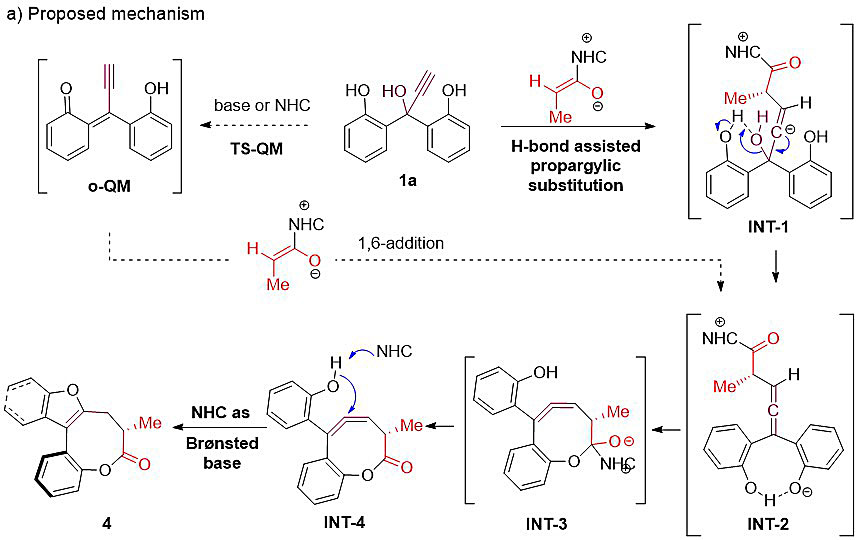

原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Diastereo- and Atroposelective Access to Bridged Biaryls Bearing an Eight-Membered Lactone through an Organocatalytic Cascade
Shenci Lu, Jun-Yang Ong, Hui Yang, Si Bei Poh, Xi Liew, Chwee San Deborah Seow, Ming Wah Wong* , Yu Zhao*
J. Am. Chem. Soc., 2019, 141, 17062-17067. DOI: 10.1021/jacs.9b08510
导师介绍

赵宇,2002年毕业于北京大学化学系,2008年在波士顿学院完成博士学位,2011年于麻省理工完成博士后深造。现为新加坡国立大学化学系副教授。课题组长期致力于金属和有机小分子催化的不对称合成研究,尤其完成了通过借氢策略实现的高经济性不对称合成以及新颖手性杂环的制备。欢迎有志于有机合成、不对称催化的同学加盟。
https://www.x-mol.com/university/faculty/4402

鲁神赐, 2011年在兰州大学完成博士学位,2018年于新加坡国立大学完成博士后深造。现为西北工业大学柔性电子研究院教授。长期致力于有机小分子的不对称催化研究,迄今以第一作者或通讯作者在J. Am. Chem. Soc., Nat. Commun., Angew. Chem. Int. Ed.(4篇), Org. Lett.(2篇), Chem. Eur. J., Adv. Synth. Catal., J. Org. Chem. 等国际一流著名期刊上发表论文十余篇。
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!













































 京公网安备 11010802027423号
京公网安备 11010802027423号