裂开母适配体靶标口袋:获得裂分适配体的新方法
近年来,适配体(aptamer)作为一种具有靶向特异性亲和力的生物识别材料,已经广泛用于生物传感、疾病诊断、环境和食品安全监测。裂分适配体(SPA)作为双片段功能核酸探针,在构建小分子污染物生物传感平台、拓展核酸适配体应用范围等方面具有重要价值。然而,SPA的获取受限于传统的“结合口袋保留”假说,仅结构中包含非功能性辅助环的母适配体才能够裂分。这一前提条件严重限制了SPA新材料的发现。目前,在超过500例核酸适配体中仅有不足20例SPA得到开发报道。
近日,清华大学环境学院周小红(点击查看介绍)团队以分子动力学(MD)模拟等前沿计算机方法结合实验手段,突破传统适配体裂分方法的限制,首次在适配体功能环结构中部进行裂分,并证明仍能保留对靶标的生物识别能力,为新型适配体工程化裂分提供了新思路,对SPA库的高效扩充以及夹心型环境小分子污染物传感方法的推广应用具有促进作用。
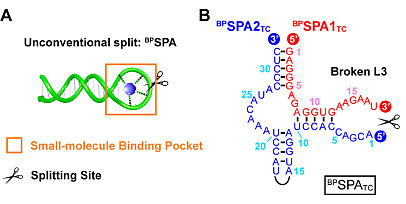
图1. 传统(A)与新型(B)适配体裂分方法
本工作结合三通(3WJ)、发卡两类代表性母适配体结构特点与靶标结合口袋信息,采用新型裂分适配体方法设计了四环素(TC)、妥布霉素(TOB)、新霉素(NEO)的新型BPSPA(BPSPATC、BPSPATOB与BPSPANEO),采用分子动力学(MD)模拟从分子层面分析了新型 BPSPA与相应靶标小分子之间的结合机理。MD模拟结果表明 BPSPATC 中有新的TC结合口袋形成,该口袋在新型裂分位点附近,与母适配体以及RPSPATC中的TC结合口袋存在明显差异。而BPSPATOB和BPSPANEO在母适配体原始靶标识别口袋完整性被破坏的情况下,仍然具备靶标识别能力,且展现出与其母适配体高度一致的识别位点。同时,作者还利用等温滴定量热技术(ITC)与荧光共振能量转移(FRET)等实验手段对模拟结果进行验证,并定量测试了各新型裂分适配体对各自靶标分子的亲和力。
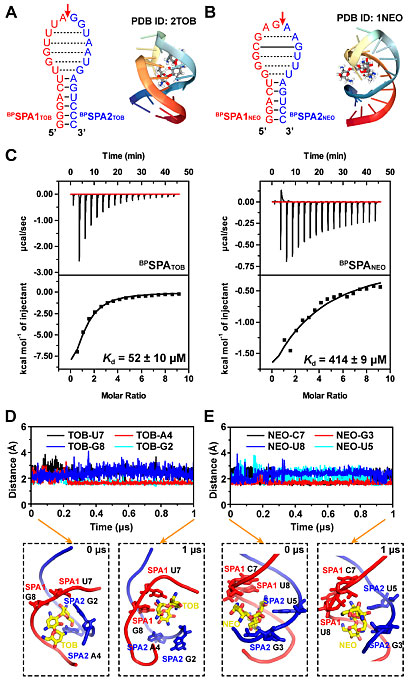
图2. 妥布霉素与新霉素裂分适配体的靶标识别机理与验证
此外,作者用获得的新型裂分适配体BPSPATOB,以妥布霉素为模型靶标物设计了基于新型裂分适配体的酶联适配体吸附实验(ELASA),对妥布霉素的裸眼检出限可达1 μM,为裂分适配体夹心传感平台的构建提供了一种简单、直观的普适性思路。
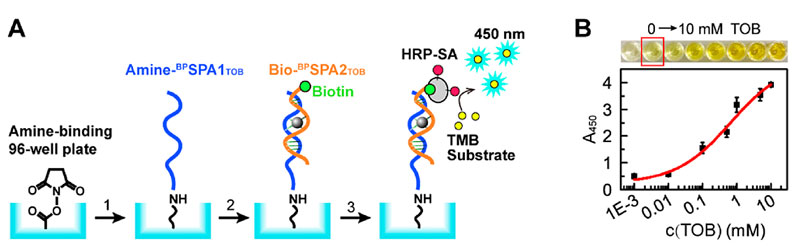
图3. 基于新型裂分适配体的妥布霉素ELISA检测流程(A)及性能(B)
这一成果近期发表在Analytical Chemistry 上并入选Supplementary Cover文章,文章的第一作者是清华大学博士研究生王若瑜和华东师范大学张乾森副教授,清华大学施汉昌教授、新加坡南洋理工大学张翼教授、Truc Kim Nguyen博士参与了本研究工作。首都师范大学娄新徽教授、南洋理工大学刘爱群教授、加拿大阿尔伯塔大学Hongquan Zhang教授对本工作提出了宝贵建议。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Unconventional Split Aptamers Cleaved at Functionally Essential Sites Preserve Biorecognition Capability
Ruoyu Wang, Qiansen Zhang, Yi Zhang, Hanchang Shi, Kim Truc Nguyen, Xiaohong Zhou*
Anal. Chem., 2019, DOI: 10.1021/acs.analchem.9b04115
导师介绍
周小红
https://www.x-mol.com/university/faculty/60667
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号