镍催化不对称Suzuki-Miyaura偶联高效构建三氟甲氧基手性中心
由于氟原子具有最大的电负性、较小的原子半径以及含氟基团特殊的亲脂性,含氟化合物在医药、农药、材料等领域具有广泛的应用。其中三氟甲氧基由于具有较高的脂溶性和较强的吸电子能力受到越来越多化学工作者的关注。近些年来,越来越多的引入三氟甲氧基的方法得以报道,但构建三氟甲氧基手性中心的方法还十分匮乏。因此,发展高效构建三氟甲氧基手性中心的方法具有十分重要的研究意义。
最近,中科院上海有机化学研究所的沈其龙研究员(点击查看介绍)团队发展了一种镍催化不对称Suzuki-Miyaura偶联的方法高效构建出三氟甲氧基手性中心。该方法巧妙地选用苯硼酸频哪醇酯与正丁基锂现场生成高活性的亲核试剂,克服了低温条件下转金属难以发生以及底物容易分解等困难,发展了一种镍催化不对称Suzuki-Miyaura偶联的方法高效构建出三氟甲氧基手性中心。相关成果发表在Angewandte Chemie International Edition 杂志上,文章的第一作者为硕士研究生黄伟臣。
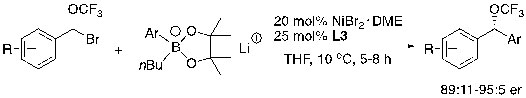
作者首先以化合物1a和芳基格氏试剂作为模板底物进行条件筛选,以20 mol %的NiBr2•DME和25 mol%的L1作为催化剂,在0 ℃的条件下反应12小时,原料可以转化完全,并以91:9 e.r.的对映选择性得到目标产物,但是产率只有38%。后来作者又尝试了锌试剂,产率同样不够理想。作者发现在锌试剂或者格氏试剂存在的条件下,底物1很容易分解。为了克服这些困难,作者又尝试使用硼酸作为亲核试剂,以碳酸钾作为碱,将反应温度提升至60 ℃,产率可以提升至81%,但是e.r.值降低至84.5:15.5。为了提高该反应的对映选择性,作者降低了该反应的温度,但是当温度降至30 ℃时,该反应几乎不能发生。
作者认为芳基硼酸对镍络合物的转金属过程需要较高的温度,所以使用硼酸作为亲核试剂时需提升体系的温度。为了加速转金属的过程,同时又不会破坏底物,作者利用硼酸频哪醇酯和正丁基锂在0 ℃现场生成化合物3作为亲核试剂的方法,化合物3与1a在0 ℃条件下反应9个小时后,以81%的氟谱产率、93:7 e.r.的对映选择性得到目标产物。反应的底物普适性较好,间位或者对位不同电性取代基修饰的底物均可以顺利地发生反应,如对位取代的氯、溴、叔丁基、烯基以及间位取代的氟、氯、溴、胺均可以兼容,反应的产率和对映选择性都可以得到满意的结果。作者还考察了α-溴代苄基三氟甲氧基化合物的底物适用范围,对位取代基为羰基、氰基、酯基、硝基等均可以获得理想的结果。为了进一步展示该反应的应用价值,作者将该方法应用于药物分子的合成中。Zeste Homolog 2 (EZH2)是一种组蛋白赖氨酸甲基转移酶抑制剂,而化合物3是其三氟甲氧基取代的衍生物。作者通过该方法以75%的分离产率、92:8的e.r.值得到化合物3a,然后再经过后续的3步反应以总产率82%、91:9的e.r.值得到化合物3。经过重结晶,该化合物的对映选择性可以高达95:5。
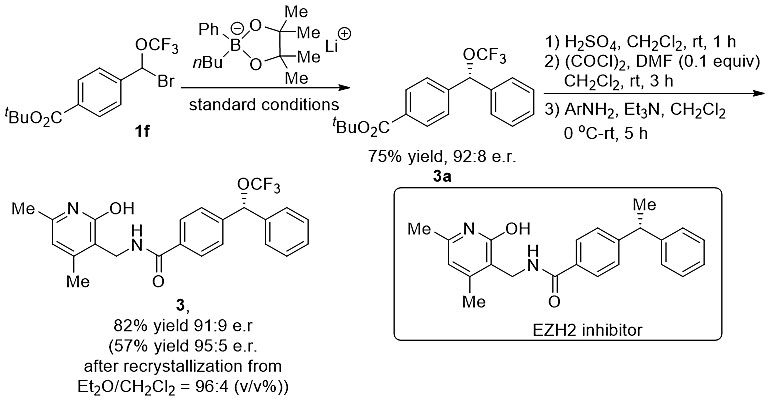
该论文作者为:Weichen Huang, Xiaolong Wan, Prof. Dr. Qilong Shen
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Enantioselective Construction of Trifluoromethoxylated Stereogenic Centers by a Nickel-Catalyzed Asymmetric Suzuki–Miyaura Coupling of Secondary Benzyl Bromides
Angew. Chem. Int. Ed., 2017, 56, 11986, DOI: 10.1002/anie.201706868
导师介绍
沈其龙
http://www.x-mol.com/university/faculty/15622
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号