短暂的离去,是为了更好的相聚——α,β-不饱和酰铵催化新进展
到目前为止,人们已经发展了多种结构的Lewis碱有机分子催化剂用于设计高选择性的催化反应。其中三级胺作为Lewis碱可以与羧酸衍生物反应获得一系列不同活性的酰铵中间体,酰铵和烯醇铵中间体广泛用于不对称的酰基转移和形式上的环加成反应。相比之下,α,β-不饱和酰铵(α,β-unsaturated acyl ammonium)的研究却相对较少。该物种的C1和C3位具有亲电性,而C2位又具有潜在的亲核性,深入探究这种酰铵中间体的反应活性有望引导人们发现更多新颖的反应,从而进一步丰富有机合成方法学。其中代表性的工作包括美国麻省理工学院的Gregory Fu教授等人报道的α,β-不饱和酰氟作为酰铵前体参与的不对称[3+2]环加成反应、英国圣安德鲁斯大学的Andrew Smith教授、美国德克萨斯A&M大学的Daniel Romo教授以及日本京东大学的Seijiro Matsubara教授等人报道的不对称Michael加成/环化、形式上环加成以及复杂的串联过程。这些反应利用α,β-不饱和酰卤或酸酐作为酰铵前体参与催化过程,但与此同时要求反应物种必须包含两个化学环境迥异的亲核位点以实现选择性共轭加成,并释放催化剂构成催化循环,由此大大限制了底物的适用范围。
最近,英国圣安德鲁斯大学Andrew Smith教授(点击查看介绍)团队在前期工作的基础上发展了手性异硫脲参与的硝基烷烃与α,β-不饱和芳基酯的不对称Michael加成反应。反应的催化循环过程通过体系中由α,β-不饱和芳基酯底物释放的芳基氧负离子“离去基团”来推动,而不是依靠反应物中的另一个亲核位点,因而使用含有单一亲核位点的亲核试剂便可以实现Michael加成过程,由此拓宽了底物的适用性(图1)。相关工作发表在Angew. Chem. Int. Ed. 上。
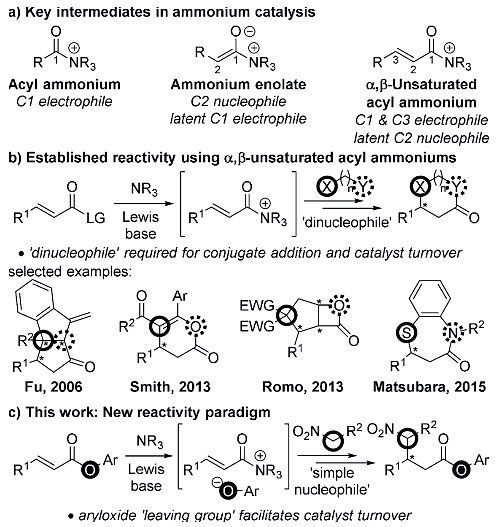
图1. 酰铵参与的催化反应。图片来源:Angew. Chem. Int. Ed.
作者首先以HyperBTM 5作为催化剂,考察溶剂和α,β-不饱和芳基酯不同芳基取代基对反应的影响。其中4-硝基苯酯1和无溶剂参与的反应条件可以得到最好的反应结果(图2)。
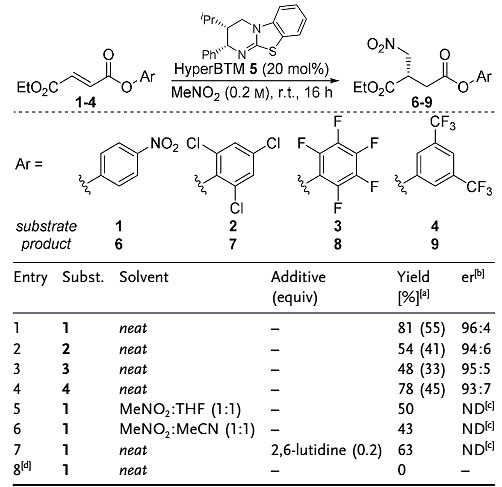
图2. 反应条件的优化。图片来源:Angew. Chem. Int. Ed.
在最佳条件下,作者随后对底物的适用范围进行了研究,考虑到苯基酯的稳定性较差,分离产率较低,因此在反应结束后需要向体系中添加合适的亲核试剂将产物转化为相对稳定的酰胺化合物。作者首先固定底物1,反应结束后对多种不同的胺类亲核试剂进行考察,都能以良好的产率(53-73%)和对映选择性(93/7-96/4)得到目标产物10-14,甲醇作为亲核试剂参与反应同样可以得到中等的收率(15)。此外,作者还对不同取代基修饰α,β-不饱和酯进行考察,也能以满意的结果得到相应的产物。当羧酸酯取代基转变为烷基时,产物的产率和选择性都出现了较大程度的下降。底物22-24不能参与反应(图3)。
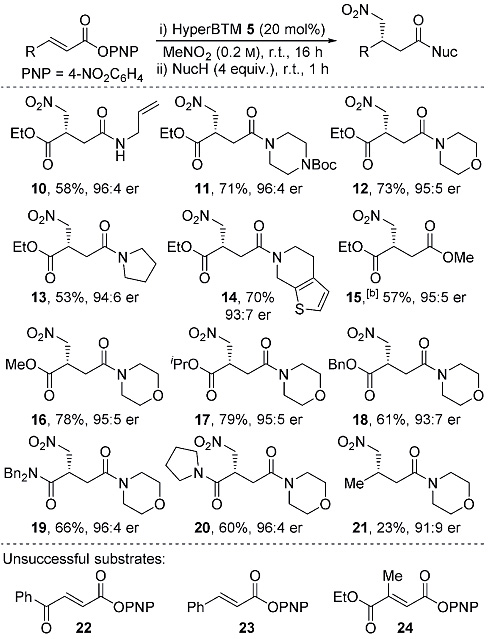
图3. α,β-不饱和酯的底物拓展。图片来源:Angew. Chem. Int. Ed.
他们随后研究了底物构型对反应的影响,结果表明顺式底物25与反式底物1参与反应时可以得到相似的结果。核磁共振波谱表征暗示顺式底物25会快速异构化为反式底物1,其异构速度要远快于产物的形成速度(图4)。
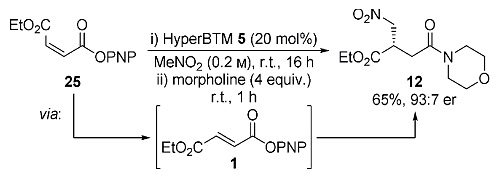
图4. 底物构型对反应结果的影响。图片来源:Angew. Chem. Int. Ed.
作者进一步研究了不同硝基烷烃对反应的影响,直链的硝基烷烃参与反应可以得到良好的产率和对映选择性,然而非对映选择性接近1/1。含支链或环状的硝基烷烃能以很好的对映选择性得到目标产物(图5)。
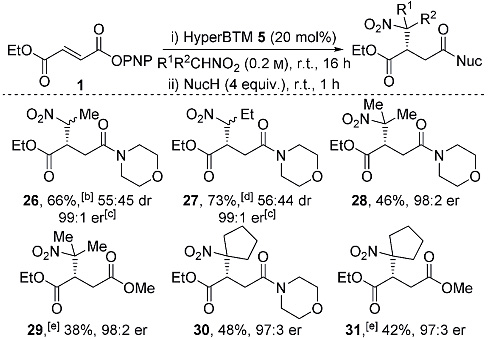
图5. 硝基烷烃的底物拓展。图片来源:Angew. Chem. Int. Ed.
为了证明该反应的实用性,作者进行了一系列的衍生化实验。产物可以顺利地通过硝基还原/环化反应构建手性的γ-氨基丁酸化合物(图6)。
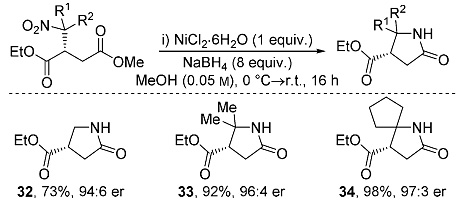
图6. 衍生化实验。图片来源:Angew. Chem. Int. Ed.
他们还对反应的机理和动力学过程进行了研究,反应的定量跟踪实验通过氟标记的底物35和催化剂(2R,3S )-8F-HyperBTM的原位19F{1H} NMR实验来完成(图7),并最终确定异硫脲催化剂在反应过程中至少存在四种状态,体系对α,β-不饱和酯及催化剂均呈现一级反应,与此同时产物对反应的动力学过程也存在影响。
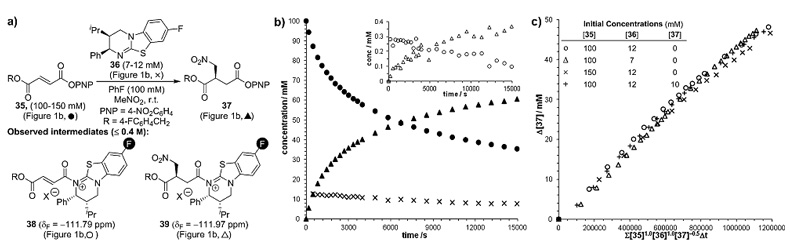
图7. 反应机理的研究。图片来源:Angew. Chem. Int. Ed.
作者进一步设计了交叉实验来探究反应的可逆性,底物40和41在标准条件下五分钟之内可快速得到40、41、42和43的混合物,随后形成相应的四种Michael加成产物44、45、46和47。他们还在标准条件下进行了产物44、45的交叉实验,同样可以得到四种交叉产物。这些实验表明异硫脲可以在α,β-不饱和酯与相应的产物之间进行快速可逆交换过程(图8)。
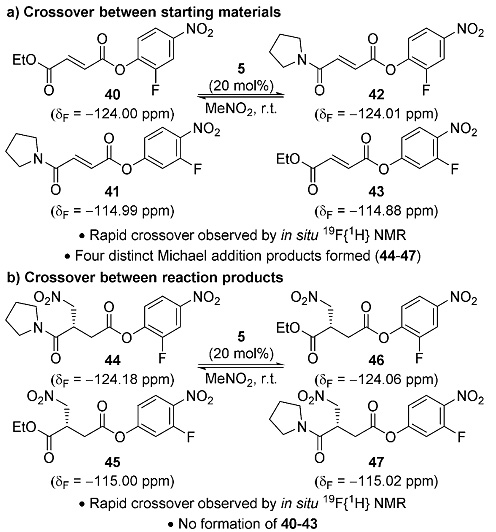
图8. 交叉实验的研究。图片来源:Angew. Chem. Int. Ed.
作者根据实验结果和一系列的机理研究提出了图9所示的反应机理。首先游离态的BTM 5与α,β-不饱和苯酯发生N-酰化反应得到中间体49,49随后发生Michael加成反应得到中间体50,50再发生质子化得到中间体51,接下来芳基氧负离子对51亲核加成-取代释放催化剂和产物,由此完成催化循环(图9)。
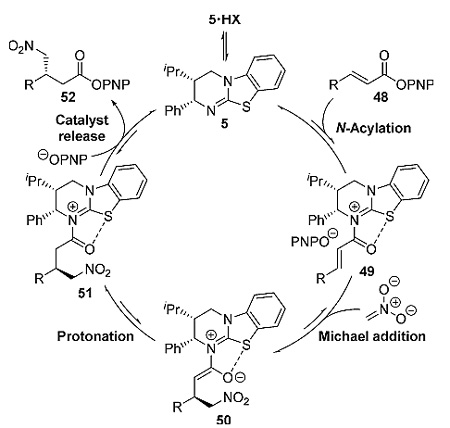
图9. 反应可能的机理。图片来源:Angew. Chem. Int. Ed.
——总结——
Andrew Smith教授团队报道了手性异硫脲参与硝基烷烃与α,β-不饱和苯酯的不对称Michael加成反应,催化循环过程通过体系中原位生成的芳基氧负离子“离去基团”来推动,反应物无需修饰另一个亲核位点。该催化体系的底物适用范围广,产物可通过一步简单的反应转化为具有实用价值的手性γ-氨基丁酸化合物。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Aryloxide-Facilitated Catalyst Turnover in Enantioselective α,β-Unsaturated Acyl Ammonium Catalysis
Angew. Chem. Int. Ed., 2017, DOI: 10.1002/anie.201706402
导师信息
Andrew Smith
http://www.x-mol.com/university/faculty/3297
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!










































 京公网安备 11010802027423号
京公网安备 11010802027423号