Ni催化端烯的1,1-双硼化
相比于格氏试剂、锂试剂等有机金属试剂,烷基硼酸酯对水、氧不敏感,易于操作,而且可以立体专一地转化为C-C键和C-X(X = 杂原子)键。因此,烷基硼酸酯作为有机合成中的重要中间体可用于构建多种不同的反应,而烷基硼试剂的制备方法一直以来都是有机化学家关心的问题。从廉价易得的烯烃出发,单硼化、1,2-双硼化、1,1,1-三硼化反应在过去均有所报道(图1a)。1,1-双硼化反应的产物同样具有非常重要的应用,该类化合物可通过特定的催化方式实现立体选择性的转化(图1b),还可用于同时构建两组C-C键(图1c)以及引入多种其他官能团(图1d)。在以往的工作中,从双卤代物、端炔、卡宾、C-H键活化和烯基硼烷出发制备1,1-双硼烷的途径均已实现(图1f),然而以烯烃为原料合成1,1-双硼烷一直以来都没有报道。最近,中国科学技术大学的傅尧教授(点击查看介绍)、肖斌副教授(点击查看介绍)在Nature Communications 上报道了Ni催化条件下末端烯烃的1,1-双硼化反应。该方法具有良好的化学选择性和区域选择性,并可用于大规模合成偕二硼化合物(图1e)。该论文第一作者为博士生李磊。
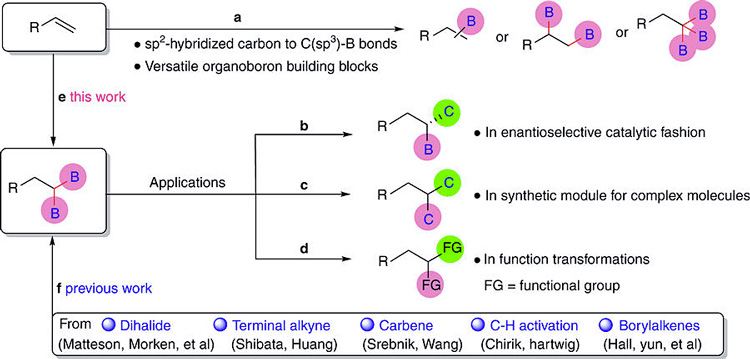
图1. 末端烯烃硼化的方法及1,1-双硼烷在合成中的应用。图片来源:Nat. Commun.
作者首先利用4-苯基丁烯(1)和B2pin2作为标准底物,对Ni催化剂、配体、碱和溶剂等反应条件进行筛选,发现使用Ni(COD)2作为催化剂、Cy-XantPhos作为配体、LiOMe/NEt3作为碱、PhMe/THF作为混合溶剂,反应能以78%的收率得到目标产物2(图2)。
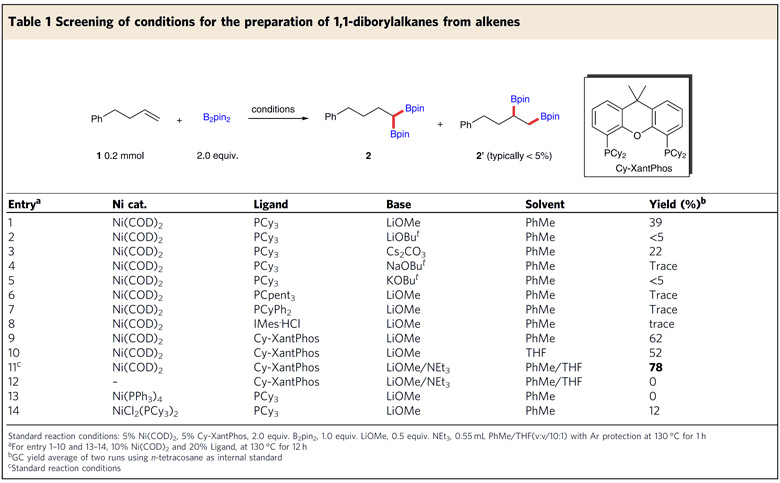
图2. 反应条件的筛选。图片来源:Nat. Commun.
得到最优条件后,作者对末端烯烃的底物适用范围进行了考察。首先,作者尝试了不同烷基取代的末端烯烃(图3),醚(8-12)、芳香杂环(13-14)、氨基(15)、酰胺(16-17)、硼酸酯(18-19)、缩酮(20)等官能团都能得到很好地兼容。B2pai2(24)也可以作为硼化试剂应用到该反应中,α位甲基取代的末端烯烃25则不能参与反应。
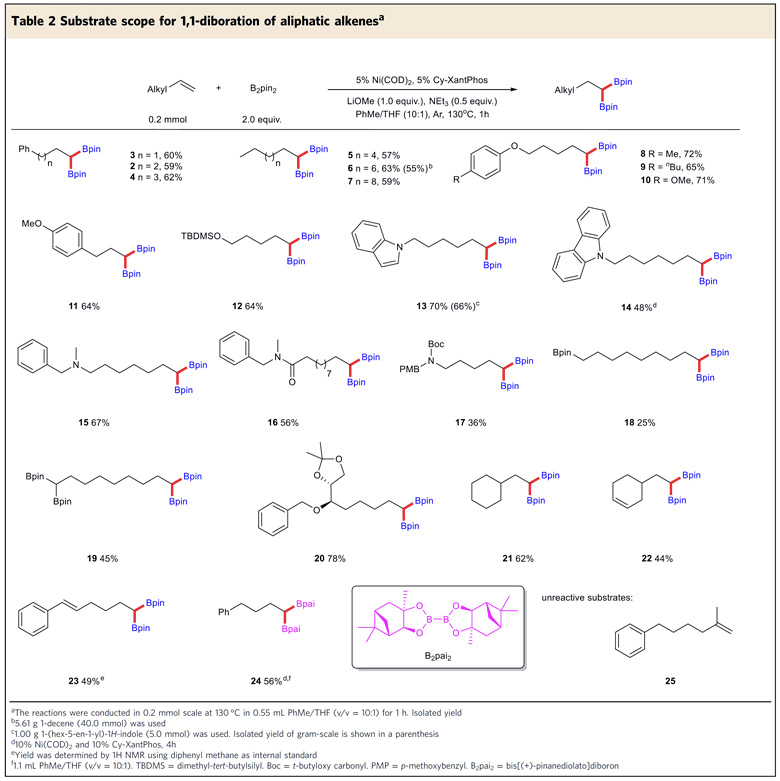
图3. 脂肪族烯烃的底物适用性考察。图片来源:Nat. Commun.
随后,作者还对乙烯基芳烃作为底物的普适性进行了考察(图4)。使用PCy3作为配体时,反应可以顺利地进行,然而芳香环上取代基的适用范围十分有限。
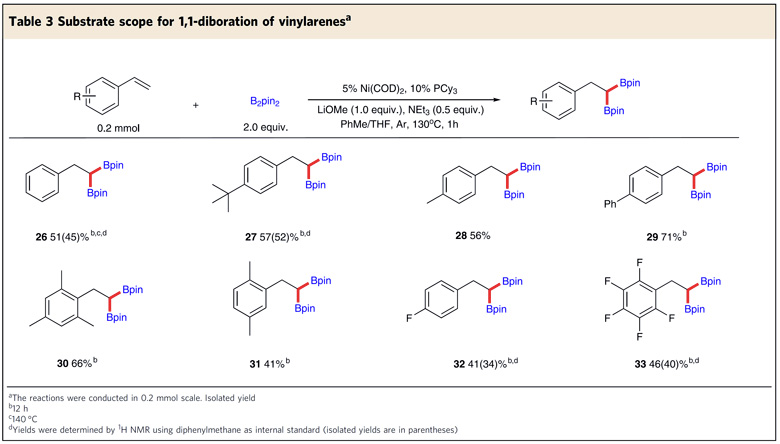
图4. 乙烯基芳烃的底物适用性考察。图片来源:Nat. Commun.
为了证明该方法的实用性,作者考察了糖类衍生物(图5a、5b)、液晶材料(图5c)和低分子量末端烯烃(图5d)的1,1-双硼化反应,并取得了满意的结果,充分说明这种方法具有很好的实用价值。
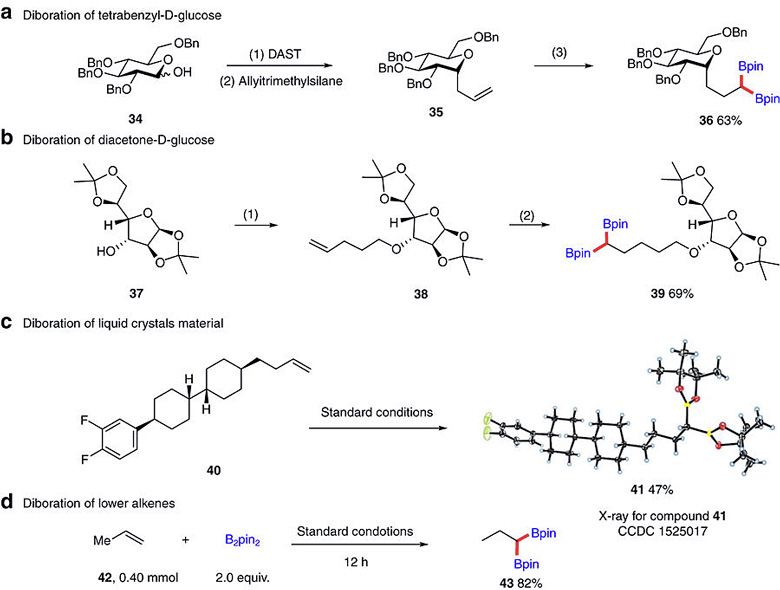
图5. 糖类衍生物、液晶材料和低分子量末端烯烃的1,1-双硼化。图片来源:Nat. Commun.
最后,作者对该反应的机理进行了一系列的研究(图6)。首先对于底物1,作者加入等物质的量的B2pin2和B2pai2设计交叉竞争实验。2、47、24的生成则表明产物中的硼原子由两分子的硼酸酯试剂提供(图6a)。作者还从氘代的底物29a-d2 出发置于标准条件下反应,产物29-d2 中苄位的氘代效率为92%。氘代实验证明了产物中苄位的氢来自末端烯烃。反应在Ni催化的条件下发生烯烃硼化后再对其氢硼化来实现烯烃的1,1-双硼化(图6b)。
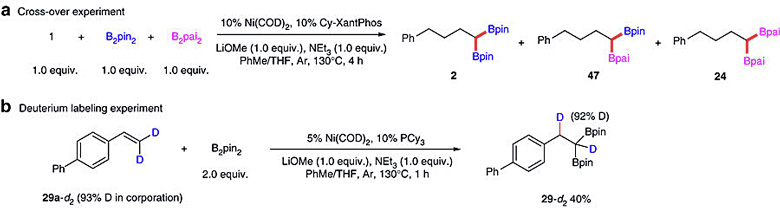
图6. 反应机理的研究:a. 交叉实验;b. 氘代实验。图片来源:Nat. Commun.
——总结——
傅尧教授和肖斌副教授等研究者发展了Ni催化末端烯烃的1,1-双硼化反应,该反应具有良好的化学选择性和区域选择性,官能团兼容性好。作者还成功地将该方法应用于糖类化合物、液晶材料和低分子烯烃的双硼化反应中,证明了该反应的应用前景。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Nickel-catalyzed synthesis of 1,1-diborylalkanes from terminal alkenes
Nat. Commun., 2017, DOI: 10.1038/s41467-017-00363-4
导师介绍
傅尧
http://www.x-mol.com/university/faculty/14770
肖斌
http://www.x-mol.com/university/faculty/45869
(本文由ChemHP供稿)
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号