硼酸修饰增强喹哚啉衍生物的体内外抗甲型流感病毒
甲型流感病毒(Influenza A Virus,IAV)的爆发流行不仅给人类的生命健康带来严重威胁,还会带来巨大的经济损失。目前上市的抗IAV药物大多副作用明显、易产生耐药性。因此,研究低毒高效的新型抗IAV药物势在必行。硼酸修饰的化合物能够结合细胞表面的糖链分子,从而改变其细胞内的定位及毒性,而硼酸修饰的化合物GSK5852还能显著地抑制HCV的RNA聚合酶活性,且已进入临床研究。IAV表面的血凝素蛋白HA和神经氨酸酶蛋白NA都是糖蛋白,病毒入侵过程需要糖链作为受体。因此,硼酸修饰的化合物可作用于细胞表面的糖链或病毒表面的糖链,从而抑制IAV的感染过程,有望被开发为一种新型的抗IAV药物。
中国海洋大学医药学院的江涛教授、王伟副教授与青岛大学附属医院的张丽娟教授等人组成的研究团队合作,利用抗IAV的分子和细胞模型,结合活细胞成像等技术对不同硼酸修饰的化合物进行抗IAV活性筛选,发现一种喹哚啉硼酸衍生物7a具有显著的体外抗IAV作用(选择指数SI > 56.0),并证明硼酸基团的引入不仅降低了喹哚啉衍生物的毒性,还大大提高了其抗IAV效果,相比未修饰的5a提高了约40倍。
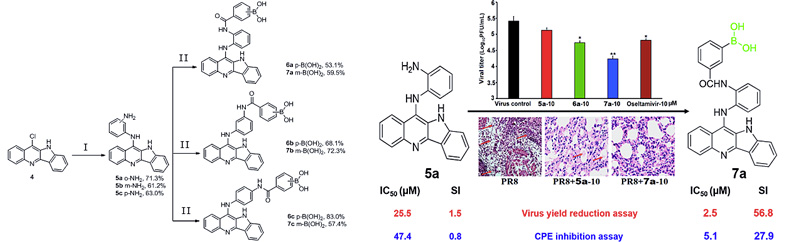
图1. 硼酸修饰增强喹哚啉衍生物的抗IAV作用
化合物7a对H1N1和H3N2亚型的流感病毒都具有很好的抑制作用,优于一线药物奥司他韦。研究表明7a能够定位于细胞质并延缓病毒RNP的入核过程,通过结合病毒NA蛋白和下调宿主细胞的NF-κB、PI3K/Akt等信号通路来抑制病毒的感染和复制。他们利用计算机分子对接等技术进一步证实硼酸修饰可能有助于增强喹哚啉衍生物与病毒NA蛋白或细胞表面糖链的作用,从而干扰IAV的侵染。化合物7a的灌胃给药还能显著降低鼠肺病毒滴度,减轻肺部病变,提高小鼠的生存率,优于5a和奥司他韦,为基于硼酸修饰新靶点抗IAV药物的研发提供了物质基础和理论参考。
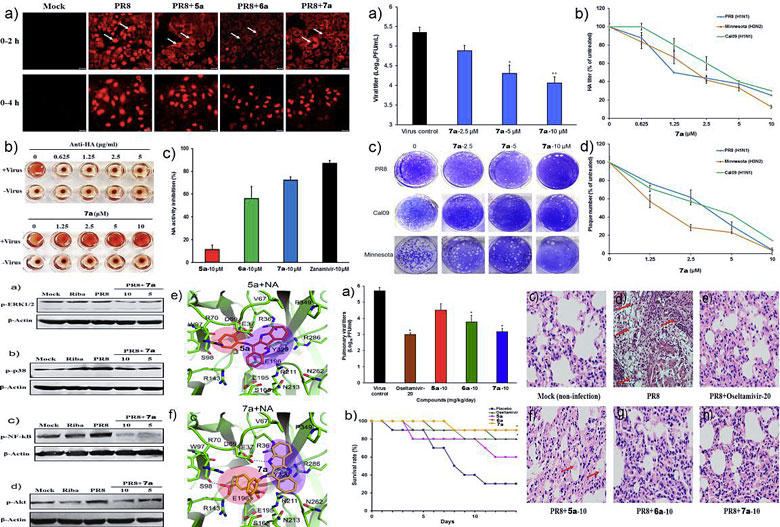
图2. 硼酸修饰的喹哚啉衍生物7a抗IAV活性及作用机制的研究
上述研究成果已于2017年3月在线发表在药物化学领域权威期刊Journal of Medicinal Chemistry 上。第一作者为中国海洋大学医药学院的王伟副教授、博士生尹瑞娟和张朦。中国海洋大学的江涛教授和青岛大学附属医院的张丽娟教授为共同通讯作者。该研究工作得到国家自然科学基金、国家海洋实验室鳌山计划及山东省博士基金等项目的资助。
该论文作者为:Wei Wang, Ruijuan Yin, Meng Zhang, Rilei Yu, Cui Hao, Lijuan Zhang, Tao Jiang
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Boronic Acid Modifications Enhance the Anti-Influenza A Virus Activities of Novel Quindoline Derivatives
J. Med. Chem., 2017, 60, 2840, DOI: 10.1021/acs.jmedchem.6b00326
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号