自焚式光敏剂用于荧光自报告的肿瘤诊疗研究
注:文末有本文科研思路分析
光动力治疗(PDT)已经成为一种非常有前途的癌症治疗方式,光敏剂是PDT的核心,因而其性质和功能对于PDT实现精准治疗起决定性作用。近日,澳门大学张宣军副教授(点击查看介绍)团队开发了激光精准控制的 “分子炸弹” 型智能光敏剂,不仅能诱导癌细胞快速胀亡,而且通过荧光变色可以自动报告治疗过程,成功实现了肿瘤诊断治疗一体化。
临床批准使用的光敏剂,如卟啉和酞菁类衍生物,已经取得了很大的突破,但是许多问题仍然限制了PDT作为一线治疗的应用。比如,临床病人治疗后,体内药物未完全代谢,身体仍处于“光敏状态”,不能接受太阳光的直射,两周内要做到避光,造成生活上的不便。其次,肿瘤乏氧的微环境严重影响了II型PDT的应用潜力。由于缺乏有效的工具监测光敏剂在体内的作用过程,使得光照时间很难控制,导致治疗不彻底或过度治疗。因此,准确评估光敏剂在何时何处起作用以及按需给予光照,对于精准治疗以及降低毒副作用具有重要意义。
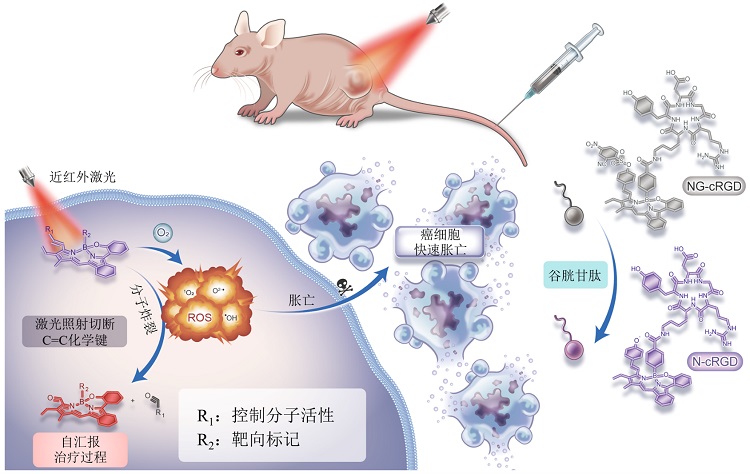
澳门大学张宣军副教授团队开发了自焚型多功能光敏剂,成功解决了上述诸多问题。新开发的光敏剂在680纳米激光照射后,产生多种活性氧(Reactive Oxygen Species,ROS),主要包括单线态氧(1O2)、羟基自由基(•OH)、超氧阴离子(O2•−),使得光敏剂分子内特定的碳碳双键高效断裂,并诱导肿瘤细胞快速胀亡。众所周知,小分子光敏剂很难主动富集在肿瘤区域。他们考虑到肿瘤细胞高表达的整合素αvβ3,于是在光敏剂上偶联了可以特异性靶向整合素αvβ3的环肽cyclo(Arg-Gly-Asp-D-Tyr-Lys)(cRGD),相关结果证明修饰后的光敏剂具有很好的肺癌细胞靶向能力。此外,为了进一步提高生物安全性,研究团队对光敏剂进行预先灭活。他们基于肺癌细胞含有高浓度的谷胱甘肽(GSH)的特点,以GSH特异性响应的2-氰基-4硝基苯磺酰基团对光敏剂进行修饰以抑制其活性,并猝灭荧光。灭活后的光敏剂在激光照射下是惰性的,因此即便有少量脱靶的分子也不会造成安全隐患。灭活的光敏剂靶向富集到肺癌细胞后,细胞内高表达的GSH有效激活光敏剂,并通过近红外荧光准确地反映肿瘤位置和最佳光照时间点。
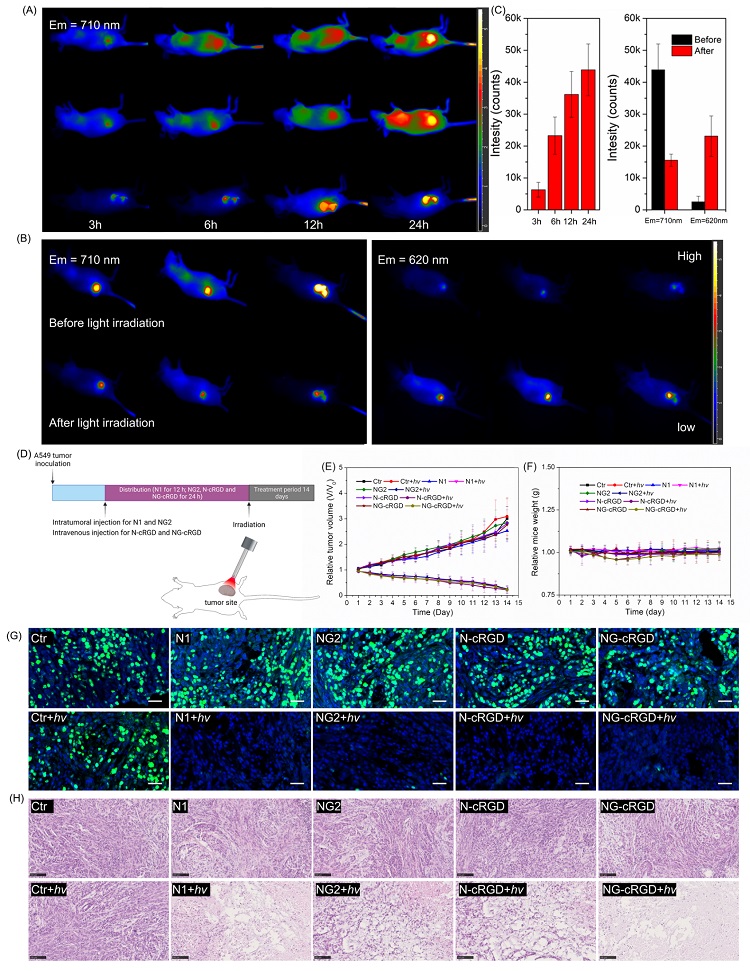
A549肺癌荷瘤小鼠活体成像结果表明,710纳米处近红外荧光的增强说明GSH能成功地激活光敏剂;620纳米处荧光的增强说明光照后碳碳双键断裂,同时也可以反映细胞胀亡的启动。因此,通过光敏剂自身产生的双色荧光可以实时反馈诊断和治疗过程。经过光动力治疗后,A549荷瘤小鼠肿瘤体积明显减小甚至有些会消除,肿瘤细胞的增殖也受到了明显的抑制。该研究表明,自焚式光敏剂对荧光自报告的肺癌光诊疗以及原位监测是非常可靠和有效的,为加速发展简易智能型有机光敏剂在未来精准肿瘤学中的应用提供了新的思路。
这一成果以封面文章发表在J. Am. Chem. Soc.上,文章第一作者为汪春飞博士。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Self-Immolative Photosensitizers for Self-Reported Cancer Phototheranostics
Chunfei Wang, Yongjie Sun, Shaojuan Huang, Zixiang Wei, Jingyun Tan, Changfeng Wu*, Qiang Chen*, and Xuanjun Zhang*
J. Am. Chem. Soc., 2023, DOI: 10.1021/jacs.3c01666 (Front Cover Paper)
科研思路分析
Q:本研究的出发点是什么?
A:从上述介绍中可知,目前PDT存在许多问题,限制了PDT在临床上的广泛应用,所以本研究的出发点是解决光敏剂存在的问题并开发智能小分子光敏剂。针对肿瘤微环境乏氧的问题,我们采用了N2O类型的苯并吡咯亚甲基硼配合物作为母核结构,光照后可高效产生多种ROS,主要包括1O2、•OH和O2•−。为了提高诊疗效果和生物安全性,我们将光敏剂进行了双重改造:(1)偶联环肽cyclo(Arg-Gly-Asp-D-Tyr-Lys)(cRGD)以促进光敏剂在肿瘤组织的富集;(2)光敏剂预先灭活:利用GSH特异性切断的2-氰基-4硝基苯磺酰基团来灭活光敏剂。灭活后的光敏剂即便在激光照射下也是惰性的,大大降低了脱靶光敏剂对正常组织造成的安全隐患。通过有针对性的分子修饰和剪裁,可以赋予光敏剂更多的功能以规避PDT中的诸多问题,从而实现精准治疗。
Q:本研究开发的自焚式光敏剂的优势是什么?
A:自焚式光敏剂在光照后自身产生的ROS介导特定的碳碳双键断裂,分子中共轭体系的变化使得荧光信号发生变化,因此研究人员可以通过荧光信号的变化实时监测光敏剂在体内的作用过程。治疗后光敏剂的代谢过程对于PDT也是至关重要的,如果治疗结束后的光敏剂不能被及时代谢并排出体外,身体处于光敏状态,会造成正常组织细胞的光毒性。本工作中新开发的自汇报型光敏探针,在光照后可高效杀死癌细胞的同时迅速降解为低毒的化合物(IC50 > 100 μM), 大大降低了治疗后引起的安全隐患。在整个诊疗过程中,光敏剂自身产生的双色荧光还可以准确反馈其在体内的剩余量。
Q:研究中遇到了哪些挑战?
A:本研究面临的主要挑战是光敏剂的合成。开发的多功能光敏剂需要连接环肽cyclo(Arg-Gly-Asp-D-Tyr-Lys)(cRGD),和GSH能特异性切断的2-氰基-4硝基苯磺酰基团,因此合成的过程会相对比较复杂,同时还要考虑到分离纯化过程中化合物的稳定性。在尝试多种基团的偶联方法后,最终确定了目前的最佳合成路线。其次,合成的多功能光敏剂是否具有预期的光诊疗效果,我们与南方科技大学吴长锋教授以及澳大健康科学学院陈强教授合作进行深入的研究,最终通过荷瘤小鼠活体成像和抗肿瘤研究证明新开发光敏剂的作用与预期一致。
Q:本研究有哪些有意义的科学发现?
A:本研究有意义的科学发现之一是新开发的光敏剂在光照后可高效产生多种ROS,主要包括1O2、•OH和O2•−,引发自身炸裂释放出红色荧光产物,因此该新型光敏药物可形象地比喻成激光可控制的“分子炸弹”。第二个发现是光敏剂能诱导肿瘤细胞快速胀亡。目前大部分光动力学治疗诱导癌细胞程序性凋亡,而胀亡是一种新颖的非凋亡式的细胞死亡方式,目前在PDT研究中非常少见,在抗肿瘤研究中得到了广泛的关注。
张宣军副教授团队
https://www.x-mol.com/university/faculty/68969
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号