利用捆绑式原位点击化学发现细胞可渗透的O-GlcNAc转移酶抑制剂
作为一种哺乳动物细胞必需的酶,O-GlcNAc转移酶(O-GlcNAc transferase,OGT)将N-乙酰氨基葡萄糖从UDP-N-乙酰氨基葡萄糖(UDP-GlcNAc)转移到蛋白质的丝氨酸和苏氨酸(Ser/Thr)羟基上。能够被O-GlcNAc糖基化的蛋白质广泛存在于细胞核、细胞质和线粒体中,包括多种转录因子、肿瘤抑制蛋白、激酶、磷酸酶和组蛋白修饰蛋白。这种蛋白质翻译后的修饰对许多细胞信号通路具有调节作用,并与多种重大疾病的发生和发展密切相关,包括胰岛素的耐受性、糖尿病的并发症、癌症、心血管疾病和阿尔兹海默病(Alzheimer's disease)等等。由于OGT的重要性,目前已报道了多种小分子能够在细胞内抑制OGT,包括四氧嘧啶(尿嘌呤模拟物)、BADGP(N-乙酰氨基半乳糖模拟物)、Ac4-5SGlcNAc(代谢前体)、BZX(中性的磷酸模拟物)和OSMI-1(喹啉-6-磺酰胺衍生物)。然而,大多数化合物并不能高效、选择性地抑制OGT。四氧嘧啶同时会抑制O-GlcNAc糖苷酶(O-GlcNAcase,OGA);BADGP会引起黏蛋白O-糖基化的紊乱;Ac4-5SGlcNAc会影响细胞表面多种类型的糖链,包括黏蛋白上的O-糖链;BZX是一个不可逆抑制剂,因为过于活泼而不能成为选择性OGT抑制剂;OSMI-1处理过的细胞,活力下降近50%。所有这些抑制剂在细胞水平均需要毫摩尔或者微摩尔浓度。因而,人们迫切需要发展全新骨架的OGT抑制剂。
在药物发展策略中,靶标导向合成(Target-guided synthesis,TGS)是一种很有前途的方法,分为动态组合化学(Dynamic combinatorial chemistry)和动力学控制的靶标导向合成(Kinetically controlled TGS),捆绑(Tething)和原位点击化学(In situ click chemistry)分别是两类方法的代表性策略。前者是一种基于二硫键交换的捕获方法,蛋白质表面的巯基能够与含有二硫键的小片段形成二硫键;后者利用不可逆的点击化学反应将两个活性模块组装成更有潜力的抑制剂。结合两种方法的优势,普遍适用策略的“捆绑式原位点击化学(Tethering in situ click chemistry,TISCC)”可用来发现OGT抑制剂。
在新的策略中,一种构建模块M含有两个活性基团X(ICH2CO)和A(N3),而另一种构建模块N则含有一个活性基团Y(C≡CH)。在没有催化剂的情况下,两组构建模块M和N中的活性基团A(N3)和Y(C≡CH)不发生反应或者反应速率极小。首先,靶蛋白和前一种构建模块M共孵育,在一些半胱氨酸位点上“捆绑”活性基团A(N3);然后,无需分离将后一种模块N加入到反应混合物中,在合适的位点发生经典的原位点击化学反应,倘若两种构建模块M和N中的活性基团A(N3)和Y(C≡CH)空间上接近,便会加速彼此间的不可逆反应形成共价键(三氮唑);最后,利用SDS-PAGE将蛋白质与小分子分离,胰蛋白酶水解,并通过LC/MS/MS找出修饰的肽段。新候选物的结构能够从修饰的精确分子量推断出来(图1a)。此后,利用铜或者钌催化叠氮-炔的环加成反应(CuAAC/RuAAC)合成新的候选物用于活性评价(图1b)。与“捆绑”和经典的原位点击化学相比,新的策略使用更普遍适用的构建模块,检测蛋白质片段而不是整个蛋白质或者配体本身,因此能够同时筛选多个结合口袋。
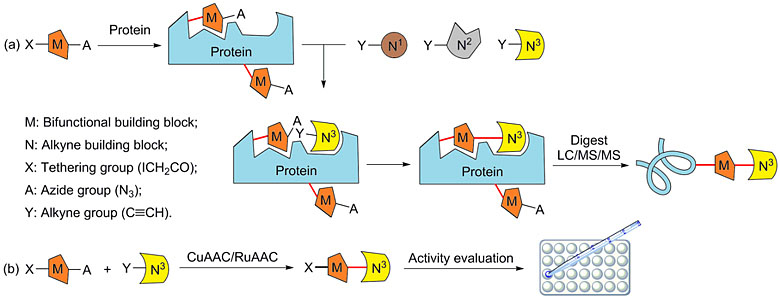
图1. 捆绑式原位点击化学(TISCC)。(a)筛选构建模块发现新的候选物;(b)合成新的候选物用于活性评价。
在该研究中,作者利用捆绑式原位点击化学(TISCC),将对叠氮碘乙酰苯胺作为双功能的构建模块M,对61种炔基构建模块N进行筛选,经过后续的化学改造发展了两种细胞可渗透的OGT抑制剂(APNT和APBT)(图2)。这两种抑制剂能够在细胞中降低O-GlcNAc糖基化水平,而没有明显的细胞毒性。对于OGT不寻常的非竞争性抑制有助于发现新的抑制剂和探索OGT的调节机制。
传统的原位点击化学通常使用高亲和力的构建模块(IC50≤ 6.4 μM)。当前体的IC50在微摩尔水平,新产生的抑制剂活性能够提高5–700倍。点击化学也曾用于发现岩藻糖转移酶抑制剂,以GDP的炔衍生物(Ki= 47 μM)出发,无需分离直接进行原位筛选。然而,二磷酸桥的结构阻止得到的抑制剂进入细胞。在本文中,APNT(IC50 = 66.7 ± 0.8 μM)由两个中性的构建模块组成,这两个构建模块对OGT的抑制活性很弱(IC50 > 4000 μM)。新产生的抑制剂活性提高超过60倍,在细胞内的作用与阳性对照BZX相仿。因而,TISCC能够用来筛选活性很弱的前体,这些前体的IC50甚至在毫摩尔水平。这一成果近期发表在Journal of Medicinal Chemistry 上。
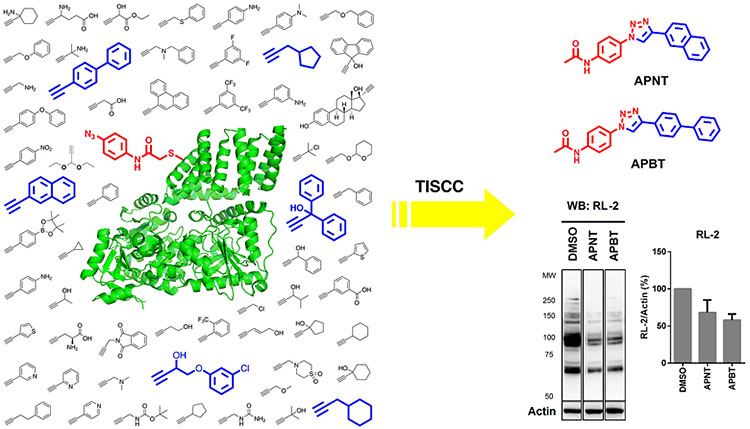
图2. O-GlcNAc转移酶抑制剂的发现
该论文作者为:Yue Wang, Jingjing Zhu and Lianwen Zhang
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Discovery of cell-permeable O-GlcNAc transferase inhibitors via tethering in situ click chemistry
J. Med. Chem., 2017, 60, 263, DOI: 10.1021/acs.jmedchem.6b01237
作者简介

王玥博士1985年出生于辽宁省,2006年在北京大学药学院获得学士学位,2006年到2012年在北京大学天然药物及仿生药物国家重点实验室叶新山教授课题组攻读硕士和博士学位,此后加入中国科学院大学化学与化工学院任讲师,2017年回到北京大学药学院叶新山教授课题组做博士后,主要研究方向为糖化学生物学和糖类药物的发现。
http://www.x-mol.com/university/faculty/23718
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号