Gregory Fu新作:Ni催化的不对称烷基-烷基交叉偶联
过渡金属催化的烷基亲核试剂和非活化的烷基亲电试剂的交叉偶联反应是构建有机化合物的重要方法。但该类反应存在两方面的挑战:(1)能否成功构建所需的C-C键;(2)化合物立体化学能否得到有效控制。由易得的消旋化合物在催化剂的作用下转化为单一构型的手性化合物日渐引起人们的关注,而由于成键困难,到目前为止使用非活化的二级亲电试剂来合成含相邻两个手性中心的不对称烷基-烷基交叉偶联反应的报道十分少见(图1)。
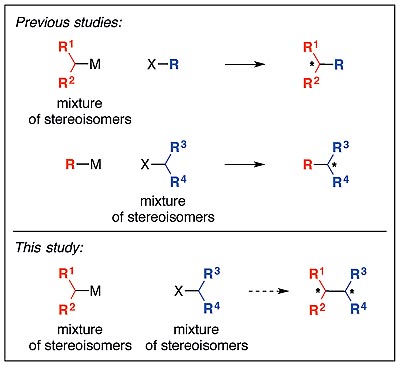
图1. 烷基-烷基交叉偶联。图片来源:Angew. Chem. Int. Ed.
吡咯烷骨架广泛存在于药物分子和天然产物中,成为有机合成化学家们高度关注的焦点。来自美国加州理工学院的Gregory C. Fu教授报道的镍催化的N-Boc-吡咯-α-锌试剂与非手性烷基亲电试剂的交叉偶联反应是很有效的方法之一,最终构建含一个手性中心的手性吡咯烷化合物(图2)。最近,Gregory C. Fu教授将其拓展到合成含两个相邻立体中心的化合物。
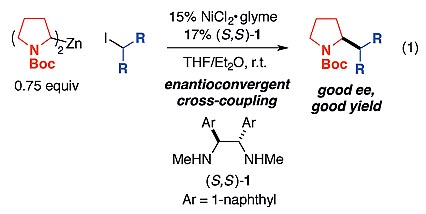
图2. 手性吡咯烷的合成。图片来源:Angew. Chem. Int. Ed.
作者对反应条件没有过多的筛选,使用2013年JACS 报道的条件(J. Am. Chem. Soc., 2013, 135, 10946-10949),能以92%的对映选择性和91/9的非对映选择性得到产物。当使用Ni(acac)2作为镍源时,对映选择性略有提升(93% ee,92/8 d.r.),同时锌试剂的量可降到0.6当量。作者随后对更多的亲电试剂进行考察,不管是环己烷衍生物还是吡喃衍生物,不管亲电试剂的顺反比例如何,都能以优秀的产率(75-94%)、良好的对映选择性(91-93%)和非对映选择性(85/15>99/1)得到产物(图3)。
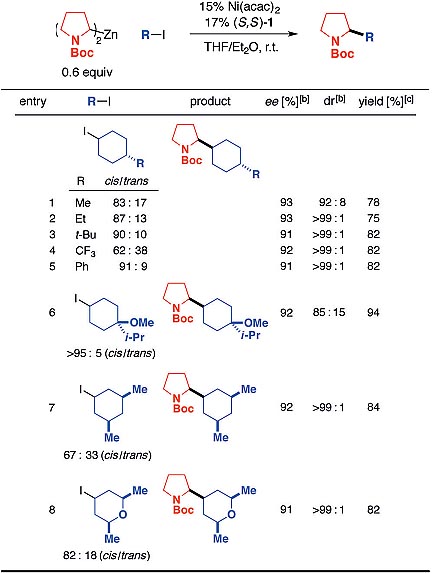
图3. 底物拓展。图片来源:Angew. Chem. Int. Ed.
作者不仅考察了非手性的亲电试剂,还考察了手性的亲电试剂。从结果可以看出,不管是简单还是复杂的手性亲电试剂,该反应都能顺利发生,以良好的产率(60-90%)和非对映选择性(86/14-97/3)得到目标产物。当使用(R, R)-1作为配体时,也能得到类似的催化结果,不同的是与氮相连的碳手性中心的构型不同(图4)。

图4. 底物拓展。图片来源:Angew. Chem. Int. Ed.
作者发现不管是使用顺式的亲电试剂还是反式的亲电试剂,得到的目标产物最终都是反式的。当作者在反应部分转化后淬灭该反应时,未反应的亲电试剂的构型发生了异构化。为此,作者给出了两个可能的原因:(1)反应过程中产生的碘化锌与亲电试剂发生了SN2反应;(2)烷基碘向Ni催化剂发生可逆碘转移反应。作者随后进行了验证试验,发现两个亲电异构体(顺式和反式)在碘化锌的存在下于THF/Et2O中室温反应48小时,不会发生任何的相互转化。最终作者倾向于反应过程中发生了烷基自由基与Ni之间的可逆的碘转移(图5)。
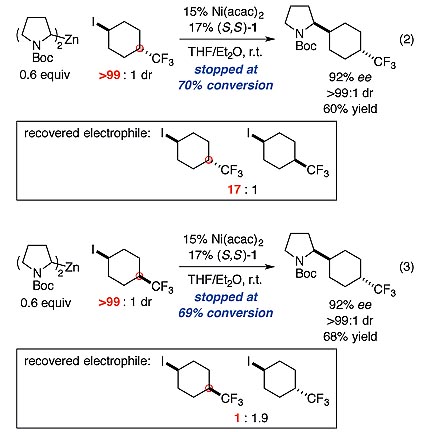
图5. 亲电试剂构型的研究。图片来源:Angew. Chem. Int. Ed.
——总结——
Gregory C. Fu课题组报道了Ni催化的烷基-烷基交叉偶联反应,高效构建了含两个相邻立体中心的手性吡咯烷化合物。由于相邻立体中心的手性化合物广泛存在于重要的有机分子中,该类方法在接下来必将得到广泛的关注和研究。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Control of Vicinal Stereocenters through Nickel-Catalyzed Alkyl–Alkyl Cross-Coupling
Angew. Chem. Int. Ed., 2017, DOI: 10.1002/anie.201702402
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号