《Science》:化学手段给癌症关键蛋白贴上“死亡”标签
在人类与癌症的长期斗争中,一个有效的策略是找到与癌症的发展有关的蛋白质,然后对其设法抑制以达到控制癌症的目的。然而,有很多这样的蛋白质却很难被药物直接作用。
最近,哈佛大学丹娜法伯癌症研究所James E. Bradner博士领导的科学家团队,设计出了一种新的化学策略,提供了一种通用的技术,在原则上可以有选择性地降解任何目标蛋白质。
在这种策略中,该团队将能与目标蛋白质结合的配体通过化学键与另一种以邻苯二甲酰亚胺为基础的分子连接起来,这种分子能够“劫持”一种cullin-RING泛素连接酶的组分cereblon(CRBN),从而启动细胞内的蛋白质降解机制,将目标蛋白质清除。
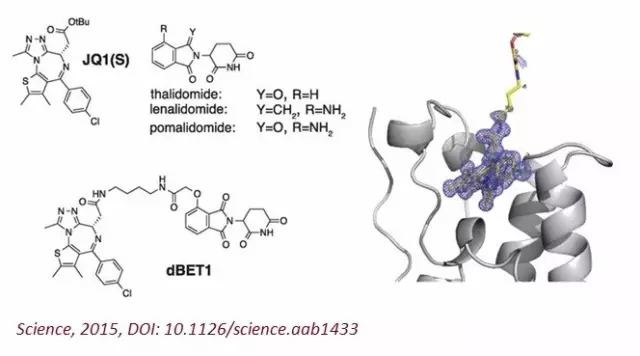
作为对这一新概念的验证研究,该团队将这种技术得到的化合物dBET1(上图)用于选择性降解一种与癌细胞的生长和存活有关的转录辅助激活因子BRD4,成功地延迟了小鼠的白血病发展。
在历史上,以邻苯二甲酰亚胺为基础的药物出现在20世纪50年代。其中最引人注目的是沙利度胺,这种药物最初被作为镇静剂,但由于其臭名昭著的灾难性致畸效果使其被从市场撤回。近来,邻苯二甲酰亚胺已成功的被重新用于治疗麻风结节性红斑、多发性骨髓瘤(MM)和骨髓增生异常综合症。正是在研究这种作用机制的过程中,这个研究团队研发出了这种用化学手段为目标蛋白做死亡标记的新型抗癌技术。
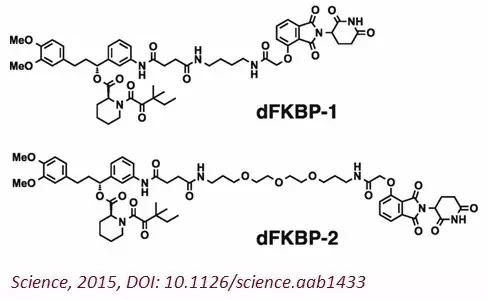
用同样的策略,该团队还研制出了类似作用机理的化合物(上图),使胞浆蛋白FKBP12也能够被选择性地降解清除,显示出了这种技术“指哪打哪”的强大效果。
这一研究成果发表在《Science》上。
http://www.sciencemag.org/content/348/6241/1376.abstract
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号