直接不对称C-酰化反应及季碳手性中心的构建
手性季碳中心是一种广泛存在于大量天然产物和药物分子中的重要结构砌块,而不对称酰基化反应是构建手性季碳中心的有效方法之一。不对称酰化反应主要通过羧酸衍生物、醇、硫醇、胺及酰胺等的酯化和酰胺化并以(动态)动力学拆分或不对称去对称化的方式实现。相比于O-酰化、S-酰化及N-酰化反应,C-酰化方面的研究相对较少。而到目前为止,仅有间接不对称酰基化如烯醇酯的Steglich和Black重排反应以及烯醇硅醚的C-酰化反应有所报导。这类反应需要额外的步骤预先制备O-酰基或O-硅基中间体,而且在C-酰化过程中需要克服较大的能垒断裂O-酰基键或O-硅基键,这限制了反应的效率和底物的范围。因此,从简单原料(烯醇或含α-H的羰基化合物)高效经济地一步得到目标产物的直接C-酰化反应具有较高的研究意义和应用价值。
上海交通大学的张万斌教授(点击查看介绍)研究团队延续前期亲核有机分子催化剂的研究工作,发展了一种手性双环咪唑催化剂OAc-DPI催化的3-取代苯并呋喃酮衍生物发生直接不对称C-酰化反应。该方法允许在较低温度下高收率高对映选择性地得到具有手性季碳中心的3,3-双取代苯并呋喃酮(如下图所示)。
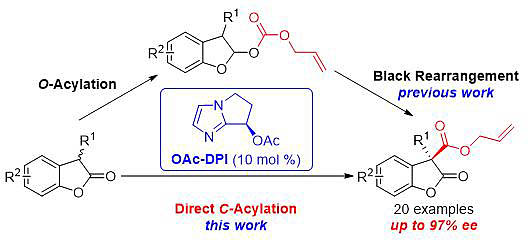
他们通过对比不同温度下一系列实验数据推测这一反应的机理是经过直接C-酰化过程而不是先经过O-酰化再进行酰基重排。对于反应中各个过渡态和最终产物的DFT计算结果也验证了这一推断的合理性。
这项工作发表于Chem. Commun. 上,第一作者是王沫,张万斌教授和张振锋副研究员为共同通讯作者。
该论文作者为:Mo Wang, Xiao Zhang, Zheng Ling, Zhenfeng Zhang and Wanbin Zhang
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Direct enantioselective C-acylation for the construction of a quaternary stereocenter catalyzed by a chiral bicyclic imidazole
Chem. Commun., 2017, 53, 1381-1384, DOI: 10.1039/c6cc09451a
导师介绍
张万斌
http://www.x-mol.com/university/faculty/12592
课题组主页
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号