立体可控地合成天然产物Kalihinol C
Kalihinols家族天然产物是一类具有复杂骨架结构和官能团的异氰萜类(isocyanoterpenes,ICT)活性分子。其中Kalihinol A具有高效的抗恶性疟原虫活性,其EC50值可达1 nM,不过其作用机制尚不十分清楚。前人对于Kalihinols家族天然产物的合成也进行了一些研究,精确地控制高度官能团化骨架中手性中心成为合成的难点。近期,美国斯克里普斯研究所(The Scripps Research Institute,TSRI)的Ryan A. Shenvi教授在JACS 上发表文章,报道了简洁高效、立体可控地合成Kalihinol C的方法。其亮点包括:新的杂原子dendralene合成子的使用、原位烯烃异构化以及新的合成异氰的方法。
近年来,Shenvi课题组利用新的dendralene以高非对映选择性的Diels-Alder反应为关键步骤合成了amphilectene(J. Am. Chem. Soc., 2012, 134, 19604)和adociane(J. Am. Chem. Soc., 2016, 138, 7268)两种异氰萜分子,考虑到amphilectenes和Kalihinols结构上的对应关系,作者希望模仿可能的生源合成途径,将中间体4中的氧亲核试剂嵌入dendralene中,进而以基于dendralene的方法实现Kalihinol的全合成。

图1. Kalihinol家族天然产物及可能的生源合成途径。图片来源:JACS
如图2所示,作者首先从乙酰乙酸叔丁酯7出发,经缩合反应得到化合物8,进而在TBSOTf作用下形成TBS保护的烯醇硅醚,并发生酯交换得到杂原子的dendralene合成子5。另一方面,作者由化合物9出发,经亲核试剂进攻,原位硒化,并进一步氧化/消除得到磷酸二乙酯取代的端烯6作为亲双烯体。
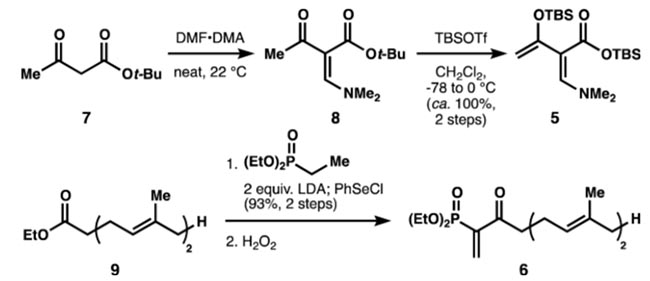
图2. D-A反应的前体5和6的合成。图片来源:JACS
化合物5和6在氢氟酸的作用下脱除TBS保护基,并发生分子间Diels-Alder反应,烯醇异构化后β-位的二甲氨基发生消除得到α,β-不饱和酮。随后羧酸负离子作为亲核试剂进攻化合物6中间的双键(见图1中的合成子4),产生的碳负离子发生Michael加成反应并进一步互变异构得到三环化合物10。在LiCl加热的条件下10发生类似Krapcho反应脱掉磷酸酯基,甲基格氏试剂进攻酮羰基得到三级醇,最后在KOH碱性条件下水解内酯并脱羧得到二醇化合物11,该过程可以以克级规模制备。接着酮羰基发生Wittig反应转化为端烯,在DMSO、KOt Bu或者DMSO、KH条件下经过渡态12发生动力学控制的烯烃异构化得到化合物2a,2a在钒氧化剂条件下先发生环内双键环氧化,随后缓慢发生侧链双键环氧化,羟基作为亲核试剂进攻侧链环氧烷得到四氢呋喃片段和三级醇。反应又在碘化钠条件下发生六元环的环氧开环得到碘化醇19,金属锌脱卤并进一步发生消除得到化合物15(机理见图4)。15侧链的醇羟基经三氟乙酸酐修饰,加热条件下发生消除得到端烯,环内的醇羟基与此同时发生三氟乙酰化,并在TMSCN、Sc(OTf)3作用下发生亲核取代引入异氰基,得到化合物25(具体过程见图5)。DMDO条件下六元环上的双键发生环氧化,随后在NH3、甲醇条件下发生环氧开环,最后在TfOCF2H条件下引入了另一个异氰基(Angew. Chem. Int. Ed., 2013, 52, 2092),由此简洁高效地完成了Kalihinol C的全合成。而最后三步反应也为Kalihinol类天然产物中A环异氰基的引入提供了一条高效、高化学选择性及立体选择性的途径。

图3. Kalihinol C的立体可控性全合成。图片来源:JACS
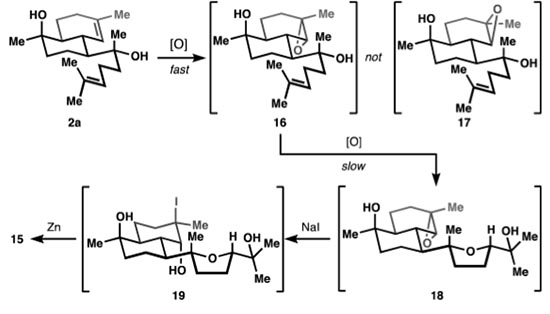
图4. 化合物15合成的机理。图片来源:JACS
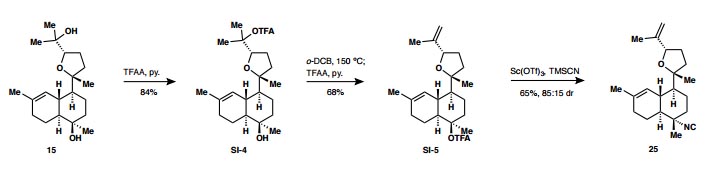
图5. 化合物25合成的机理。图片来源:JACS
——总结——
Ryan A. Shenvi课题组报道了一条简洁高效、立体可控地合成Kalihinol C的路线。该路线中的几个关键反应包括:新的杂原子dendralene合成子的使用,通过一锅法D-A/环化反应得到六元/六元反式并环,在DMSO、KOt Bu条件下原位发生烯烃异构化以及新的合成异氰的方法。这对于Kalihinol家族其它天然产物的合成具有重要意义。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文) :

Stereocontrolled Synthesis of Kalihinol C
J. Am. Chem. Soc., 2017, 139, 3647-3650, DOI: 10.1021/jacs.7b01124
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号