铑催化的烯丙基二级醇的不对称异构化反应
铑(Rh)、钌(Ru)、铱(Ir)等过渡金属的络合物,在实现烯丙醇催化异构化得到羰基化合物的反应中得到了广泛应用。Fu和Mazet等人在过渡金属催化的烯丙基一级醇的不对称异构化反应方面做出了开创性的工作,而烯丙基二级醇的不对称异构化反应目前只能通过消旋醇的动力学拆分过程进行。因此,寻找实现烯丙基二级醇的不对称异构化反应的高效方法显得尤为重要。新加坡国立大学的赵宇(Yu Zhao)教授(点击查看介绍)长期致力于研究中性条件下的不对称氧化还原反应,如通过“借氢”策略的醇的胺化反应。受以往工作的启发,他们最近报道了Rh催化剂催化的烯丙基二级醇在中性条件下氧化还原的不对称异构化反应,有效实现了α-二取代手性酮的合成(图1)。
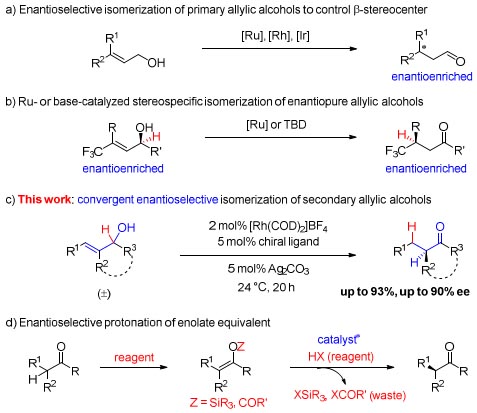
图1. 不对称烯丙醇异构化反应。图片来源:JACS
尽管烯丙基二级醇在中性条件下的氧化还原具有更好的原子经济性,然而实现这一过程存在许多潜在的困难,如底物的普适性差,对碱的选择要求苛刻,且在实现质子有效穿梭的同时,又不能引起产物的消旋。
作者首先选择烯丙醇1a作为模板底物对条件进行优化。反应以[Rh(COD)2]BF4作为Rh催化剂,Ag2CO3作为碱,考察了一系列手性膦配体。权衡产率和对映选择性,使用(R )-BINAP给出最好的结果,以90%的产率和84%的对映选择性得到产物2a。作者随后考察了不同碱对反应的影响:反应在不加入碱时不能发生;使用弱碱能以中等的对映选择性得到产物2a;加入强碱虽然能顺利得到产物2a,但产物发生消旋。最终他们得到最佳的反应条件:[Rh(COD)2]BF4/(R )-BINAP作为催化剂,Ag2CO3作为碱,甲苯作为溶剂,4Å分子筛作为添加剂在室温条件下反应(图2)。

图2. 条件筛选。图片来源:JACS
作者在最优条件下对反应的底物普适性进行了考察。首先他们固定R1与R2为苯基,考察R3取代基对反应结果的影响。从结果可以看出,当R3为不同取代基取代的苯环时,反应能以良好的产率(86-91%)和对映选择性(81-84%)得到目标产物2a-2d。作者随后考察了其它R1、R2和R3取代基对反应的影响,结果发现只要R1、R2和R3同时为芳香基团时,反应就能以良好的结果得到目标产物。而其中任意一个基团为烷基取代时,产物的对映选择性会出现较大幅度的下降(图3)。
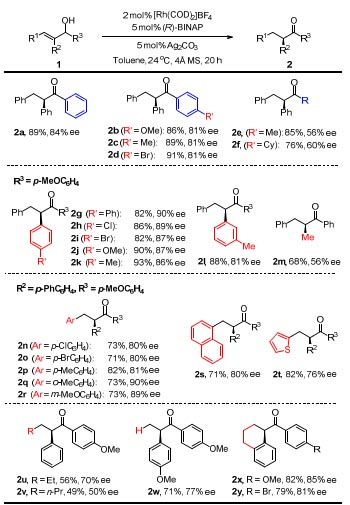
图3. 底物拓展。图片来源:JACS
作者随后考察了一系列环状烯丙醇的异构化反应,从结果可以看出,该类底物的普适性同样较为理想,以五元至七元环状烯丙醇作为底物,反应都能以良好的产率(60-93%)和对映选择性(70-84%)得到目标产物4a-4k(图4)。
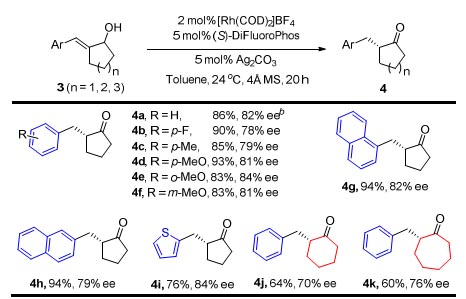
图4. 底物拓展。图片来源:JACS
作者随后进一步扩展了底物的范围,反应能以理想的结果构建含γ手性中心的手性螺环酮,反应中以[Rh(COD)2]BF4/(R )-DTBM-SegPhos作为催化剂,Ag2CO3作为碱,均三甲苯作为溶剂于室温条件下反应(图5)。
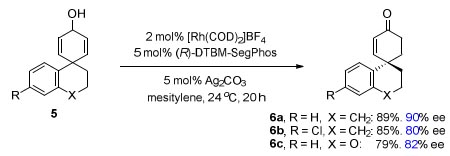
图5. 底物拓展。图片来源:JACS
作者还提出了该反应的可能机理。首先底物烯丙醇在碱的参与下去质子与Rh金属中心形成烷氧基中间体A,随后A发生β-氢消除反应得到烯酮中间体B,该中间体发生烯酮的共轭还原得到η1-Rh络合物C,中间体C通过η3-Rh络合物D异构为关键中间体E,最终E经过质子化反应得到目标产物,催化剂再次进入新的循环。为了证明该反应机理的合理性,作者随后进行了一系列氘代实验、交叉实验以及在体系中外加还原剂的验证实验,所有实验都证明反应机理中氢归属的正确性,并且证明[Rh-H]中间体不能发生分子间的还原反应(图6)。
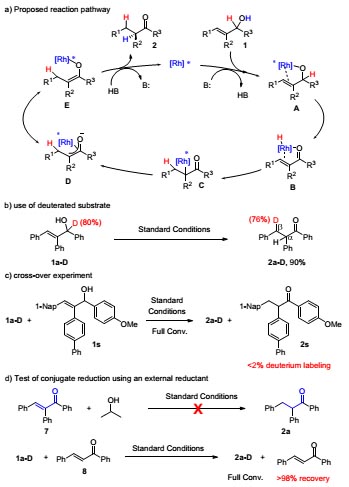
图6. 机理研究。图片来源:JACS
——总结——
赵宇教授课题组报道了第一例Rh催化的不对称烯丙基二级醇在中性条件下氧化还原的不对称异构化反应,有效实现了α-二取代手性酮的合成。该反应底物普适性较好,不仅能构建简单的脂肪链手性酮,还能构建结构复杂的螺环手性酮。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Rhodium-Catalyzed Enantioselective Isomerization of Secondary Allylic Alcohols
J. Am. Chem. Soc., 2017, 139, 3643-3646, DOI: 10.1021/jacs.7b01096
导师介绍
赵宇
http://www.x-mol.com/university/faculty/4402
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号