JACS:Pd催化芳基酯的Suzuki-Miyaura偶联
Suzuki-Miyaura偶联是目前构建C-C键最重要的方法之一。传统意义上的Suzuki-Miyaura偶联采用的亲电试剂主要是芳基卤代物及类卤代物,扩宽亲电试剂的使用范围无疑可以进一步提高反应的实用性。例如,从便宜易得的羧酸衍生物如羧酸酯出发,作为亲电试剂与亲核试剂反应,成为构建C-C键的又一思路。鉴于羧酸酯的C-O键有两种:酰基C-O键与芳基C-O键,目前从羧酸酯出发,在过渡金属参与下,反应的类型主要分为这三种:芳基C-O键对Ni氧化加成,而后接受亲核试剂的进攻得到C-C键偶联的产物(path A);酰基C-O键对Ni氧化加成,接受亲核进攻、脱碳得到C-C键偶联的产物(path B);以及近期渥太华大学Stephen G. Newman(点击查看介绍)和加州大学洛杉矶分校的Kendall N. Houk(点击查看介绍)等人在JACS报道的方法,使用基于N-杂环卡宾(NHC)的Pd催化剂,催化酰基C-O键对Pd氧化加成,而后直接与芳基硼酸偶联,实现了从羧酸酯制备芳基酮(path C)。
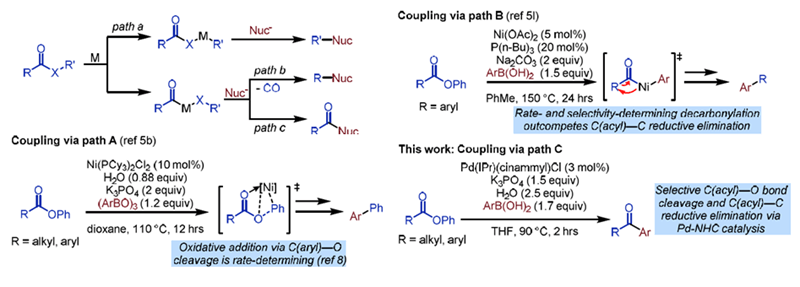
Scheme 1. 羧酸酯的交叉偶联。图片来源:JACS
作者采用羧酸酯1A和苯硼酸2a作标准底物,对条件进行优化。经优化发现,在使用Pd(IPr)(cinnamyl)Cl作催化剂,K3PO4作碱,水作添加剂,THF作溶剂,于100 ℃反应16 h条件下,反应最优(Scheme 2)。
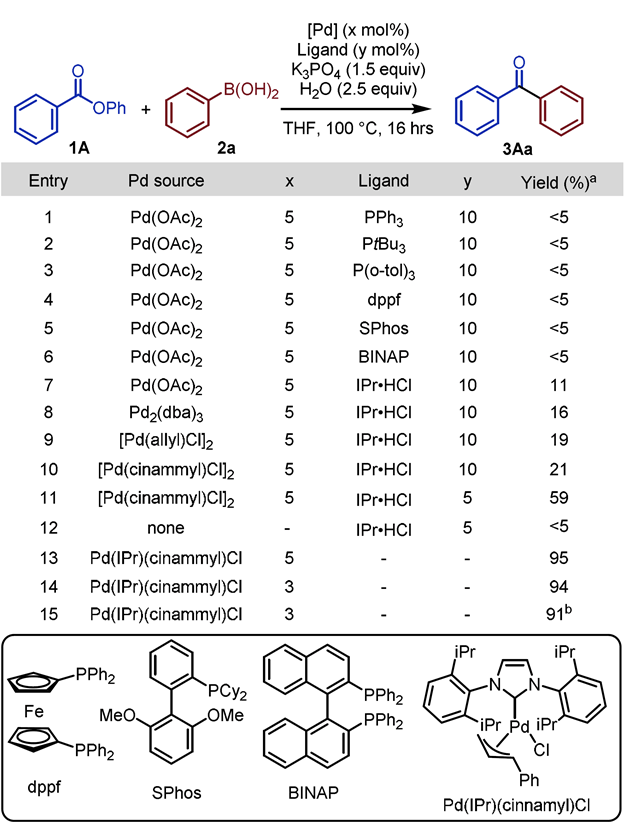
Scheme 2. 条件优化。图片来源:JACS
在该条件下,作者对羧酸酯与芳基硼酸的底物适用范围进行了考察(Scheme 3)。可以看出,底物的适用范围广,反应产率高,多种结构的二芳基酮或芳基烷基酮都可以成功的制备(Scheme 3A)。同时,在较低的温度(70 ℃)下,作者对羧酸酯与芳基硼酸的电性进行了比较。不同的电性,如OMe、H、CF3取代的羧酸酯与芳基硼酸表现了不一样的反应活性(Scheme 3B)。这表明对于特定的底物,反应的速决步骤可能不一样。
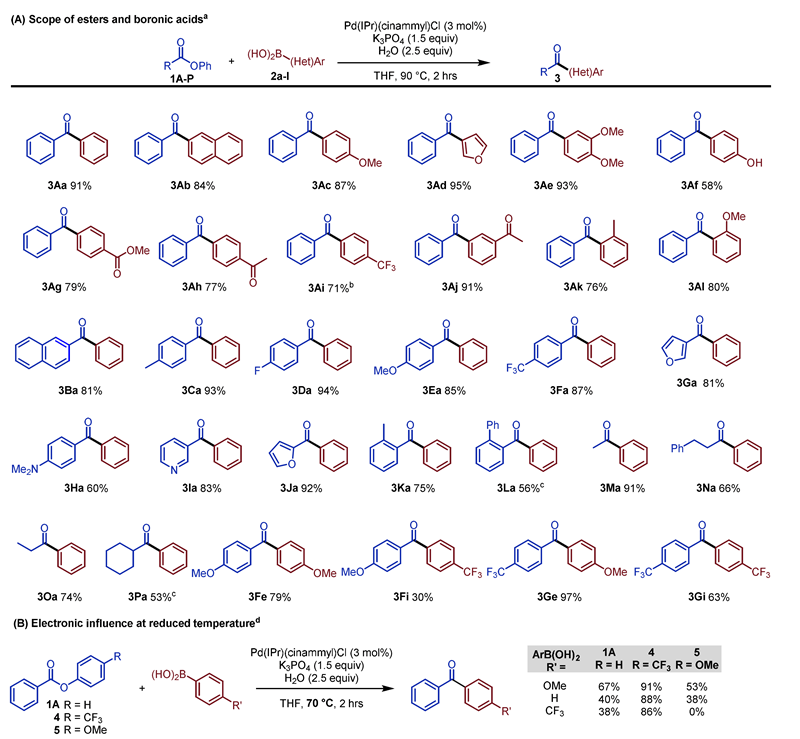
Scheme 3. 羧酸酯与芳基硼酸的适用范围。图片来源:JACS
基于不同化学键键能的差别,作者从含多种化学键的底物出发,经先后化学键活化,构建多种C-C键。如从C-S/C-O、C-N/C-O、两种不同活性的C-O选择性和C-Cl/C-O先后活化,生成多取代芳基酮(Scheme 4)。
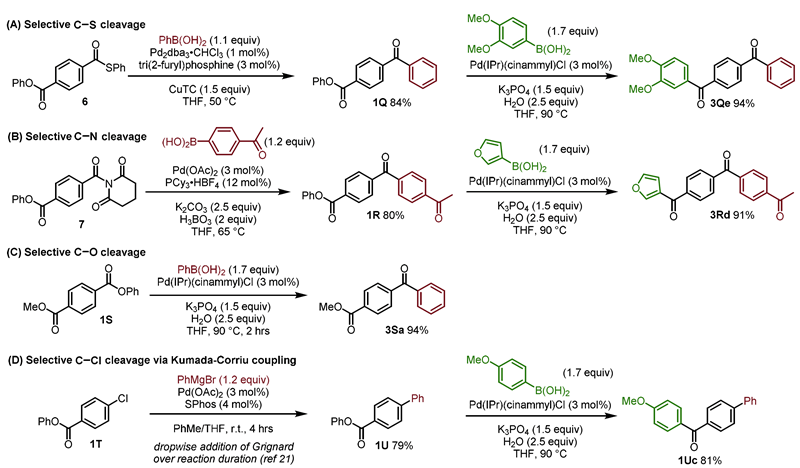
Scheme 4. 多官能团化底物中化学键选择性转化。图片来源:JACS
而后,作者还分析了使用羧酸酯作酰基化试剂的独特优势。首先,羧酸酯可以经由多种方法高效制备(Scheme 5A)。同时,通过两步反应可以从便宜易得的苯乙酮或苯甲酸制备芳香酮(Scheme 5B&C)。催化剂的调控可以制备脱碳或不脱碳的产物(Scheme 5D)。
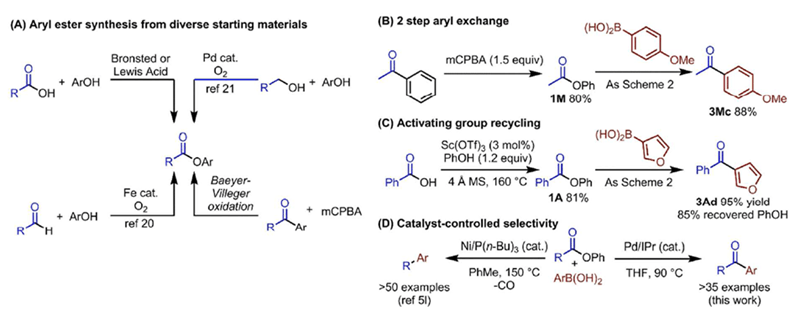
Scheme 5. 使用羧酸酯作酰基化试剂的独特优势。图片来源:JACS
最后,在Kendall N. Houk课题组的理论计算帮助下,作者对反应的历程做出了如下的解释(Scheme 6):酰基C-O键对Pd氧化加成比芳基C-O键对Pd氧化加成能垒低,因而反应经氧化加成得到TS9过渡态。随后转金属、还原消除释放产物。
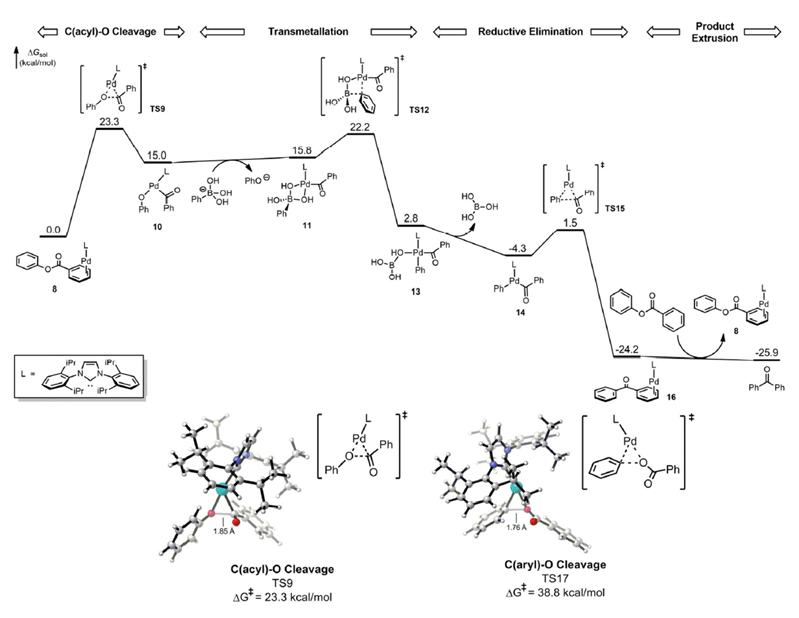
Scheme 6. 机理研究。图片来源:JACS
—— 总结 ——
在该工作,作者发展了从羧酸酯出发,酰基C-O键对Pd氧化加成,而后与芳基硼酸试剂偶联得到芳香酮的方法。该反应不同于以往羧酸酯的C-O键活化(Scheme 1)。反应产率高,选择性好。此外,作者还通过设计实验证明了该方法学的实用性。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Palladium-Catalyzed Suzuki-Miyaura Coupling of Aryl Esters
J. Am. Chem. Soc., DOI: 10.1021/jacs.6b12329
导师介绍
Stephen G. Newman
http://www.x-mol.com/university/faculty/6394
Kendall N. Houk
http://www.x-mol.com/university/faculty/843
(本文由ChemHP供稿)
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号