Lewis酸-碱相互作用控制的芳基硫醚邻位C-H硼化
芳基硫化物是天然产物和药物分子重要的结构单元,但是高效原子经济地合成该类化合物一直是一个难题。近年来,芳基C-H键活化硼化反应及硼试剂后续参与的交叉偶链、Chan-Lam-Evans偶联、氧化偶联等反应,在一定程度上解决了这一难题。目前已有文献报道了Ir/联吡啶体系催化芳基间、对位的直接C-H硼化反应。但是对于邻位的反应,依然少有文献报道,并且活化模式相对固定:1)通过导向基的辅助;2)通过外层相互作用(如氢键);3)通过Lewis酸-碱相互作用。最近,来自日本东京大学的Motomu Kanai课题组做出了突破,在Angew. Chem. Int. Ed.报道了通过Lewis酸-碱相互作用控制芳基硫化物邻位C-H硼化的反应(Figure 1)。
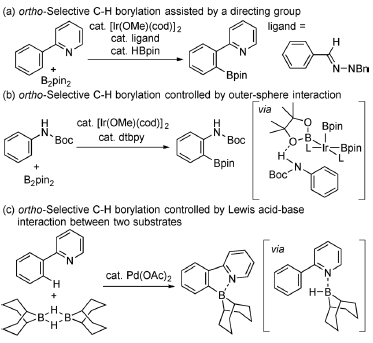
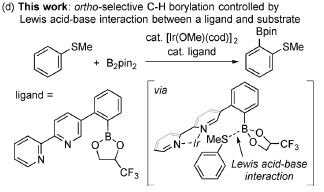
Figure 1. 邻位C-H硼化。图片来源:Angew. Chem. Int. Ed.
Kanai课题组一直都关注通过底物与催化剂之间的非共价键作用,完成C-H键的官能团化反应。2015年,他们通过配体与底物之间的氢键作用,完成了Ir催化间位C-H硼化反应;但是因为氢键的相互作用较弱,Ir催化中心和底物之间的位阻过大,无法完成邻位C-H活化。因此,他们设想使用结合方式更强的Lewis酸-碱相互作用,或许可以得到理想的结果。使用苯甲硫醚1a和双片呐醇硼酸酯2为底物,[Ir(OMe)(cod)]2为催化剂,4,4’-二甲基2,2’-联吡啶作为配体,55 ℃反应,可以以70%总收率得到邻、间、对位取代的混合产物,但是其中邻位只有不到10%的产率。当在配体中引入含有Lewis酸性的硼酸酯基团,对邻位的选择性有了很好地提升(Scheme 1)。使用3a作为配体,选择性有了较大的提高,选用位阻较小的3b-3d,反应的选择性并无太大变化;当引入强吸电子基团,改变配体中硼的电性,使其具有更强的Lewis酸性,三氟甲基取代的3f,邻位/(间位+对位)的比例可以达到30以上,但是对于四取代的3g,多引入的三氟甲基使得B与S的配位作用显著增强,反应反而无法很好进行。
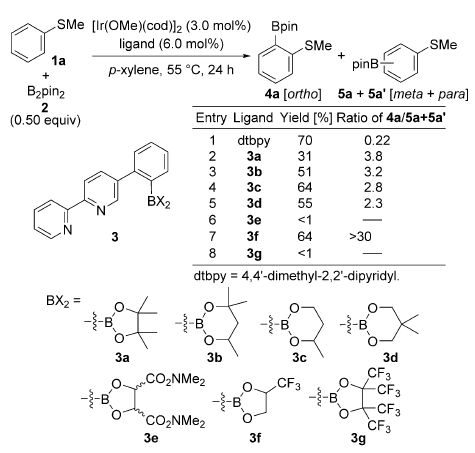
Scheme 1. 反应条件筛选。图片来源:Angew. Chem. Int. Ed.
接下来,作者对底物普适性进行了研究(Scheme 2)。乙硫醚比甲硫醚具有更高的活性。芳环上含有卤素、烷烃、酰胺、酯基、氰基等官能团,都可以得到理想产物,并且间位取代的产物很少,但是使用联吡啶作为配体时,反应邻、间、对位的选择性就差。当芳环上含有醚、胺、硅谜等对Ir有一定配位的杂原子时,反应依然发生在硫醚的邻位。并且一系列的实验结果也证实了Lewis酸-碱相互作用控制了邻位C-H硼化:1)邻位/(间位+对位)的比例在非极性溶剂中比极性溶剂中高;2)邻位/(间位+对位)的比例在低温下比高温中高;3)硫醚含有大位阻的取代基时(如异丙基苯硫醚),邻位/(间位+对位)的比例很显著降低;4)配体上B的Lewis酸性显著影响邻位/(间位+对位)的比例;5)在一些控制实验中无法观测到邻位产物,含硼官能团在联吡啶对位时,邻位/(间位+对位)的比例为0.33。
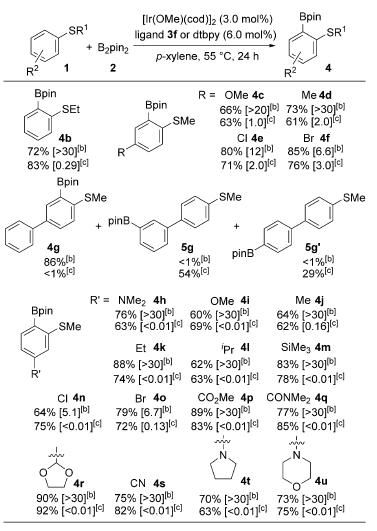
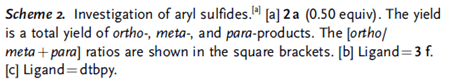
Scheme 2. 底物普适应研究。图片来源:Angew. Chem. Int. Ed.
接下来,作者课题组将该方法拓展到克级别的反应中,能够以72%收率得到产物(Scheme 3a)。该方法也可以应用到Xa因子抑制剂的合成中,在后续的Suzuki-Miyaura偶联中,裸露的NH并不会发生副反应(Scheme 3b)。在杀虫剂8的衍生化中,在标准条件下可以得到邻位硼化产物9;使用联吡啶作配体,可以得到间位硼化产物10;并且该反应中硫代磷酸酯中的S原子对反应的配位性也没有影响(Scheme 3c)。
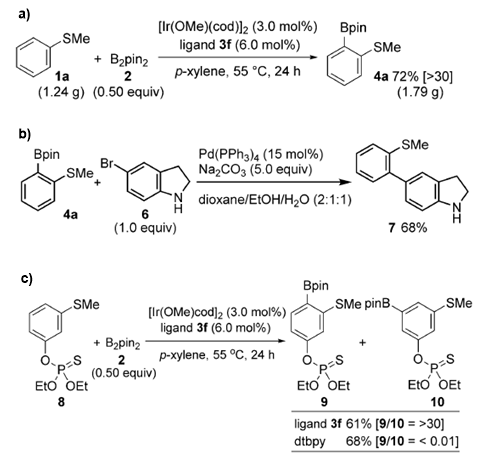
Scheme 3. 反应的进一步拓展。图片来源:Angew. Chem. Int. Ed.
—— 小结 ——
Motomu Kanai课题组成功发展了一种Ir/联吡啶复合物催化芳基硫醚邻位C-H硼化的反应。该反应的选择性主要由配体连吡啶上B原子与芳基硫醚的S原子之间的Lewis酸-碱相互作用决定,这是文献中的首次报道。相较于其他多数C-H直接官能团化反应所需要的苛刻条件,该可逆的Lewis酸-碱相互作用控制的邻位C-H活化反应具有很大的优势,很有希望进一步应用于药物分子和天然产物的末端合成中。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Lewis Acid–Base Interaction-Controlled ortho-Selective C−H Borylation of Aryl Sulfides
Angew. Chem. Int. Ed., 2017, DOI: 10.1002/anie.20161004
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号