氟化试剂:全氟代烷烃叠氮的制备与反应
近年来,含有三氟甲基和全氟代烷烃的有机化合物在医药、农药和功能性材料中得到了极大地应用。比如药物分子中引入三氟甲基,能够在很大程度上增加分子的代谢稳定性和脂溶性,并且也可以改变邻近易电离基团的pKa值。全氟代烷烃(RF)通常都与芳环相连,最近也有文献报道了与杂原子相连的全氟代烷烃(RFS、RFO)的合成。然而,由于产物的稳定性,含有RFN官能团的有机化合物少有文献报道。另一方面,有机叠氮化合物,既可以与亲电/亲核试剂反应,也可以作为偶极子发生环加成反应,并且也是一种广泛使用的氮宾前体,是一类非常重要的有机反应中间体。但是,叠氮化合物也有一大缺点——易爆。在含叠氮的分子中引入强吸电子基团,可以很好地提高其稳定性,Makarov和Christe等人相继报道了全氟烷烃叠氮化合物(Scheme 1)。1a虽然在300 ℃以下都是热稳定的,但是其制备需要剧毒试剂以及气体反应,有很大的局限性。近期,来自捷克科学院的Petr Beier博士等人在Angew. Chem. Int. Ed. 报道了他们所发展的新的全氟烷烃叠氮化合物的合成方法,并将其应用到铜催化的叠氮-炔环加成(CuAAC)反应中。
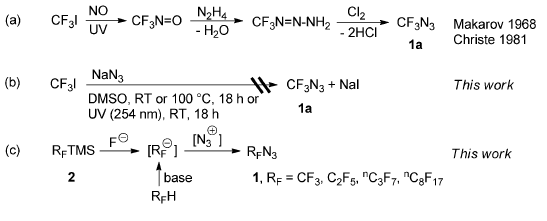
Scheme 1. 全氟烷烃叠氮化合物的合成策略。图片来源:Angew. Chem. Int. Ed.
作者首先设想CF3I与叠氮化钠在光照或者加热条件下,通过SRN1途径得到CF3N3,但是很遗憾该条路径并未实现(Scheme 1b)。接下来,他们设想选择RFTMS或者RFH产生带有负电性的RFˉ,与带有正电性N3+的反应,或许可以得到目标产物(Scheme 1c)。他们选择CF3TMS为底物,TsN3提供叠氮来源,尝试不同引发剂(QA)对反应的影响,该反应的主要副产物为氟仿4、二氟代硅烷5和三氟乙酸盐6。通过尝试不同的碱,最终CsF作为引发剂,在-60 ℃至-30 ℃反应4 h,能够以79%收率得到目标产物(Table 1)。
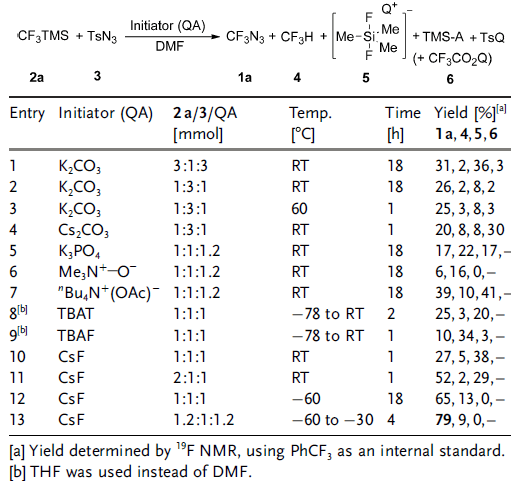
Table 1. CF3N3合成的条件筛选。图片来源:Angew. Chem. Int. Ed.
1a的合成可以放量到10-20 mmol,但是又因其沸点较低(-28.5 ℃),分离纯化存在一定的难度。最终发现,在反应结束后,加入THF或者CDCl3蒸馏,可以得到1a的溶液,并且低于0.3 M浓度的THF溶液可以在室温下储存五周以上。利用类似的方法,也可以得到其他全氟代烷烃叠氮,1c、1d通过NfN3为叠氮来源得到;1b则需要C2F5H与丁基锂反应(Scheme 2)。
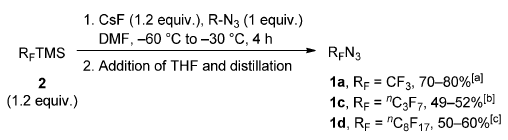
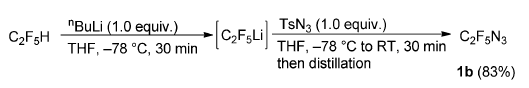
Scheme 2 RFN3的制备。图片来源:Angew. Chem. Int. Ed.
完成RFN3的合成之后,作者又想对其反应活性进行考察。CuAAC反应可以高选择性的得到1,4-二取代三唑,但是全氟代烷烃叠氮的该类反应还没有文献报道,并且RF取代的三唑类化合物也鲜见报道。可喜的是,RFN3可以在室温下以很好地收率与炔发生CuAAC反应,得到新型的N-全氟烷基三唑(Table 2)。芳香、杂环以及脂肪末端炔都有很好的收率,并且卤素、酯基、未保护的羟基和氨基对反应都有很好的容忍性。接下来,作者又尝试两步反应一锅进行,最终发现在DMF溶剂中,对于部分底物可以一锅得到产物N-全氟烷基三唑。
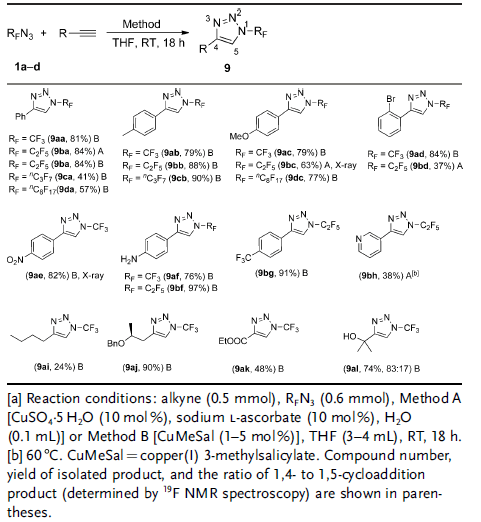
Table 2. RFN3与炔的CuAAC反应。图片来源:Angew. Chem. Int. Ed.
非末端炔烃的反应速率要远低于末端炔烃,即使升高温度,也很难发生反应。使用炔基铜与1b在I2单质参与时,可以以不错的收率得到碘代三唑9bp,之后发生Suzuki–Miyaura反应,可以得到4,5-二取代三唑(Scheme 3)。
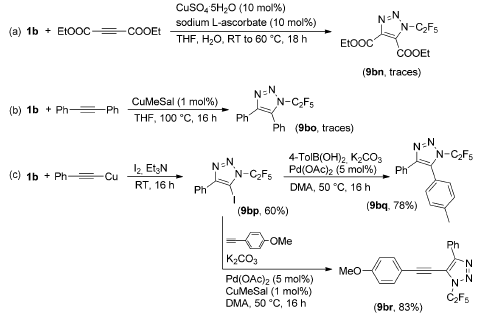
Scheme 3. 4,5-二取代N-全氟烷基三唑的制备。图片来源:Angew. Chem. Int. Ed.
—— 小结 ——
Petr Beier课题组发展了一种通过全氟代烷烃碳负离子与亲电性的叠氮试剂反应,制备RFN3的方法,该方法操作简单、经济,并且可以大量制备。并且全氟代烷烃叠氮可以与末端炔发生CuAAC反应得到新型的N-全氟烷基三唑和4,5-二取代三唑。该方法为全氟代烷烃的合成提供了新的反应模式。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Azidoperfluoroalkanes: Synthesis and Application in Copper(I)-Catalyzed Azide-Alkyne Cycloaddition
Angew. Chem. Int. Ed., 2017, 56, 346-349, DOI: 10.1002/anie.201609715
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号