开发具有质谱标签转移功能的光交联探针用于活细胞研究蛋白-蛋白相互作用
蛋白-蛋白相互作用是支撑生命活动的重要基础,其相互作用网络十分复杂,在活体条件下开展研究极具挑战性。基因编码的光交联探针因具有高反应活性和高时空分辨率的特性,已经成为活细胞內研究蛋白-蛋白相互作用的有力工具。该技术通过基因编码非天然氨基酸将光活性基团定点引入蛋白质相互作用界面,并利用紫外光照射激活并捕捉“诱饵”蛋白。
近年来,北京大学的陈鹏(点击查看介绍)研究组致力于开发基因编码的光交联探针用于活细胞蛋白-蛋白相互作用的研究。该研究组曾于2011年开发了第一代光交联探针DiZPK,并用其鉴定了极酸环境下大肠杆菌抗酸伴侣蛋白HdeA的“客户”蛋白(Nat. Chem. Biol, 2011, 7, 671)。然而,第一代光交联探针DiZPK下游处理步骤采用了传统的“亲和”纯化方法,从而不可避免的引入非特异性吸附蛋白和非直接相互作用的蛋白。另一方面,利用传统的光交联探针获得的交联肽段结构复杂,难以解析,从而丢失了蛋白质相互作用的界面信息。在接下来的研究中,陈鹏研究组于2014年开发了第二代,可切割的光交联探针DiZSeK (J. Am. Chem. Soc., 2014, 136, 11860)。该探针可以在交联后实现底物蛋白与诱饵蛋白的分离,排除了诱饵蛋白的干扰,在一定程度上降低了鉴定背景。但是DiZSeK仍无法解决交联肽段和交联位点的鉴定问题。
近日,陈鹏研究组和北京大学王初(点击查看介绍)研究组合作,开发出了一种具有“质谱标签”转移功能的探针DiZHSeC,解决了交联位点鉴定的问题。该探针不仅可以实现交联后底物蛋白与诱饵蛋白的分离,还能同时在底物蛋白上原位产生一个特异的“质谱标签”。通过该“质谱标签”,研究者们可以很容易地在质谱结果中区分底物与非特异性吸附以及非直接相互作用的多肽片段。此外,通过“质谱标签”,研究者们可以使用常规的质谱分析软件对交联位点进行鉴定,从而获得蛋白质相互作用界面的信息。他们利用基于DiZHSeC设计的IMAPP技术对HdeA的“客户”蛋白进行了进一步鉴定,鉴定的假阳性率从原先的50%降低到了4%。紧接着,他们还利用IMAPP技术对 HdeA二聚化界面,以及HdeA与HdeA“客户”蛋白- DegP的相互作用界面进行了绘制。最后,他们还将该技术拓展至哺乳动物细胞中,研究了小G蛋白RhoA与其支架蛋白RTKN的相互作用,并鉴定了二者的作用界面。通过上述的应用展示,作者期望IMAPP技术可以被广泛应用于捕捉蛋白质相互作用网络以及绘制蛋白质相互作用界面。这一策略尤其适用于那些利用传统结构分析方法难以获得的相互作用界面,如固有或者条件无序蛋白,以及膜蛋白相互作用的界面。
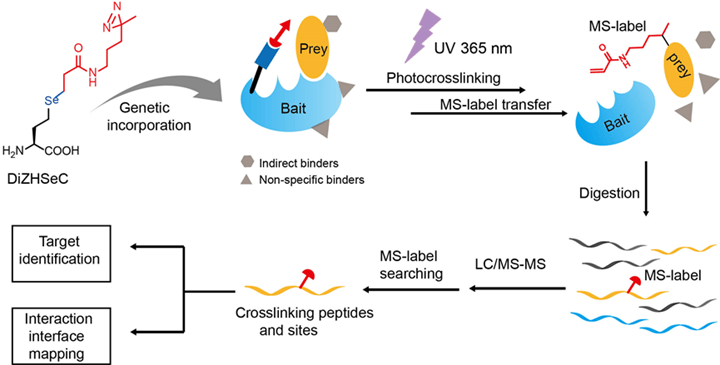
利用IMAPP技术鉴定活细胞内的蛋白-蛋白相互作用
这一成果近期发表在《Nature Communications》上,文章的第一作者是陈鹏研究组的博士研究生杨熠。陈鹏和王初为本文的共同通讯作者。
该论文作者为:Yi Yang, Haiping Song, Dan He, Shuai Zhang, Shizhong Dai, Shixian Lin, Rong Meng, Chu Wang, Peng R. Chen.
原文(扫描或长按二维码,识别后直达原文页面):

http://www.nature.com/articles/ncomms12299
Genetically encoded protein photocrosslinker with a transferable mass spectrometry-identifiable label.
Nat. Commun., 2016, 7, 12299, DOI: 10.1038/ncomms12299.
导师介绍
陈鹏教授
http://www.x-mol.com/university/faculty/8704
http://www.chem.pku.edu.cn/index.php?id=366
王初教授
http://www.x-mol.com/university/faculty/8705
http://www.chem.pku.edu.cn/index.php?id=479
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号