《Science》:憎水基团表面上的离子相互作用
化学分子的极性相互作用,如静电力和氢键,在生物过程比如分子识别和酶的作用中起到了非常重要的作用。而由于非极性氨基酸基团大约覆盖了蛋白质表面的大约75%,因此蛋白质表面的极性相互作用主要发生在疏水环境中。而离子之间相互作用的强度取决于它们的溶剂化环境。

图片来源:zzbbs.com
在20世纪50年代,美国犹他大学的John A. Schellman通过计算推断出,当水性溶剂化的离子接近疏水性表面(例如蛋白质表面的部分),离子之间的相互作用将得到加强。这种分子相互作用的变化无疑对于理解和模拟生物分子的结构和功能至关重要。尽管这非常重要,至今其中的定量关系仍不是很清楚。虽然Schellman的理论方案在解释和模拟的蛋白质结构时经常使用。但它缺乏直接的实验支持。
在最近的《Science》杂志上发表了以日本东京大学的Takuzo Aida教授为首的研究团队的文章,他们通过实验的方法来测试Schellman的这个理论。具体的研究是,该团队观察了通过盐桥接合的有机离子在添加酸后的解离过程,来定量测量离子的相互作用。实验结果证实,在疏水性表面的离子相互作用确实是由其到表面的微小距离差异(小于纳米尺度)来控制。
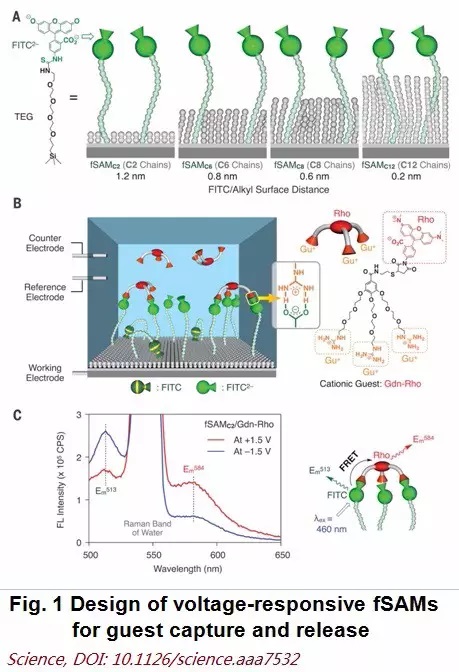
他们设计出了一系列以C2、C6、C8的和C12烷基链作为空间填充的自组装单层结构(SAM),其中带有离子性的末端基团,并通过形成多盐桥捕获具有相反电荷的树枝状游离分子。加酸后这些被捕获的分子被质子替换而释放的程度,反映了其离子相互作用强度。定量实验结果显示,当这种离子对与疏水性的单层结构的距离从1.2(C2)变为0.2(C12)纳米时,增加的盐桥强度约为每摩尔3.9千卡。
在测量离子对的相互作用时,该团队利用了自组装单层结构上带荧光的离子基团与被捕获的相反离子基团之间的荧光共振能量转移(FRET)机理。在这种机理中,当能量转移受体(即被捕获分子上的生色团)因被捕获后与自组装单层结构上的荧光生色团靠近时,后者本来因被光激发而释放出荧光的能量转移到了受体上,再由受体发出波长已经红移的荧光。通过测量两种不同颜色荧光的比例,就可以判断该离子对是否解离。
http://www.sciencemag.org/content/348/6234/555.abstract
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!










































 京公网安备 11010802027423号
京公网安备 11010802027423号