Angew:结合铁催化与生物催化,动态动力学拆分新思路
在过去的几十年中,过渡金属催化在化学和药物工业中有着举足轻重的地位。最近几年,研究的热点逐渐转移之地球上含量丰富的廉价金属,比如铁。手性醇在化学领域是非常重要的有机合成中间体,通过酯化或者水解的动力学拆分是合成它们的重要手段之一。动力学拆分方法的一个主要缺陷是最高产率不会超过50%,然而,动态动力学拆分(dynamic kinetic resolution)方法可以很好的解决这一问题,其理论产率最高可达100%。在早期的研究中,Williams和Bӓckvall等科学家报道了Rh和Ru等贵金属催化的醇的动态动力学拆分1。随后,Berkessel和Akai等人分别报道了AlMe3/binol/lipase和vanadium/lipase催化剂体系催化醇的动态动力学拆分,取得了良好的结果2。尽管醇的动态动力学拆分已经发展了较多的催化体系,但发展更为廉价且可得的催化体系仍然显得至关重要。
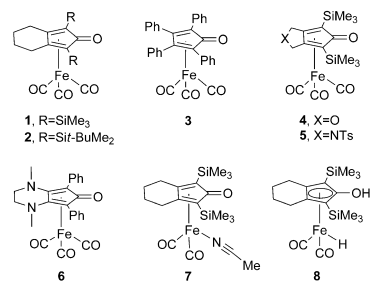
Figure 1. 铁羰基络合物。图片来源:Angew. Chem. Int. Ed.
在Casey、Guan和Beller等人报道的铁催化剂8催化的羰基类化合物和亚胺类化合物的对映选择性氢化还原这样一个背景下(Figure 1),来自德国亚琛工业大学的有机化学家Magnus Rueping教授(点击查看介绍)受到自然界Fe-氢化酶催化氢的可逆异裂反应的启发,把铁催化和酶催化相结合,高效实现了醇的不对称动态动力学拆分(Scheme 1)3。(Merging Iron Catalysis and Biocatalysis—Iron Carbonyl Complexes as Efficient Hydrogen Autotransfer Catalysts in Dynamic Kinetic Resolutions. Angew. Chem. Int. Ed., 2016, 55, 13602-13605, DOI: 10.1002/anie.201606197)
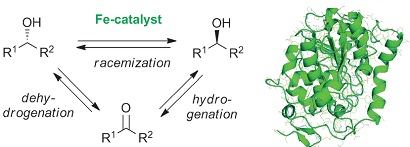
Scheme 1. 铁催化和生物催化的醇的动态动力学拆分。图片来源:Angew. Chem. Int. Ed.
作者首先使用(R)-1-苯基乙醇作为模板底物研究了一系列铁催化剂催化醇的消旋化反应。从结果可以看出,催化剂8呈现出最好的活性和选择性(Table 1)。
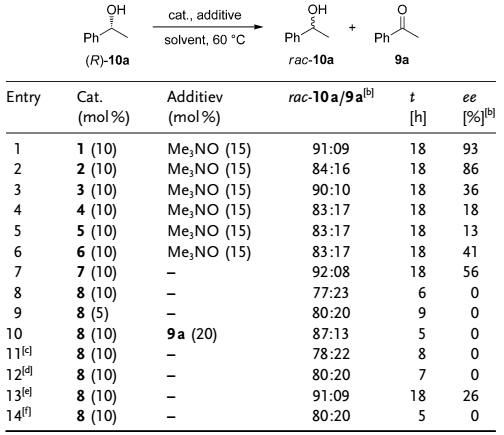
Table 1. 条件筛选。图片来源:Angew. Chem. Int. Ed.
作者发现消旋化反应对温度的依赖性很大,当反应温度为90 ℃时,只需要90分钟就可以实现彻底的消旋化;当温度为60 ℃时,则需要6小时才能实现彻底的消旋化;而当温度为40 ℃时,催化剂呈现出很低的催化活性(Figure 2)。
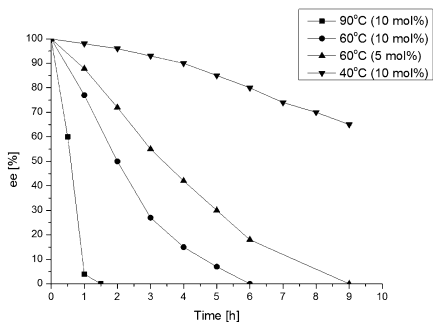
Figure 2. 温度考察。图片来源:Angew. Chem. Int. Ed.
作者随后使用铁催化剂8和热稳定性、活性较高的酯化酶Novozyme-435作为催化剂组合筛选了一系列动态动力学拆分所需要的乙酰基化试剂。最后发现醋酸对氯苯酚酯是最好的乙酰基化试剂。能以100%的化学选择性和99%的对映选择性得到手性产物11a。最佳的反应条件是:使用甲苯作为溶剂,对氯苯酚酯作为乙酰基化试剂,反应温度为60 ℃,铁催化剂8和酶Novozyme-435作为催化剂组合(Table 2)。
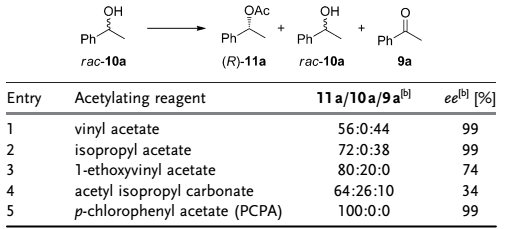
Table 2. 条件筛选。图片来源:Angew. Chem. Int. Ed.
在最佳反应条件下,作者对反应的底物普适性进行了考察。从结果可以看出,该催化体系对不同的1-芳基乙醇的芳基取代基有很好的包容性。不管取代基在芳环的对位还是间位,不管取代基是富电子基团还是贫电子基团,目标产物都能以高收率(81-93%)和高对映选择性(95-99%)得到。五元并环和六元并环的醇也能很好的适应该催化体系,目标产物以非常优秀的结果得到。作者也对长链醇和芳杂环醇进行了考察,都能以优秀的结果得到目标产物(Table 3)。
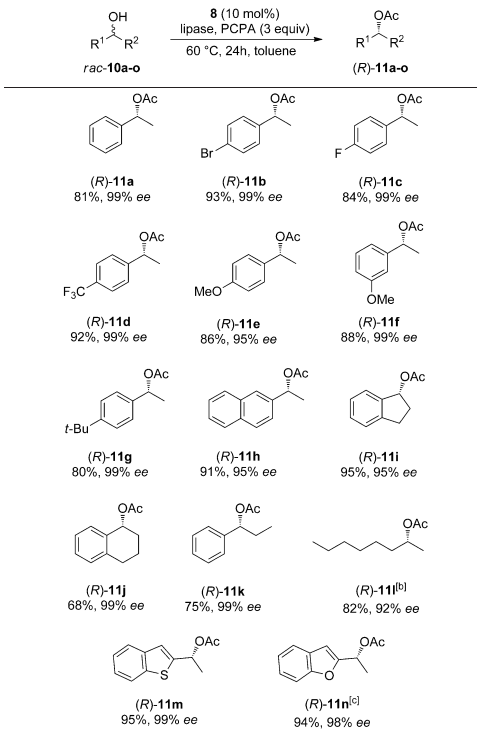
Table 3. 底物拓展。图片来源:Angew. Chem. Int. Ed.
作者随后还研究了构型反转反应,当使用(S)-1-苯基乙醇作为底物时,会以非常优秀的产率和对映选择性得到100%构型反转产物。这在有机合成中可以作为Mitsunobu反应的一个可供选择的方法来合成手性反转的醇(Scheme 2)。

Scheme 2. 构型反转研究。图片来源:Angew. Chem. Int. Ed.
总结:
本文作者发展了第一个非天然的铁和酶协同催化的例子,这个体系的关键是铁催化脱氢—氢化过程和酶催化的兼容性问题。铁催化的脱氢—氢化过程所需反应条件很温和,而这正是酶催化所需要的。这一方法对各种手性醇都有非常好的产率和对映选择性。考虑到铁催化和酶催化的良好兼容性,以及铁催化剂廉价易得,我们相信这样一个催化体系必定会为双重催化体系开启一个新的篇章。
参考文献:
1. (a) P. M. Dinh, J. A. Howarth, A. R. Hudnott, J. M. J. Williams, W. Harris, Tetrahedron Lett., 1996, 37, 7623. (b) A. L. E. Larsson, B. A. Persson, J.-E. Bӓckvall, Angew. Chem. Int. Ed., 1997, 36, 1211.
2. (a) A. Berkessel, M. L. Sebastian-Ibarz, T. N. Müller, Angew. Chem.Int. Ed., 2006, 45, 6567. (b) S. Akai, K. Tanimoto, Y. Kanao, M. Egi, T. Yamamoto, Y. Kita, Angew. Chem. Int. Ed., 2006, 45, 2592.
3. O. El-Sepelgy, N. Alandini, M. Rueping, Angew. Chem. Int. Ed., 2016, 55, 13602.
http://onlinelibrary.wiley.com/doi/10.1002/anie.201606197/full
导师介绍
Magnus Rueping教授:http://www.x-mol.com/university/faculty/3688
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号