JACS:仿生催化对映选择性制备黄酮类化合物
黄酮类化合物一般具有苯并吡喃酮结构,广泛存在于自然界的植物或浆果中,并具有多样的生物活性(Scheme 1A)。目前公认的黄酮类化合物的主要合成途径是通过苯酚与苯并吡喃盐的简单加成反应或者环加反应得到C或D(Scheme 1B),虽然有机化学家们发展了多种合成黄酮类化合物的方法,但大多集中在重新构建吡喃环的策略上,而模拟苯并吡喃盐与苯酚直接加成的仿生化学尚未见报道。最近,加州大学伯克利分校的F. Dean Toste 教授实现了突破,利用仿生催化方法,高对映选择性地制备黄酮类化合物。(Biomimetic Approach to the Catalytic Enantioselective Synthesis of Flavonoids. J. Am. Chem. Soc., 2016, 138, 9775-9778, DOI: 10.1021/jacs.6b05939)
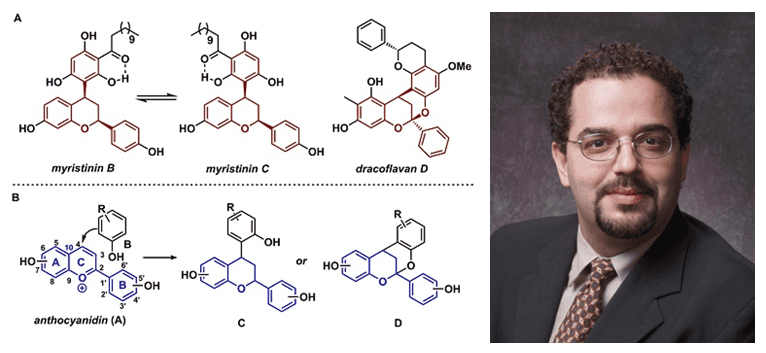
Scheme 1. 图片来源:J. Am. Chem. Soc.和Toste教授网站
仿生合成黄酮类化合物要求催化剂能够促进亲核试剂对苯并吡喃的平面正离子进行立体选择性加成,非常具有挑战性,一般催化剂很难实现该类反应。研究小组将注意力集中在手性阴离子相转移催化剂,该类催化剂已经广泛应用到对映选择性地构建C-F、C-Br、C-I和C-N键中(Scheme 2A)。受这些工作的启发,研究小组认为手性阴离子催化剂与不溶的苯并吡喃盐进行阴离子(PF6-)交换,得到溶解的手性离子对,然后接受苯酚进攻,通过阴离子手性环境诱导作用,高对映选择性地得到目标产物(Scheme 2B)。
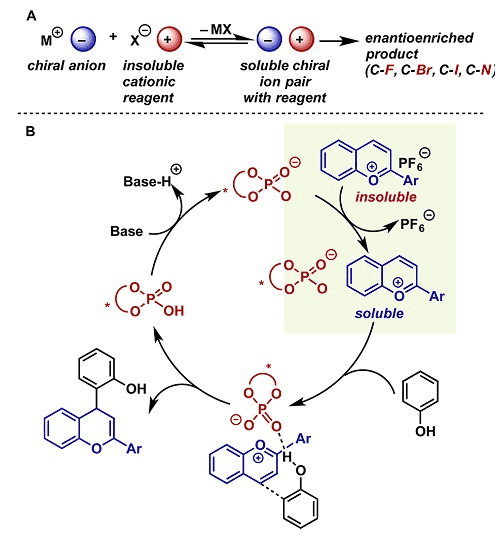
Scheme 2. 图片来源:J. Am. Chem. Soc.
研究小组首先对反应条件进行了优化,以1a为底物,考察了手性磷酸骨架对反应的影响,然后筛选了不同的溶剂和无机碱,当体系中有氧气和水的存在会降低产物的ee值。最终,研究小组使用手性磷酸2b,在氮气保护下,以甲苯为溶剂,Na3PO4为碱,4Å分子筛为添加剂,0 ℃下得到最好结果,以83%的收率和93%的ee值得到目标产物(Scheme 3)。

Scheme 3. 图片来源:J. Am. Chem. Soc.
接下来研究小组对底物进行了拓展,当使用亲核性不如萘酚的苯酚底物时,需要将反应温度升高到室温以提高转化率。反应体系能够适用很多不同底物,一般都能够得到较好的收率和优秀的对映选择性(Scheme 4)。
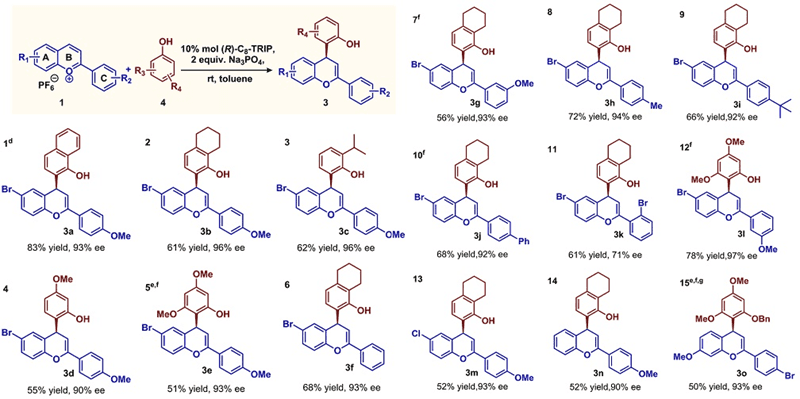
Scheme 4. 图片来源:J. Am. Chem. Soc.
最后,研究小组利用该方法合成了自然界常见的生物活性骨架化合物5和6(Scheme 5)。使用苯并吡喃盐1j与3,5-二甲氧基苯酚反应得到产物后,研究人员设计了两条衍生化途径:(1)在酸作用下发生异构化/亲核加成反应得到桥环缩酮化合物5;(2)苄基保护酚羟基得到3o,再发生钯催化的C-O偶联与氢化还原反应,得到产物6。产物6具有Myristinin B和C的核心骨架(见Scheme 1)。
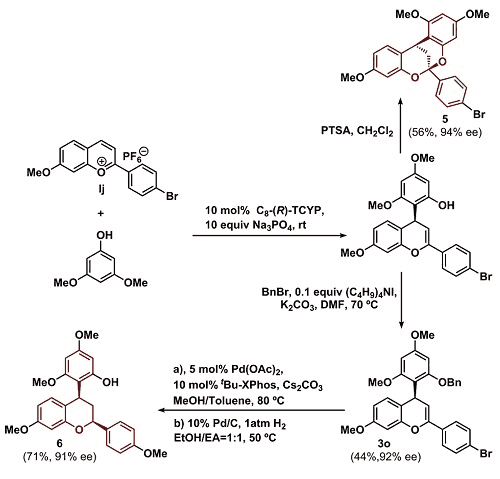
Scheme 5. 图片来源:J. Am. Chem. Soc.
总结:
Toste教授首次报道了使用手性阴离子相转移催化策略,模仿自然界的生物催化路径,诱导苯酚类化合物与苯并吡喃盐进行不对称加成反应,高效高对映选择性地制备黄酮类化合物。该催化体系是否可以应用到苯胺体系,而不仅仅限于苯酚呢?期待中……
Toste小组链接:http://www.cchem.berkeley.edu/toste/toste.html
http://pubs.acs.org/doi/abs/10.1021/jacs.6b05939
(本文由moonlight供稿)
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号