《Nature Chem.》:有机硼试剂与全氟烷基酮的不对称加成反应
含氟有机化合物是现代有机化学的研究热点之一,被广泛地应用到医药、农药和材料中。因此高效高对映选择性地制备含氟有机化合物有着巨大的社会需求。
最近,波士顿学院(Boston College,BC)的Amir H. Hoveyda小组在《Nature Chemistry》报道了有机硼试剂对全氟烷基酮类化合物的不对称加成反应。他们使用廉价易得的催化剂,通过静电相互作用,以优秀的对映选择性得到含全氟烷基的手性叔醇类化合物,该方法还应用到了药物fluralaner的合成中(Scheme 1a)。(Catalytic enantioselective addition of organoboron reagents to fluoroketones controlled by electrostatic interactions. Nature Chem., DOI: 10.1038/nchem.2523)
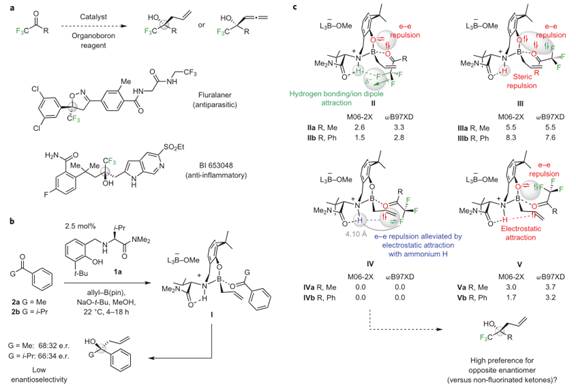
Scheme 1 图片来源:NPG
亲核试剂对一般酮底物不对称加成反应报道比较多,而对全氟烷基酮底物的报道却非常少,主要是因为全氟烷基位阻较大而且背景反应也容易发生。Hoveyda小组使用氨基苯酚类衍生物1a催化烯丙基硼试剂对酮的加成反应,当使用苯乙酮2a和苯基异丙基酮2b时反应的对映选择性很差(Scheme 1b)。而使用苯基三氟甲基酮时能得到优秀的结果(Scheme 2a)。通过DFT计算,作者研究了反应几种可能的过渡态(Scheme 1c)。其中过渡态IV是能量最低的过渡态,过渡态II存在羰基和苯酚氧孤对电子的排斥作用;过渡态III不仅存在氧氧孤对电子排斥也存在与氟孤对电子的排斥作用;过渡态V存在苯酚氧孤对电子和氟原子孤对电子的排斥作用;在过渡态IV中因为氨基与氟原子的距离是4.10 A, 所以不可能存在氢键作用,但两者可能存在静电吸引作用,这也在一定程度上抵消了部分排斥作用,是能量有利的过渡态。
作者以三氟甲基苯基酮为底物,在1a作用下,使用NaOtBu和MeOH时能够以93%的收率,96:4的er值得到产物。提高反应温度时产物er值降低,降低反应温度时收率降低。使用有机碱DBU时也能得到较好结果(88% yield, 90:10 er),这说明金属离子Na+并不参与反应过渡态(Scheme 2a)。随后作者对底物进行了拓展,酮底物上的芳环上可以带有不同取代基、或者是呋喃环或噻吩环,还可以为苄基、环己基;三氟甲基可以为五氟乙基和七氟丙基;烯丙基硼试剂的2位也可以带有不同取代基。但当酮底物上的苯环邻位含有取代基时产物的ee值大幅减低,可能是由于苯环邻位带有取代基后位阻增加,从而增加了与手性胺上苯环的排斥作用(Scheme 2b)。
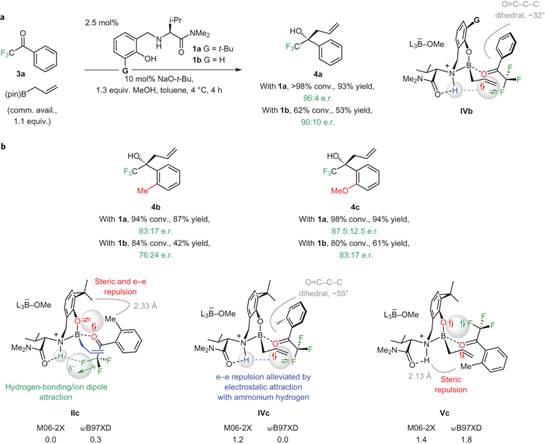
Scheme 2 图片来源:NPG
随后研究小组将烯丙基硼试剂拓展到了联烯硼试剂,反应通过两次重排得到了联烯加成的产物。当使用1a时产物的er值为93:7,当将1a上的叔丁基换为三苯基硅基时er值提高到95:5。通过DFT计算作者发现在过渡态IIe中氨基与F的距离仅2.25 Å,可能存在氢键作用,这可能是使用1b时产物er提高的原因之一(Scheme 3)。作者随后将三氟甲基换为了单氟甲基和二氟甲基时,产物的er值都比较差。而苯环拓展到含氟芳环,能得到较好的结果。
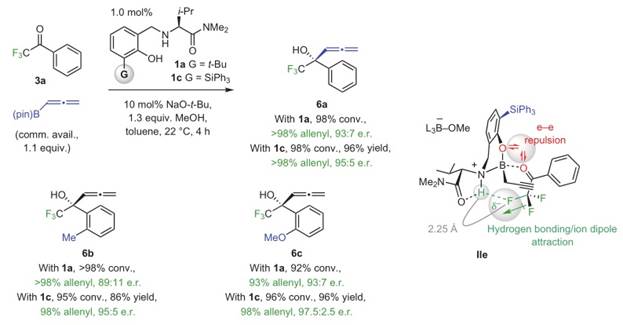
Scheme 3 图片来源:NPG
研究小组最后将该方法应用到了药物fluralaner的全合成中,能够以40%的总收率合成前体化合物 19。首先使用烯丙基硼试剂与三氟甲基酮不对称加成得到手性叔醇4r,然后臭氧化得到醛,再与格氏试剂加成后经Dess-Martin氧化得到化合物18,化合物18在盐酸羟胺作用下和酮羰基缩合并最终成环得到中间体化合物19,再按照之前文献报道的方法就可以高效地完成Fluralaner的形式全合成(Scheme 4)。
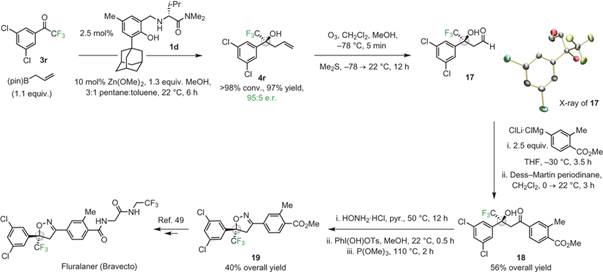
Scheme 4 图片来源:NPG
总结:Hoveyda小组报道了高效高对映选择性地制备含全氟烷基的手性叔醇类化合物的方法,这一方法将在药物研究中有着广阔的应用前景。通过DFT计算化学对该反应中过渡态进行了研究和探讨,特别是氨基与有机氟原子之间的非键相互作用探讨,为人们接下来的研究提供了非常有价值的借鉴。
http://www.nature.com/nchem/journal/vaop/ncurrent/full/nchem.2523.html
(本文由moonlight供稿)
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号