《Science》:新技术精准操控细胞与纳米粒子相互作用
在人类几千年的医药历史上,几乎所有的给药方案都如同从手枪中打出子弹或从炮管中发射炮弹,一旦这些“弹药”进入人体,就不再受到“发射者”的控制。就算是那些具有高度特异性的抗体药物,虽然可以更加精准地找到目标细胞,但是在这些药物进入人体后,人们也一样无法操控它们。
为了更好地进行操控,近年来,科学家们想出了一些办法来改变细胞与材料表面的相互作用。比如,一种已经用于临床的技术可以通过降温使细胞从高分子聚合物的表面上脱离,因为冷却过程可以使这种聚合物膨胀而失去粘性。而在最近的《Science》杂志上,来自加拿大多伦多大学以Warren C. W. Chan为首的一个研究团队,发表了一种新技术,可以更加精准操控细胞与用于诊断和治疗的纳米粒子表面的相互作用。(DNA-controlled dynamic colloidal nanoparticle systems for mediating cellular interaction. Science, DOI: 10.1126/science.aad4925)
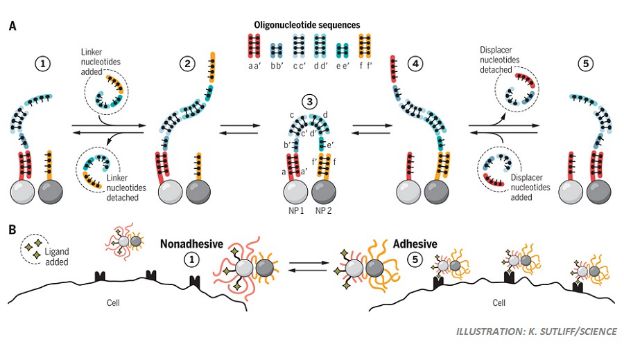
利用这种技术,纳米粒子可以在两种状态中来回切换。在粘性状态时,纳米粒子表面上的配体是开放的,于是纳米粒子可以与细胞上具有特异性的受体结合,从而让细胞“吞”进这种纳米粒子;而在非粘性状态时,这种靶向配体被隐藏起来,则细胞就不会与该纳米粒子作用,其被细胞“吞下”的几率就大大降低。这样一来,就达到了操控这种纳米粒子与细胞作用的目的。这种状态切换由短寡聚核苷酸序列引起,因此在被“遥控”的情况下,该纳米粒子(和其上携带的任何“货物”,如药物)可被投送到在表面上有特异受体过表达的靶细胞上。
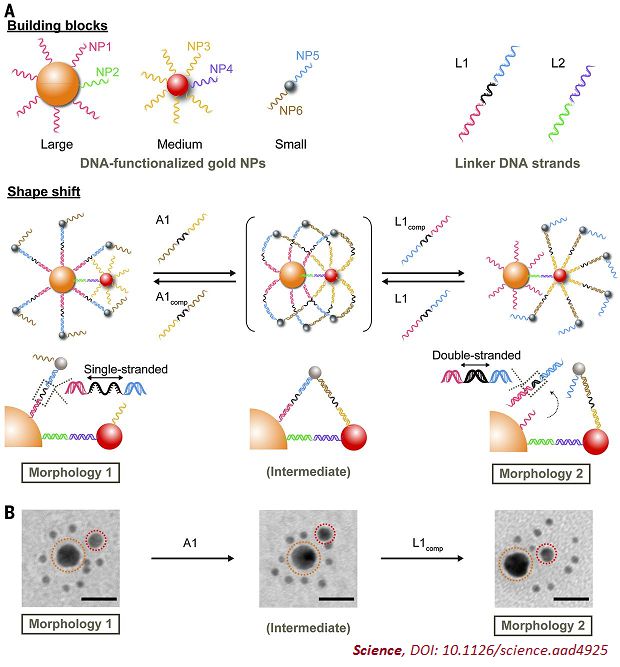
这两种模式之间的切换,来自于一个较长的寡聚核苷酸与两种纳米粒子的杂合过程。这个长DNA分子在其它几种不同的短DNA序列存在的条件下,能够以完全可逆的方式从一种纳米粒子转移到另一种纳米粒子上。这样就可以改变纳米粒子表面的DNA长度。而这两种不同的纳米粒子也通过DNA链互补成对结合在一起。通过透射电子显微镜(TEM),研究人员直接观察到了该纳米粒子系统从非粘性到粘性状态的转变,还观察到了二者之间的中间过渡状态。
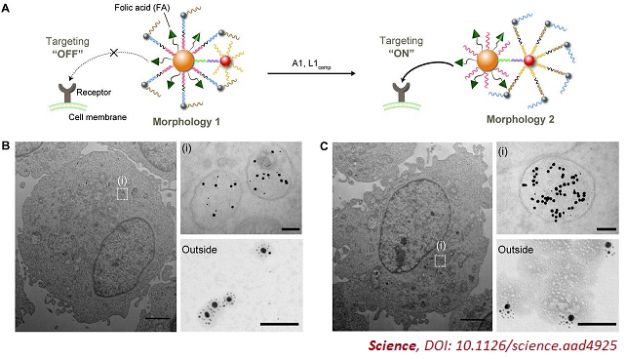
这项技术的另一个要点在于将具有靶向特征的配体(如叶酸)添加到其中一种纳米粒子的表面,如果这种携带配体的纳米粒子现在连接了长的DNA链,那么这些长DNA链会将这些配体掩盖起来,使整个纳米粒子系统成为非粘性状态。而当在另一种寡核苷酸序列存在的条件下,长DNA分子会转移到不携带配体的纳米粒子上,而使配体被从长DNA链的缠绕中解放出来“重见天日”,进而可以将这种处于粘性状态下的纳米粒子结合到靶细胞上,然后通过细胞的内吞作用进入细胞。
虽然这项工作是技术上的重要突破,但是也还有未解决的问题。这些纳米粒子系统含有遗传物质,如果用于药物制剂是否有潜在的长期副作用?在进入人体内后,这些成分是否可能会被降解,从而在到达其目标之前失去功能?
使用纳米粒子作为药物制剂的探索才刚刚开始。
1. http://science.sciencemag.org/content/351/6275/841
2. http://science.sciencemag.org/content/351/6275/814.full
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号