LIGHTSABR——廉价便携的药物发现系统
筛选化合物库,并从中选出具有理想生物活性的化合物是发现新药的有效方法,但这种方法需要庞大、昂贵、复杂的设备。如今,斯克里普斯研究所(The Scripps Research Institute, TSRI)的Brian M. Paegel团队设计了一个筛选系统的核心部分,将筛选设备的体积和成本减少数个数量级。(hνSABR: Photochemical Dose–Response Bead Screening in Droplets. Anal. Chem., DOI: 10.1021/acs.analchem.5b04811)
目前的高通量筛选系统通常占据10,000平方英尺或更大的空间,并需要花费数百万美元。它们在很大程度上依赖于能检索化合物库的机器人装置,将每个化合物放入“微孔板阵列(assay microplate)”的单独小孔中,并测定每种化合物的生物活性。这样的系统筛选效率惊人,但其成本也同样惊人,限制了它们的大规模应用。
Paegel说,“我们开发的这种设备很小,但功能上完全可以媲美高通量化合物筛选。”
他们使用“一珠一化合物(one-bead-one-compound,OBOC)”库,其中每个微珠连接一种化合物。这种库制备快速且价格低廉,基本上可作为实验室的消耗品。“建一个包含数百万化合物的OBOC库很可能仅花费在一周时间和500美元,”Paegel实验室的高级研究员Alexander K. Price说,也是该文的第一作者。
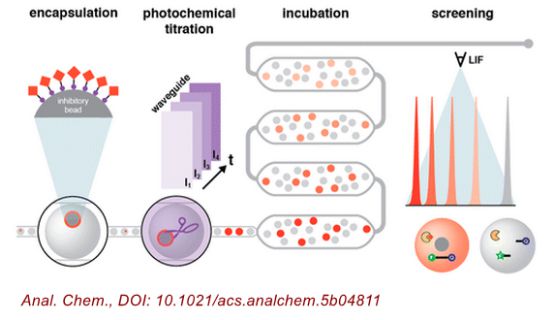
将连在微珠上的化合物投入微型筛选设备中仍是一个技术难题。Paegel和Price等人设计出了一种台式装置,以满足这些挑战,并可以筛选OBOC库。该装置基于微流体原理及喷墨打印技术而制造,使用该团队之前发明的“悬浮液料斗”,OBOC库中的微珠被引入微小液滴中进行特定的测试(如酶活性测定)。这些液滴的体积要比高通量筛选中测试所用的体积少约100,000倍。
然后,该设备用UV诱导光化学反应,将每个化合物从微珠中释放出来,经过一段时间的反应,记录每个液滴的结果。
他们的这个设备被命名为LIGHTSABR(Light-Induced and Graduated High-Throughput Screening After Bead Release)。关键创新在于,它允许用户通过改变紫外线照射从而调整微珠中被释放的化合物的量,从而调整被测化合物的剂量。该团队通过筛选HIV-1蛋白酶(这是引起艾滋病病毒复制的关键酶)的抑制剂,成功证明了这一剂量调整的功能。
Paegel和Price下一步将致力于LIGHTSABR系统的推广。“在世界各地,数以百计的实验室可以运行自己的小型化筛选设备,利用他们自己的测试方法针对最感兴趣的靶标进行药物筛选,”Price说。
1. http://pubs.acs.org/doi/abs/10.1021/acs.analchem.5b04811
2. http://phys.org/news/2016-02-lightsabra-cheap-portable-drug-discovery.html
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号