贵金属纳米材料“类氧化酶”的分子机制:分子氧的低温活化
空气中氧气(O2)的体积含量约为21%,氧元素约占整个地壳质量的49%,氧在整个生态系统的物质循环和能量利用过程中发挥着关键作用。在高温条件下,O2能和大多数物质发生剧烈化学反应;在较低温度条件下,O2具有很强稳定性。这一特性源自于O2分子具有特殊的顺磁电子结构:每个O2拥有一对自旋向上的未成对电子,填充在一对简并的π*反键轨道上,总自旋S = 1。因此,O2在和大多数物质发生化学反应时需经历高自旋过渡态,这些高自旋态能量很高,阻止了O2在低温下发生反应。在生物体系中,O2却能在温和条件下发生反应,这是由于生物体中存在氧化酶,可有效降低反应能垒,将O2活化。正是氧化酶催化的O2反应,驱动着包括人类在内所有需氧生物的物质和能量代谢。
已有研究表明,除天然氧化酶外,当一些金属尺寸减小至纳米尺度时,也可表现出类似的氧化酶活性。例如,O2在钯和铂纳米棒存在条件下,可在室温条件下氧化常见的氧化酶底物,如3,3',5,5'-四甲基联苯二胺。贵金属纳米材料和天然氧化酶具有迥异的结构却具有相似的氧化酶活性,这一现象自身值得关注,然而贵金属纳米材料氧化酶活性机理一直是个谜。
最近,江西师范大学、中科院高能物理研究所的高兴发课题组和国家纳米科学中心的吴晓春课题组合作,对贵金属及其合金纳米材料的氧化酶活性机理开展了深入研究。他们提出,贵金属纳米材料的氧化酶活性可用O2在金属表面的分解反应加以解释:当O2吸附到金属表面后,金属中自旋向下电子转移到O2的π*反键轨道上,降低O2键级?致其分解;在此过程中,净电子自旋从O2转移到金属,O2被分解成单原子O而被活化。因此,O2在金属表面发生分解反应的难易程度可作为预测此种金属氧化酶活性大小的依据,即O2分解反应能垒(Eact)和反应能(Er)可用来预测金属材料的氧化酶活性大小。他们用第一性原理方法计算了O2在不同金属材料表面的Eact和Er值,并实验测定了贵金属纳米材料的氧化酶活性,理论预测的氧化酶活性顺序和实验测定顺序一致,有力验证了他们提出的机理。他们的研究结果为O2活化指出了一条通用路径,为今后基于金属纳米材料设计氧化酶提供了依据。
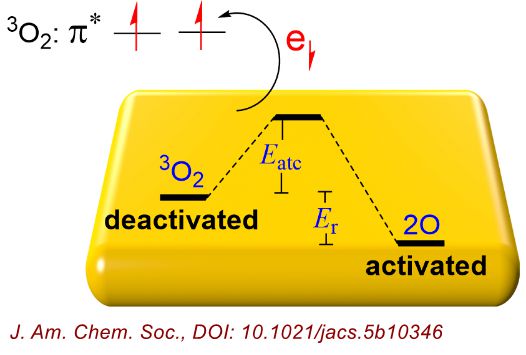
氧气在纳米金属表面分解活化示意图
研究结果发表在国际知名化学期刊《美国化学会志》(DOI: 10.1021/jacs.5b10346)。
http://dx.doi.org/10.1021/jacs.5b10346
原文标题:Mechanisms of Oxidase and Superoxide Dismutation-like Activities of Gold, Silver, Platinum, and Palladium, and Their Alloys: A General Way to the Activation of Molecular Oxygen
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号