钛催化自由基氧化还原中转实现环丙烷酮与烯烃的不对称[3+2]形式环加成
钛配合物具有多个连续的氧化态,故常用于催化各种氧化还原自由基的转化反应。尽管手性钛配合物能够参与各种自由基反应,进而对映选择性地构建碳-碳键,这些反应主要局限于类频哪醇偶联反应、Barbier反应和氧杂环丙烷的开环官能化反应。林松(点击查看介绍)课题组近期报道了利用三价钛引发烯烃和氮杂环丙烷氧化还原串联环加成反应合成吡咯烷的新策略。该策略展现出钛催化剂的几种独特的性质,包括四价钛的亲氧性、三价钛可用于削弱强化学键以及四价钛-氮杂烯醇的双自由基性质。与之前报道的双金属催化光氧化还原策略相比,该工作仅需通过调控钛配合物的配位环境就实现了对立体化学的高效控制。
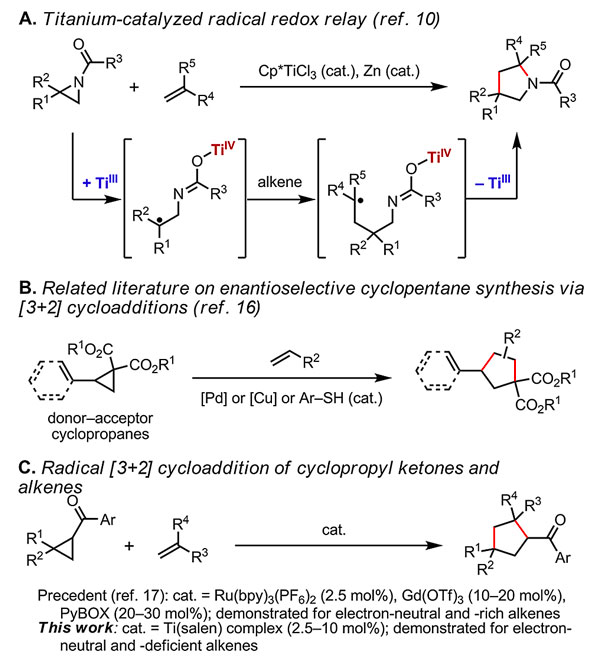
多取代环戊烷酮结构在生物活性分子中十分普遍,并经常作为吡咯烷的类似物用于生物医学研究。基于之前的工作(图1A),林松课题组认为自由基氧化还原串联策略可以同样用于实现环丙烷酮的[3+2]反应。通过对反应条件的筛选,他们以手性二苯基乙二胺和3-金刚烷基-5-甲基水杨醛缩合而成的Ti-salen配合物作为催化剂,锰和三乙胺盐酸盐作为添加剂,乙酸乙酯作为溶剂,室温条件下就能够几乎定量地将环丙烷酮和苯乙烯转化为环加成产物,并实现高效的立体选择性控制(trans d.r.>19:1, 97% ee)。进一步的研究发现,改变手性胺骨架或者水杨醛的取代基都会降低反应活性和立体选择性。值得注意的是,在之前的[3+2]环加成合成吡咯烷的工作中,使用的最佳催化剂Cp*TiCl3 对该反应也具有催化活性,同时选择性地生成顺式产物,由此改变催化剂的结构就能够选择性地得到两种非对映异构体。
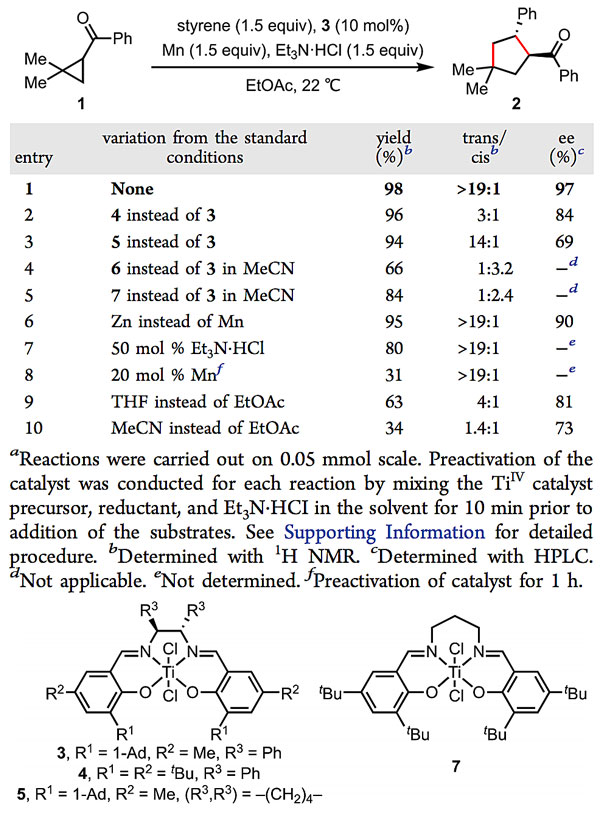
表1. 反应条件的优化
随后,作者对底物的适用范围进行了考察(图2)。反应对苯乙烯及其衍生物具有良好的适用性,并实现了高效的立体选择性控制。频哪醇硼酸酯、含氮杂环等一系列官能团都能够与反应体系兼容。但作者也注意到,对于具有吸电子基团的苯乙烯类底物,反应的立体控制效果较差,常需要更低的温度和更长的反应时间。缺电子烯烃也能够高效地用于合成多取代环戊烷酮。值得注意的是,以二取代烯烃为底物,该反应能够实现四级碳手性中心的高效构建。克量级规模反应证明该反应依然具有不错的选择性和产率。进一步的机理研究表明,该反应经过以自由基为中间体的反应路径(图3)。
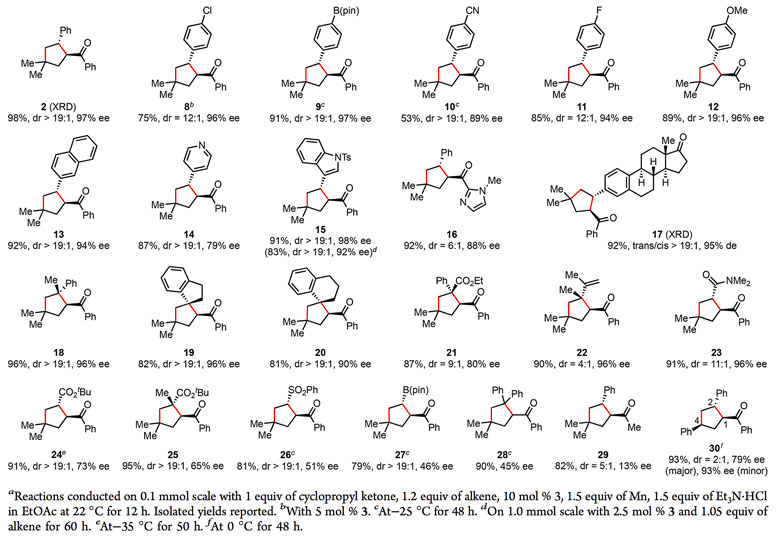
图2. 底物适用范围的考察
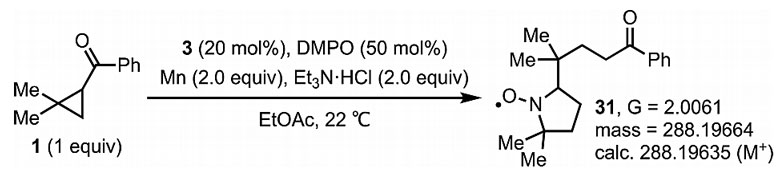
图3. 机理的研究
总结
林松教授及其团队利用先前开发的过渡金属催化[3+2]环加成反应,结合钛催化的氧化还原串联策略,发展了一种新颖的立体选择性合成多取代环戊烷酮的方法。该反应以易于制备的原料出发,基于单一手性催化剂的调控,实现了温和高效的反应性和控制性。该研究中所利用的自由基氧化还原催化策略可作为其他有机合成中难题的潜在解决方案,因而具有广阔的应用前景。
该论文作者为:Wei Hao, Johannes H. Harenberg, Xiangyu Wu, Samantha N. MacMillan and Song Lin
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Diastereo- and Enantioselective Formal [3 + 2] Cycloaddition of Cyclopropyl Ketones and Alkenes via Ti-Catalyzed Radical Redox Relay
J. Am. Chem. Soc., 2018, 140, 3514, DOI: 10.1021/jacs.7b13710
导师介绍
林松
http://www.x-mol.com/university/faculty/48471
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号