癌症组织“低”pH响应的siRNA载体胶束
随着对癌症研究的深入,其治疗手段越发丰富,生物大分子(特异性蛋白、核酸)的使用便是近年来表现突出的一种方法。但是这些分子用于临床试验的最大困难在于,怎样让“药物”到达癌细胞内。
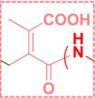
一方面是选择性问题。对癌细胞的选择性,可以依靠酶响应的胶束运载,因为癌细胞会过量表达一些蛋白酶,它们可以水解载药分子中的化学键,产生选择性释药。但是癌组织有一个更为突出的特点——pH(6.2-6.9)偏低呈酸性,相比之下正常组织pH为7.2-7.4。虽然这样的差别很小,但是借助于特异的化学键仍能做到区分,比如烷基取代的单酰胺马来酸,它的酰胺键可以在pH稍低时断裂,并且可通过调节取代烷基改变pH敏感程度,进而设计pH响应的分子。
另一方面,大分子在体内易受到免疫系统的清除,并且癌细胞对大分子的吸收也难度更高。借助于PEG等惰性组分的保护,可以让胶束稳定化,进而延长药物的体内循环时间。同时,正电性胶束可以促进核酸的跨膜运输,这也是得到深入研究的方法。
于是,综合以上提到的三个组分,来自中科大的王军课题组设计了如下的三嵌段高分子,它可以形成载药胶束。
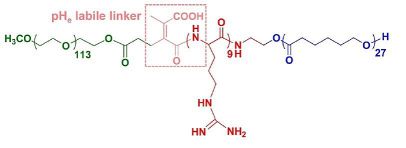
分子中的PEG链段作为生物稳定的亲水端,保证胶束在体内被缓慢降解。而酸敏感的linker,pH 7.4时半衰期在24 h以上,pH 6.5时,则在6 h内降解超过60%。当酰胺键断裂,胶束转化为精氨酸链段暴露在外的正电胶束,可以促进siRNA的胞吞过程。
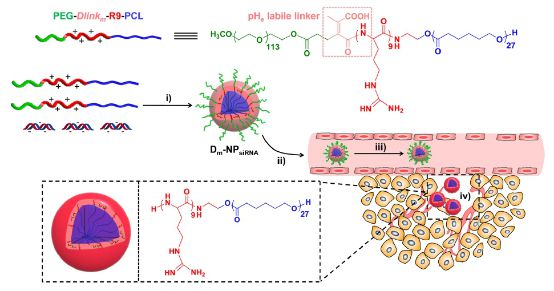
保护及释放效果图
而这一载体的体内实验也表现良好。由于该胶束在低pH发生较快的水解,因此在内循环中逐渐于癌组织附近富集,产生脱PEG链段的正电胶束,在携带了siRNA后,可以表现出显著的基因沉默效果,并且可以在小鼠中抑制肺癌细胞生长。
作为一篇ASAP,全文的实验十分详细,对照组的设计也较为周全。本文的最大突破在于设计并证明了,癌组织的低pH可以作为特异性刺激,来进行癌症的针对治疗;并且其巧妙的分子设计也使得siRNA的运载得以实现,这一平台具有很好的应用前景。
相关工作发表在《J. Am. Chem. Soc.》上。
http://pubs.acs.org/doi/10.1021/jacs.5b09602
(本文由 小朱 供稿)
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号