ABNO介导哌啶类化合物的电化学氧化α-氰基化反应
哌啶是FDA批准的药物中常见的杂环结构,具有良好的药物动力学性质(图1A)。环胺中N邻位C-H键的官能化一直是人们关注的焦点,以往设计该类反应多是利用N保护(即N-酰基或N-芳基/烷基)的三级胺衍生物作为底物进行,这些化合物在药物合成中可利用价值小,氨基保护/脱保护繁琐的操作过程也限制了人们对二级哌啶类化合物的有效利用。因此,开发二级哌啶类化合物C-H键直接官能化的方法非常必要。
近日,美国威斯康星大学麦迪逊分校化学系的Shannon S. Stahl教授(点击查看介绍)课题组在J. Am. Chem. Soc. 上发表文章,报道了电化学方法实现二级哌啶类化合物N邻位C-H键的氧化氰基化,反应无需对哌啶的N-H键进行保护基修饰,利用9-氮杂双环壬烷-N-氧化物(ABNO)作为预催化剂,促进二级哌啶脱氢氧化形成相应的环亚胺,进而发生氰根负离子的加成得到最终产物。该方法需要的电极电势较低,一系列杂环结构以及氧化敏感的基团都可以很好地兼容。
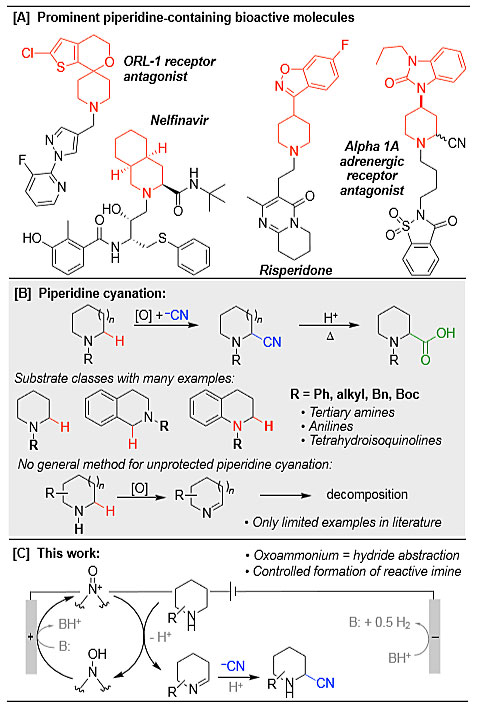
图1. 二级哌啶类化合物的α-氰基化。图片来源:J. Am. Chem. Soc.
氰基可以转化为其它多种取代基,包括羧酸、酰胺、酮和胺等(图1B)。目前报道的工作仅限于活化底物如四氢异喹啉和三级胺/酰胺衍生物的氰基化,尚无普适的方法用于二级哌啶的氰基化,反应过程中环亚胺很容易发生分解。
以往报道胺的电化学氧化反应通常是以三级胺衍生物发生单电子转移(ET)引发的,随后发生快速的质子和电子转移(PT-ET)形成相应的亚铵离子。作者在近期的研究中发现,氮氧化物参与的电化学氧化反应可以规避常规的ET-PT-ET过程,通过电化学氧化促进底物的直接氢转移。氮氧化物参与的反应能在较低的电极电势(> 1 V)下进行,从而大大扩展了官能团的兼容性和底物适用范围(图1C)。
作者首先通过循环伏安法(CV)研究有无ABNO参与的情况下4-苯基哌啶1a的氧化还原情况。底物1a在739 mV处呈现出不可逆的阳极CV曲线(图2,绿色线),而低电势小位阻的氮氧化物ABNO表现出E1/2= 195 mV的可逆CV(图2,灰色线)。含有1a和ABNO溶液的CV分析表明,ABNO氧化还原电势的阳极特性显著增加,阴极特性相应减少(图2,红色线)。ABNO和1a的阳极峰值电势(ΔEp > 500 mV, 绿色与红色线)之间的巨大差异表明,底物氧化时产生的电极电势较低是由ABNO介导的氢转移引发,而不是电极引发的电子转移导致的。
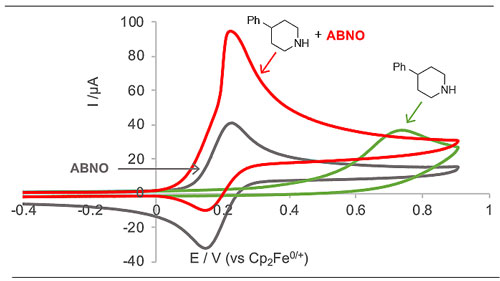
图2. 循环伏安法研究1a的氧化还原情况。图片来源:J. Am. Chem. Soc.
随后作者转而探索底物氰基化的最佳条件,以石墨电极和Pt电极构成电解池,在恒定电流(1-3 mA)下反应,TMSCN作为氰基来源。他们最初尝试在电极上进行底物的直接氧化,产物2a产率较低(19%,entry 1)。反应中加入10 mol%的ABNO,2a的产率翻倍(37%,entry 2)。反应中加入1化学计量的六氟异丙醇(HFIP)可作为质子源促进阴极H2的产生。
他们还对其它氮氧化物进行考察,TEMPO和4-乙酰氨基TEMPO(ACT)具有比ABNO更高的氧化还原电势,但产率较低(entry 4和5)。KetoABNO参与反应具有最高的产率,但由于其氧化还原电势较高,可能会影响官能团的兼容性。反应将电解电流从1 mA增加到3 mA,产率从54%增加到66%(entry 3和7)。他们还使用MeOH替代HFIP作为质子添加剂,并将其化学计量降低至0.5当量,最终以84%的产率得到目标产物(entry 7-10)。反应以1 g量级规模进行(entry 11和12)也能以良好的收率得到2a。

图3. 电解条件的优化。图片来源:J. Am. Chem. Soc.
在优化的反应条件(红色线)下,维持3 mA电流所需的电极电势较低(约为3 mA)。在不存在MeOH(蓝色线)的情况下,只有当通过的电荷小于ABNO电化学氧化至ABNO+所需的电荷时,才能观察到较低的电势。在不存在MeOH和ABNO(绿色线)的情况下,反应则需要更高的电极电势来维持3 mA电流,初始观测到的电势与CV研究中的期望值接近。然而,在实际反应过程中,该电势显著上升,可能是直接电解过程中产生的反应中间体对电极污染造成的。反应的产率与维持该反应所需的电势成反比,表明在非隔离电池中,氮氧化物与质子穿梭过程需要很好地匹配才能提高产率。
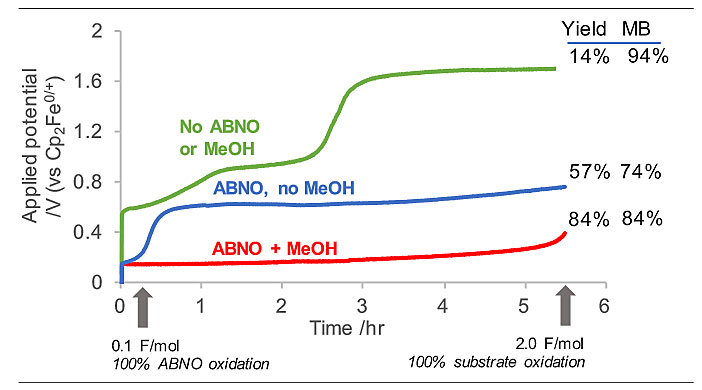
图4. 恒流电解过程的分析。图片来源:J. Am. Chem. Soc.
有了最佳的反应条件,作者对底物的适用范围进行了考察(图5A)。对于4-取代的哌啶类化合物,不同官能团修饰的底物,包括芳基、芳基卤化物、芳基醚、酰胺、酯、吡啶和相关的杂芳基衍生物以及偶氮类化合物(3a-3r),参与反应都能获得良好的产率。该方法甚至能够兼容游离的二级羟基(3x),表明胺氧化的过程优先于氮氧化物介导的醇氧化。反应混合物中回收的电解质盐(TBAPF6)还可以重复使用。底物中存在大位阻取代基(3a-3p,3s)时,反应可以得到较高的非对映选择性,通常只得到单个对映体。作者通过NOE和单晶衍射结构分析,证实了氰基与不同取代基之间存在良好的反位关系。立体化学分析表明,氰化物对亚胺中间体进行轴向进攻,该反应模型与Houk和Cieplak曾报道的立体化学模型一致。该方法还适用于哌啶类化合物以外的杂环化合物,如吡咯烷(3ac)、吗啉(3u)。
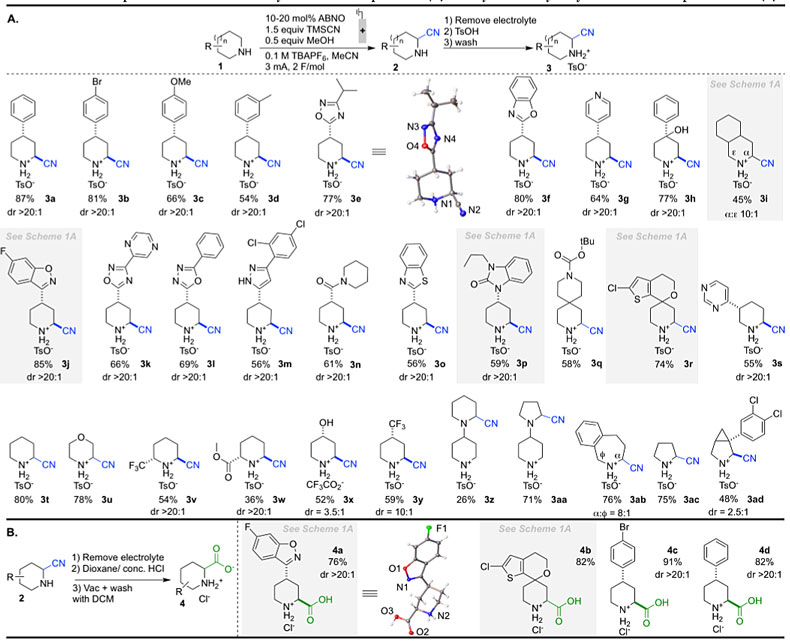
图5. 底物适用范围的考察。图片来源:J. Am. Chem. Soc.
对于同时含有保护基修饰和游离氮的二级哌啶类底物,氰基化只发生在未保护的哌啶环(3q)上。另一方面,含有五、六元环三级烷氨基取代的二级哌啶底物(3z,3aa)在烷氨基环上优先发生氰基化反应。这种方法在药物化学中也可以得到充分的利用,反应能直接对活性药物和候选药物分子如利培酮(3j)、2种受体拮抗剂(3p和3r)和抗HIV药物Nelfinavir(3i)等进行衍生化。抗抑郁药物分子阿米拉法丁(3ad)发生氰基化也能取得48%的收率。氰基水解为羧酸还可以用于合成相应的非天然氨基酸,几种氰化产物能直接在不分离的条件下水解生成相应的羧酸衍生物(4a-d,图5B)。
总结
Shannon S. Stahl教授课题组发展了一种高效、环境友好的方法用于二级哌啶类化合物的电化学α-氰基化,可用于合成一系列重要的药物砌块。ABNO参与氢转移过程可使反应在低电极电势下进行,具有良好的官能团兼容性。该方法在药物研发中具有十分重要的应用价值。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Electrochemical Aminoxyl-Mediated α-Cyanation of Secondary Piperidines for Pharmaceutical Building Block Diversification
J. Am. Chem. Soc., 2018, 140, 11227, DOI: 10.1021/jacs.8b08145
导师介绍
Shannon S. Stahl
http://www.x-mol.com/university/faculty/98
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号