国家纳米科学中心研究团队多肽与DNA/辅基共组装构建类酶催化中心
酶是生物体细胞内具有催化功能的特殊蛋白质,能在常温常压下高效而专一地催化生物化学反应,促进生物体新陈代谢。基于酶催化原理发展的超分子模拟酶近些年来引起广泛的关注。如何人工模拟天然酶活性中心的几何结构和化学环境,使其催化效率接近甚至超过天然酶是一项具有挑战性的研究课题。国家纳米科学中心研究团队通过生物分子模块化自组装的方法实现了对辣根过氧化物酶(Horseradish peroxidase,HRP)活性中心的重构。
酶的活性中心是利用诸如氢键、范德华力或疏水相互作用与底物直接结合或者促进底物与辅基结合。形成酶活性中心的必要氨基酸残基并非来自一级结构上的相邻位置,它们通过肽链的盘绕和折叠在空间构象上彼此靠近,组成具有特定空间结构的区域。HRP活性部位中具有典型的氨基酸残基三维排列,如邻位组氨酸配体(His170)、远端组氨酸残基(His42)和精氨酸残基(Arg38)分别处于血红素两侧,协同性地降低血红素到反应中间体(化合物I)的活化能垒。显然,设计和构建适当的超分子自组装体系,在稳定血红素辅基的同时,为其提供三维排布的轴向配体和远端的催化功能官能团,是提高催化反应效率甚至接近天然酶的关键。
自然界中广泛存在着蛋白质和DNA(或RNA)协作发挥生物活性的复合物体系,如聚合酶、端粒酶、核小体或Crisper-Cas9系统,表明折叠的多肽与核酸具有结构和序列上的互补性,二者的自组装可能会形成独特的异相催化界面。受此启发,在前期的研究中(ACS Nano, 2017, 11, 7251),国家纳米科学中心的研究团队以DNA G-四链体作为支撑模块,稳定氯化血红素并提供轴向配体基团;以聚组氨酸作为活化模块,为血红素提供可作为远端酸碱催化剂的组氨酸残基(Histidine, His),G-四链体DNA和聚组氨酸多肽能够对血红素协同活化。在前期研究的基础上,研究团队通过设计含有谷丙酰胺残基(Glutamine, Gln)的多肽,使其通过分子间作用力形成β-sheet二级结构和自组装,聚集羧酰胺官能团(carboxamide)并使其空间取向,模拟天然HRP活性中心精氨酸残基的氢键给体功能,提高催化中心血红素对H2O2的亲和性;随后与富含组氨酸的β-sheet短肽共组装,模拟HRP活性中心的催化三联体(His42-Arg38-His170)功能,实现氢键网络与组氨酸功能的协同,进一步提高催化效率。
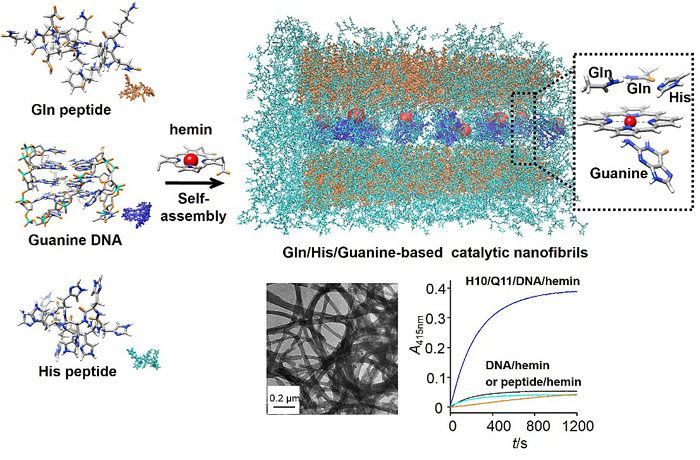
研究结果表明,谷丙酰胺的多肽与DNA及血红素共组装形成纳米级纤维,多肽和DNA G-四链体各自维持二级结构。含有谷丙酰胺的多肽与G-四链体对于血红素催化具有显著的协同作用;多肽二级结构的形成能力能够影响血红素络合物体系的催化活性,证实了多肽的自组装以及催化基团空间排布和取向的重要性。结合动力学同位素效应和血红素活化的时间分辨吸收光谱,他们证实Gln残基对于催化过程中的氢键网络功能。与聚组氨酸多肽的共组装能够进一步提高体系的底物转换数(kcat)和催化效率(kcat /Km):相对于G-四链体/血红素催化剂,催化效率提高了一个数量级。结合分子动力学模拟的分析表明在血红素附近可能形成三维分布的Guanine(碱基)-His(氨基酸残基)-Gln(氨基酸残基)三联体,与HRP活性中心的催化三联体功能相似。密度泛函理论模拟表明,催化三联体的形成促进了H2O2在血红素表面的吸附、O-O键的断裂和反应中间体化合物I(Cpd I)的形成。Gln多肽与G-四链体共组装,也为还原性手性底物(如L-或D-DOPA)接近催化中心提供了手性的化学环境,使复合体系具备手性选择性催化能力。
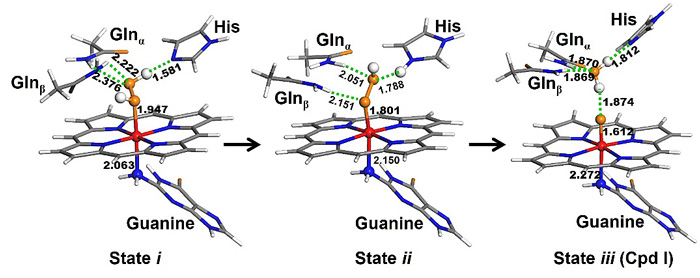
这一成果为构建具有三维活性部位的超分子模拟酶的设计与构建提供了研究思路。需要指出的是,复合自组装体系的催化活性依赖于活性中心关键反应性基团的类型与分布方式,取决于组装模块(多肽和DNA)的二级结构和相互作用,借助血红素氧化催化反应产生可视化产物,为DNA或多肽分子可感应的生命信号分子提供检测平台。
这一成果近期发表在ACS Catalysis 上,文章的通讯作者是国家纳米科学中心的王振刚研究员、施兴华研究员和丁宝全研究员,第一作者为王振刚研究员、王会博士、刘清博士。
该论文作者为:Zhen-Gang Wang, Hui Wang, Qing Liu, Fangyuan Duan, Xinghua Shi, Baoquan Ding
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Designed Self-Assembly of Peptides with G-Quadruplex/Hemin DNAzyme into Nanofibrils Possessing Enzyme-Mimicking Active Sites and Catalytic Functions
ACS Catal., 2018, 8, 7016, DOI: 10.1021/acscatal.8b00896
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号