锌催化杂双芳基酮的动态动力学拆分
轴手性双芳基化合物是一类常见的分子骨架,广泛存在于天然产物和生物活性分子中。此外,该类结构在不对称催化领域也发挥着重要的作用,可用作过渡金属催化剂的配体或直接用作有机分子催化剂。芳香族化合物的不对称交叉偶联反应或氧化二聚反应是合成该类化合物最直接的方法,但此类反应的底物适用性有限,用于构建杂双芳香烃分子时并不理想。除此之外,过渡金属催化的动态动力学拆分(DKR)反应、有机分子催化的方法等也陆续报道用来构建该类结构。例如,Gerhard Bringmann课题组利用DKR过程发展了双芳基内酯的不对称开环反应,随后Tohru Yamada及王伟团队分别利用过渡金属催化剂及有机分子催化剂发展了相应的不对称催化过程。Takahiko Akiyama课题组基于双芳基半缩醛胺可轻松发生开环、再环化,设计了苯基亚氨基苯酚的不对称氢化还原得到高对映选择性的手性双芳基化合物。Nicholas Turner与Jonathan Clayden等人又报道了酮还原酶参与的双芳基氮氧化物醛的生物催化DKR过程,由此发展了构建包含杂芳香基的手性双芳基化合物的方法,但该反应仅适用于形成六元环过渡态时位阻较小的底物。
西班牙CSIC-US化学研究所(IIQ)的José M. Lassaletta、Valentín Hornillos及塞维利亚大学的Rosario Fernández等人致力于发展Pd催化C-C键、C-P键和C-N键形成的动态动力学不对称转化反应(DYKAT)。最近,他们报道了锌催化杂双芳基酮的羰基硅氢化还原反应,基于杂芳香烃中氮原子与酮羰基之间的Lewis酸-碱相互作用,实现了构型不稳定的杂双芳基酮高对映选择性的动态动力学拆分(DKR)过程,由此构建了包含轴手性及手性中心的二级醇产物。相关工作发表在Angew. Chem. Int. Ed. 上。
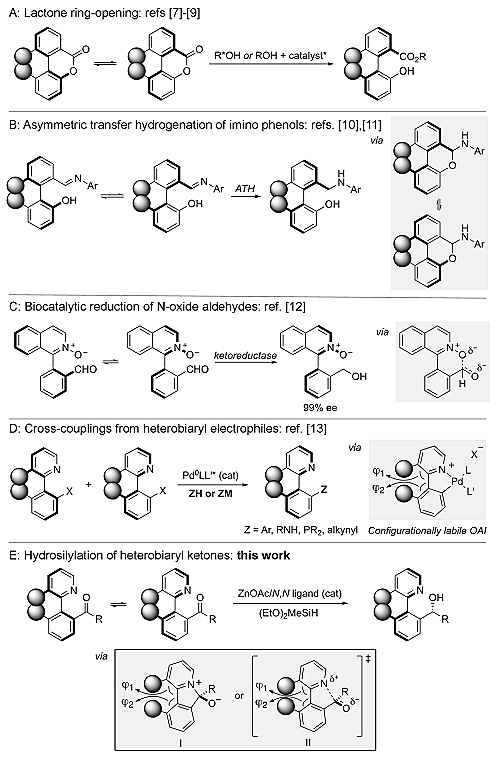
图1. 轴手性双芳基化合物的合成方法。图片来源:Angew. Chem. Int. Ed.
作者首先合成了酮2a,该化合物可由消旋的1a与乙烯基正丁醚通过Heck反应/水解两步高效合成,X射线单晶衍射分析确定了固态条件下1a以两种异构体的形成存在,然而手性HPLC分析只显示一个特征峰表明2a在溶液中构型不稳定,可发生互变异构。作者接着使用NaBH4对2a进行还原,手性HPLC分析表明体系中存在四种立体异构体。另一个证明酮2a构型不稳定的实验是手性烯醇醚中间体4的水解反应。反应需要将4缓慢加入过量的盐酸溶液中,反之将盐酸加入底物中时会产生消旋的异喹啉盐中间体。
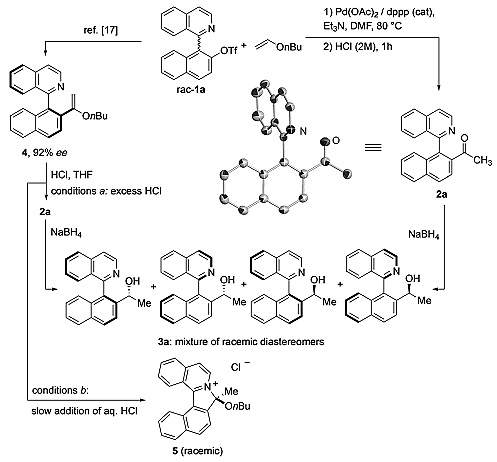
图2. 杂双芳基酮2a的合成。图片来源:Angew. Chem. Int. Ed.
接下来,作者以底物2a对反应条件进行了筛选,主要考察不同配体对反应结果的影响。当使用L1作为配体时,反应基本得到消旋的产物。作者接着增大配体R取代基的位阻,反应的对映选择性和非对映选择性都得到了显著的提高。权衡转化率和立体选择性,配体L6脱颖而出。
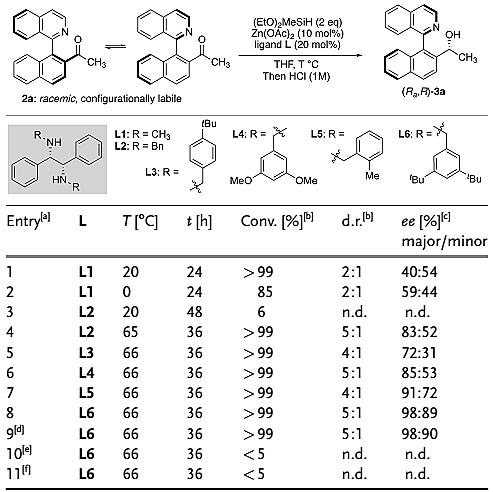
图3. 反应条件的筛选。图片来源:Angew. Chem. Int. Ed.
在最佳条件下,作者对底物的适用范围进行了考察,主要探究芳香环取代基和酮的R1取代基对反应结果的影响。总体来说,萘环取代基的位置对反应影响较小,不同底物都能以良好的结果实现动态动力学拆分。此外,单吡啶双芳基酮底物2c也能以93%的产率和96%的对映选择性得到目标产物。当使用含有嘧啶的双芳基酮底物2e时,由于产物的极性较大,作者将其转化为相应的醋酸酯,在分离时除了得到目标产物外,还得到了N-酰基化及分子内羟基1,2-加成的副产物。作者最后对R1取代基进行了考察,从反应结果可以看出,R1取代基对产率、对映选择性和非对映选择性影响较大,底物2i参与反应时非对映选择性非常好,但是产物的ee 值只有80%。
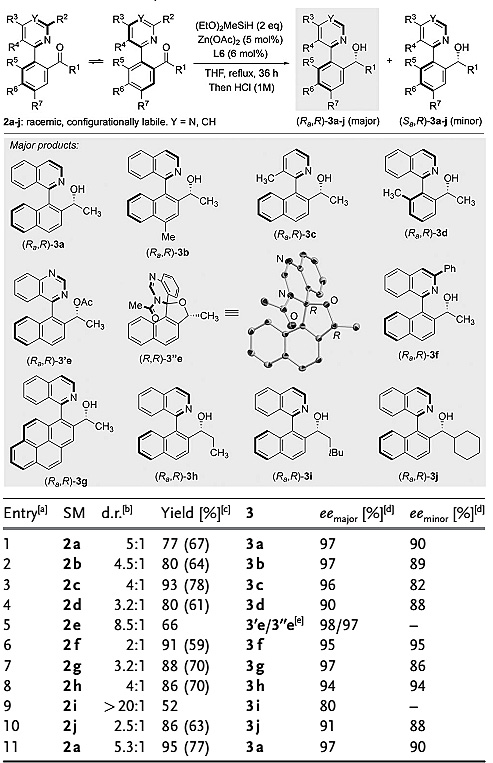
图4. 底物适用性的考察。图片来源:Angew. Chem. Int. Ed.
为了证明产物的实用性,作者对手性的3a进行了一系列的衍生化实验。首先3a可在m-CPBA的作用下以定量的产率氧化为氮氧化物醇6,也可以在DPPA/DBU的条件下将羟基转化为构型反转的叠氮化合物7。7可通过Cu(I)催化的环加成过程转化为手性双氮配体8。此外,化合物7可以先通过Staudinger还原反应得到相应的胺,接着与异硫氰酸酯反应得到手性硫脲化合物10。
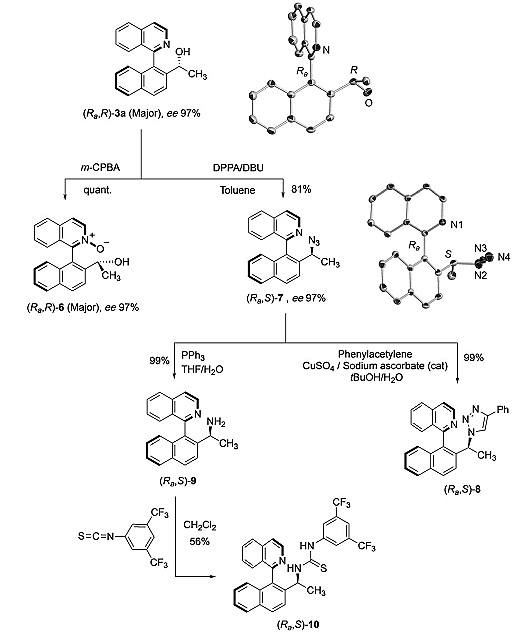
图5. 产物的衍生化。图片来源:Angew. Chem. Int. Ed.
总结
西班牙化学家基于杂芳香烃中氮原子与酮羰基之间的Lewis酸-碱相互作用,报道了锌催化杂双芳基酮的DKR反应,由此构建了包含轴手性及手性中心的二级醇产物。得到的手性化合物经过简单的衍生化过程可用于合成手性双氮鳌合配体和双官能化的手性硫脲催化剂,彰显了该方法的重要应用价值。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Dynamic Kinetic Resolution of Heterobiaryl Ketones by Zinc‐Catalyzed Asymmetric Hydrosilylation
Angew. Chem. Int. Ed., 2018, 57, 3777, DOI : 10.1002/anie.201713200
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号