基于肽段等重标记的蛋白质泛素化串级质谱定量新方法
注:文末有本文作者科研思路分析
蛋白质泛素化是生物体内一种常见的翻译后修饰,参与调节细胞周期进程、蛋白降解以及DNA修复等多种重要细胞生理过程。异常失调的蛋白质泛素化与许多疾病的发生、发展密切相关。在蛋白质组水平上对泛素化进行定性定量分析有助于更进一步了解生物体内蛋白质泛素化的进程,对于认识和治疗由于泛素化系统紊乱引起的各种疾病,尤其是恶性肿瘤具有重要意义。
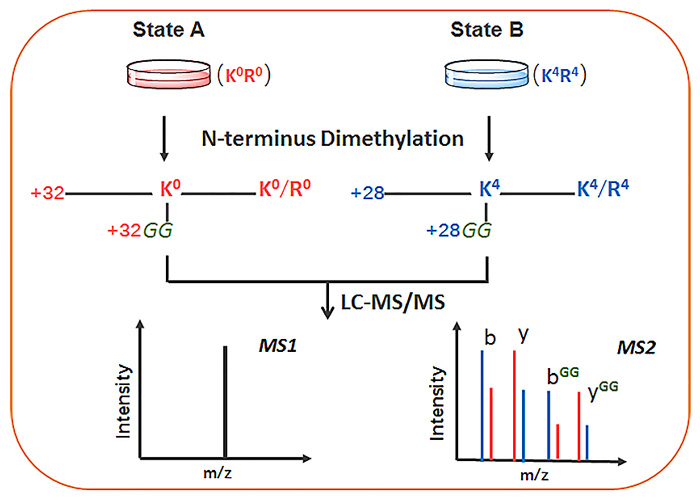
目前,蛋白质泛素化的定量方法主要是基于一级质谱定量的SILAC (Stable Isotope Labeling with Amino Acids in Cell Culture)以及部分基于串级质谱报告离子定量的iTRAQ(Isobaric Tags for Relative and Absolute Quantitation)和TMT (Tandem Mass Tags)。近年来,基于串级质谱碎片离子定量的肽段终端等重标记方法也开发应用于定量蛋白质组学中,这种定量方法克服了传统一级质谱定量干扰多、灵敏度低的缺陷。另一方面,利用整个串级谱图中碎片离子的定量克服了基于报告离子定量方法的低质量端抑制效应。同时,多对碎片离子也提供了更加准确、可靠的定量结果。复旦大学的陆豪杰教授(点击查看介绍)团队近年来也发展了一系列串级碎片离子定量的等重标记方法及相应的定量软件(Anal. Chem., 2011, 83, 6026; Proteomics, 2015, 15, 3755等)。近日,该团队首次将肽段等重标记应用于蛋白质泛素化的定量,结合SILAC标记以及肽段N端选择性的二甲基化反应,发展了一种基于泛素化肽段(K-ε-GG)等重标记的串级质谱b、y离子定量方法,实现了位点水平上蛋白质的泛素化定量。作者将该方法应用于MCF-7细胞样本,共准确定量得到2874个泛素化位点。除了肽段终端等重标记定量方法的固有优势,等重标记的K-ε-GG肽段在一级质谱中形成单峰,质谱响应信号增强,有利于复杂样本中泛素化肽段的鉴定分析。此外,对于多聚泛素化肽段,串级质谱b、y离子定量可以针对该肽段上每一个泛素化位点的变化提供独立的定量信息,实现了位点特异性的蛋白质泛素化定量,克服了一条肽段定量包含多个修饰位点变化情况的缺陷。
该论文作者为:Ting Cao, Lei Zhang, Ying Zhang, Guoquan Yan, Caiyun Fang, Huimin Bao and Haojie Lu
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Site-Specific Quantification of Protein Ubiquitination on MS2 Fragment Ion Level via Isobaric Peptide Labeling
Anal. Chem., 2017, 89, 11468, DOI: 10.1021/acs.analchem.7b02654
导师介绍
陆豪杰
http://www.x-mol.com/university/faculty/9645
科研思路分析
Q:这项研究的想法是如何产生的?
A:传统的翻译后修饰定量方法都是通过一条肽段的定量比值来反映肽段翻译后修饰的定量信息,当肽段上有多个翻译后修饰位点时,现有的方法都只能提供一个肽段总体的定量信息,很难将定量信息归属到每一个特定发生修饰的氨基酸位点。由于肽段终端等重标记定量的方法是利用串级质谱碎片离子定量,我们便可以将翻译后修饰的定量信息归属到具体被修饰的氨基酸残基上,从而实现位点特异性的定量。
Q:研究中遇到哪些挑战?
A:研究中遇到的主要挑战是对泛素化肽段的高效选择性富集。
Q:这项研究成果可能有哪些应用或社会效应?
A:首先,我们将肽段等重标记成功应用到蛋白质泛素化的定量当中,为蛋白质泛素化提供了一种新的准确可靠的定量分析方法。另一方面,该定量方法可以针对泛素化肽段上每一个泛素化位点的变化提供独立的定量信息,实现位点特异性的定量,这对于多聚泛素化肽段的定量来说尤为重要。我们也希望这一定量方法能有助于深入了解生物体内的蛋白质泛素化进程。
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号