磷-硼脱硫法:一种简单有效的多肽蛋白合成及特异性氘化反应
随着生物医学的快速发展,多肽及蛋白质的化学合成也越来越多地受到人们的关注。通过化学合成的方法,人们不仅可以将20种天然氨基酸以外的非天然氨基酸插入序列的任意位置,而且能够实现特定位点的蛋白翻译后修饰。然而传统的酰胺缩合反应难以实现较长肽链(50个氨基酸以上)的合成,并伴有产率低、易消旋等缺点。为此,人们希望能够通过化学选择性的连接过程对两段未保护的肽链进行偶联,在连接位点形成天然的肽键且不导致差向异构化。1994年,芝加哥大学的Stephen Kent教授课题组报道了一种基于半胱氨酸的天然化学连接(Native Chemical Ligation, NCL)反应(Science, 1994, 266, 776)。NCL利用N端半胱氨酸与C端硫酯之间的硫捕获及S-N部分酰基的迁移,可以高效生成“任意氨基酸-半胱氨酸”位点的肽键,并具有高化学选择性。然而,半胱氨酸的丰度较低(蛋白中的丰度为1.4%),极大地限制了NCL在蛋白合成方面的应用。为了解决此类问题,香港大学化学系的李学臣(点击查看介绍)课题组发展了丝氨酸/苏氨酸的连接反应(Serine/Threonine Ligation, STL)。在过去的数年中,他们将该反应相继成功应用于多肽药物(Org. Biomol. Chem., 2013, 11, 5584)、蛋白质ACYP1(Proc. Natl. Acad. Sci. U.S.A., 2013, 110, 6657)、糖蛋白IL-25(J. Am. Chem. Soc., 2016, 138, 10477)、核蛋白HMGA1a(Org. Lett., 2016, 18, 5944)、重复序列糖肽MUC1(Chem. Commun., 2013, 49, 6200)、环肽抗生素与天然产物(J. Am. Chem. Soc., 2013, 135, 6272; Org. Biomol. Chem., 2013, 11, 7616; Tetrahedron, 2014, 70, 7770; Nat. Commun., 2016, 7, 12394)以及高张力环状四肽(Angew. Chem. Int. Ed., 2013, 52, 10212)的合成,并对该反应的机理进行了研究(Front. Chem. Biol., 2014, 2, DOI: 10.3389/fchem.2014.00028)。
另外一个策略是首先在天然氨基酸的β或γ位引入巯基,然后完成类似NCL的连接过程,最后通过脱硫反应实现相应氨基酸位点肽键的生成。2001年,Dawson课题组报道了Pd/Al2O3和兰尼镍参与的脱硫反应(J. Am. Chem. Soc., 2001, 123, 526),成功将NCL产物中的半胱氨酸转化为丙氨酸,然而金属配合物极易与蛋白发生吸附。随后Danishefsky课题组报道了VA044/TCEP/tBuSH引发的无金属参与的自由基脱硫反应,引起该领域的技术革新,并得到了广泛的应用(Angew. Chem. Int. Ed., 2007, 46, 9248)。最近,李学臣课题组使用简单的硼-磷试剂,不仅能够实现多肽和蛋白的脱硫反应,而且还能在脱硫的位置特异性地引入氘元素。这一研究成果近期发表在Angewandte Chemie International Edition 上(VIP paper),论文的第一作者为博士研究生金康。
作者首先以简单的含硫多肽H-ACVCVRPRVMG-OH为底物,对多种反应条件进行了筛选。最终确定了使用TCEP-NaBH4或TCEP-LiBEt3H的pH = 6.0~7.0缓冲溶液为最优的反应条件。研究发现,TCEP以及硼试剂的投料顺序对反应同样具有至关重要的影响,如果先投入TCEP,或者先把两种试剂混合,反应都可顺利进行,而先投入NaBH4或LiBEt3H,反应则不能发生。随后作者又对含硫底物的适用范围进行考察,发现不同底物可以特异性地与半胱氨酸的巯基反应,而其他含硫基团,如Met、Biotin、Thz等均不受影响。
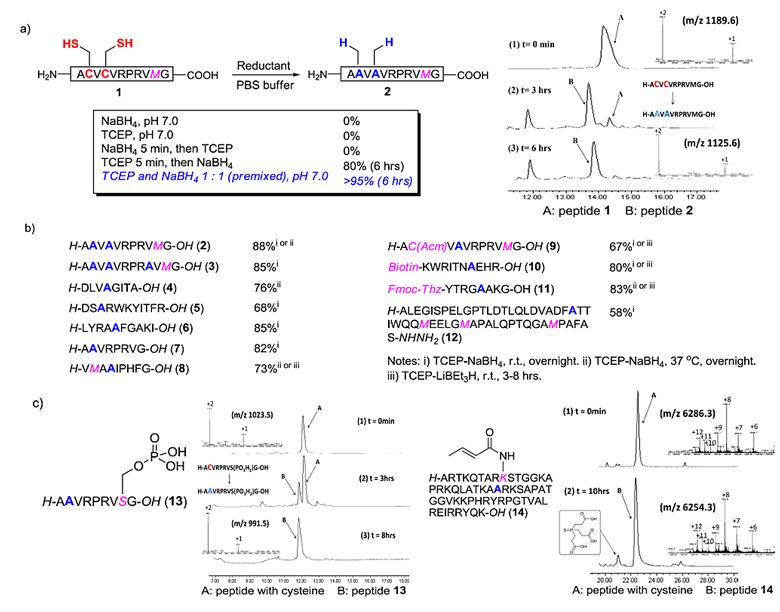
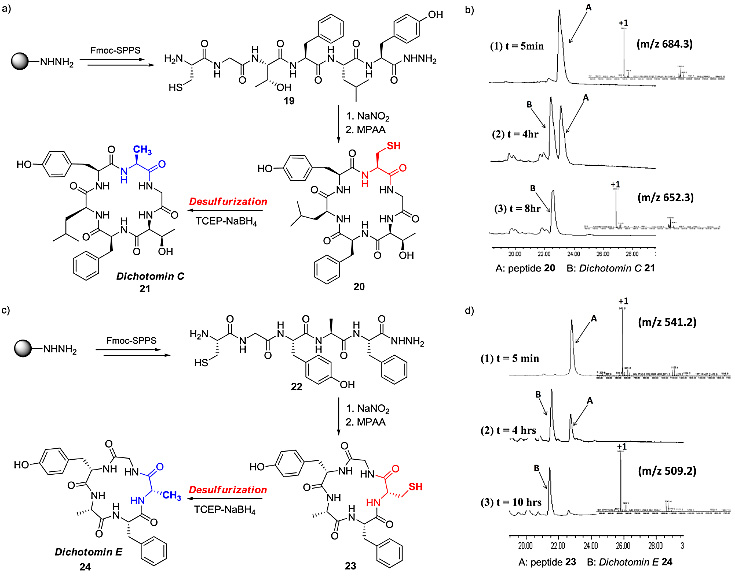
为了进一步拓展该方法的适用范围,作者分别选用两条磷酸化及巴豆酰化的含硫多肽作为底物,并使用“磷-硼脱硫法”成功将半胱氨酸残基转化为丙氨酸残基。与此同时,磷酸基团与含有C=C双键的巴豆酰基均未受到影响。此外,作者通过NCL与“磷-硼脱硫法”串联的方法还完成了天然活性环肽Dichotomin C 和Dichotomin E 的全合成。
随后,作者对该反应进行了初步的机理探究,并提出了较为合理的反应历程。在机理探究的过程中,作者还发现,使用重水作为反应溶剂可以成功将氘元素特定地引入脱硫位置。

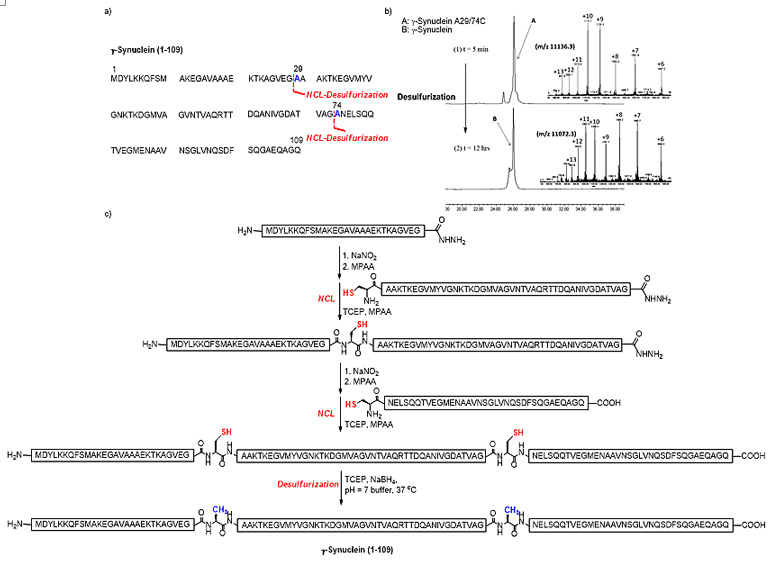
为了进一步验证反应的适用性,作者再次通过NCL与“磷-硼脱硫法”串联的策略成功实现了天然蛋白质ubiquitin、γ-synuclein 以及histone H2A 的全合成。
该论文作者为:Kang Jin, Tianlu Li, Hoi Yee Chow, Han Liu, Xuechen Li
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

P−B Desulfurization: An Enabling Method for Protein Chemical Synthesis and Site-Specific Deuteration
Angew. Chem. Int. Ed., 2017, 56, 14607, DOI: 10.1002/anie.201709097
李学臣博士简介
李学臣,香港大学化学系副教授;2006年于哈佛大学获得博士学位,2007-2009年于斯隆-凯特癌症研究中心从事博士后研究,2009年起供职于香港大学化学系。李学臣博士主要从事蛋白质、多肽及多糖的化学合成和化学生物学的研究,具体内容包括蛋白质化学合成新方法的研究(丝氨酸/苏氨酸连接反应, Serine/Threonine Ligation)、具有重要生物活性的环肽天然产物及结构类似物的合成与药物化学研究、疾病相关多糖的全合成研究、化学选择性蛋白质修饰研究等。
李学臣
http://www.x-mol.com/university/faculty/7051
课题组主页
http://www.chemistry.hku.hk/staff/xcli/XCLiGroup/index.html
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号