谍反应家族的拓展:以序列编码正交的蛋白质反应性
近年来,以谍反应为代表的多肽-蛋白质反应对吸引了众多研究者的目光。谍反应是谍标签(SpyTag)和谍捕手(SpyCatcher)之间自发形成异肽键的反应过程。该反应的两个组分完全基于天然氨基酸单元,可以通过基因编码的方式直接将化学反应性写入蛋白质的序列中,因而在蛋白质工程、生物材料、化学生物学和合成生物学等方面具有广泛的前景。北京大学的张文彬(点击查看介绍)课题组和来鲁华(点击查看介绍)课题组通过定向进化的方式改造了野生型谍标签和谍捕手的反应性,发现在极高的序列相似度下可以编码完全不同、甚至彼此正交的反应特性。
谍标签和谍捕手的氨基酸序列及折叠结构是影响其反应活性的关键因素,因此在相同的结构骨架下,通过改变序列即可改造其反应特性。但是,如何在双组份体系中区分强的物理结合作用和化学键合作用,实现化学反应性的定向进化是亟待解决的关键问题。这两个课题组首先通过计算分析了该反应对的接触界面,指认出对反应特异性和效率可能有影响的关键氨基酸残基,分别对其进行饱和突变,并通过细胞内的蛋白质原位环化反应来筛选具有反应性的突变体,实现了反应性的定向进化(图1)。
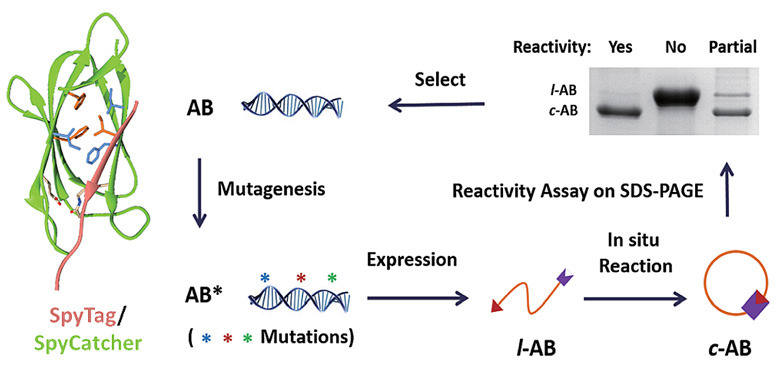
图1. 谍标签和谍捕手复合物的结构及相应的定向进化过程。
研究发现,增大谍标签上第三位氨基酸的侧链基团尺寸会使其对谍捕手的反应性减弱(I>F>Y>W),而减小谍捕手催化位点附近两个氨基酸的尺寸可以保留其与野生型谍标签的反应性。该谍捕手突变体BVA基本不与谍标签的酪氨酸突变体AY发生反应,但却能和具有更大侧链尺寸的色氨酸突变体Aw发生反应,并显示出与野生型谍捕手截然相反的温度依赖性。因此,野生型谍标签就好比一把万能钥匙,与谍捕手及其BVA突变体都能很好地反应;而谍标签AY就像一把子钥匙,只能选择性地和野生型谍捕手反应。有趣的是,谍标签Aw在低温下更倾向于和BVA突变体发生反应。因而在低温下,短时间内Aw 和BVA的反应与AY和B的反应之间几乎是彼此正交的(图2)。值得一提的是,这些迥异的反应特性是仅仅通过三个突变实现的。该项工作预示通过蛋白质工程可以发展反应性各异、具有不同特色的蛋白质-多肽反应对,不断丰富合成生物学的“化学工具箱”。
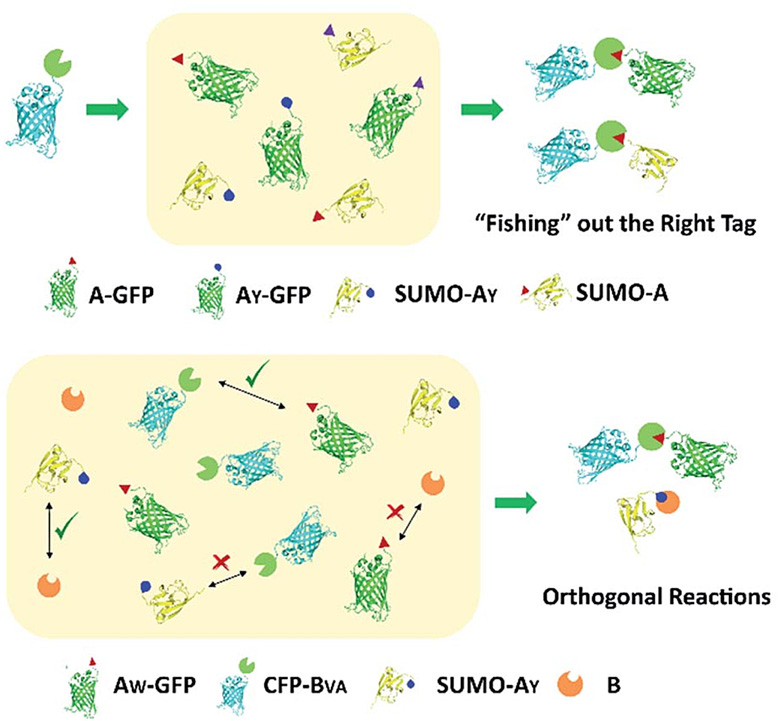
图2. 谍标签和谍捕手的突变体展示出丰富的反应特性。
这一成果近期发表在Chemical Science 上,文章的共同第一作者是北京大学博士研究生刘雅杰和博士后刘栋以及PTN(北大-清华-北京生命科学研究所)项目博士研究生杨为。
该论文作者为:Yajie Liu, Dong Liu, Wei Yang, Xia-Ling Wu, Luhua Lai, and Wen-Bin Zhang
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Tuning SpyTag–SpyCatcher mutant pairs toward orthogonal reactivity encryption
Chem. Sci., 2017, 8, 6577-6582, DOI: 10.1039/c7sc02686b
导师介绍
张文彬
http://www.x-mol.com/university/faculty/8713
来鲁华
http://www.x-mol.com/university/faculty/8669
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!










































 京公网安备 11010802027423号
京公网安备 11010802027423号