具有治疗潜力的新型环胍二聚体类抗生素
细菌的耐药性问题已经成为21世纪的三大全球公众健康危害之一。其中,包括耐甲氧西林金黄色葡萄球菌(MRSA)、耐甲氧西林表葡菌(MRSE)、抗万古霉素肠球菌(VRE)在内的革兰氏阳性菌,和包括大肠杆菌(E. coli)、克雷伯氏肺炎菌(K. pneumoniae)、绿脓杆菌(P. aeruginosa)在内的革兰氏阴性菌已成为医院里常见的感染源。研究发现能够有效抑制这些多重耐药细菌的新型抗生素一直是科学界不懈的追求之一。近日,南佛罗里达大学的蔡健峰教授团队和上海中医药大学的李琦教授团队报道了一类新的环胍二聚体类化合物并且系统研究了体外和体内活性以及其毒性和机理。
近些年来,宿主抵抗肽类(host-defense peptides, HDPs)被研究者发现成为一种可克服细菌耐药性的新型方法。众所周知,传统的抗生素都有明确的细胞膜或者细胞内靶点,然而,HDPs由于其特异的双亲性结构(具有带正电荷和亲脂性的基团),会优先通过跟细菌细胞壁结合从而破坏细菌的细胞壁,进而导致细菌死亡。HDPs的抗菌机理比较复杂,但其能选择性结合细胞壁进而破坏细胞壁的机理最能解释该肽类化合物可以大大减少耐药性的产生,因为其跟细菌细胞壁的结合主要是通过电荷-电荷作用而非特定的膜位靶点结合。该特殊机理也使HDPs具备广谱的抗菌活性。然而,HDPSs一般都是分子量较大(1500‒3000)的天然多肽,难于大量合成、原子经济效益低,且有潜在的免疫和系统毒性,最近许多研究者开始研究能够模拟HDPs功能的小分子化合物。
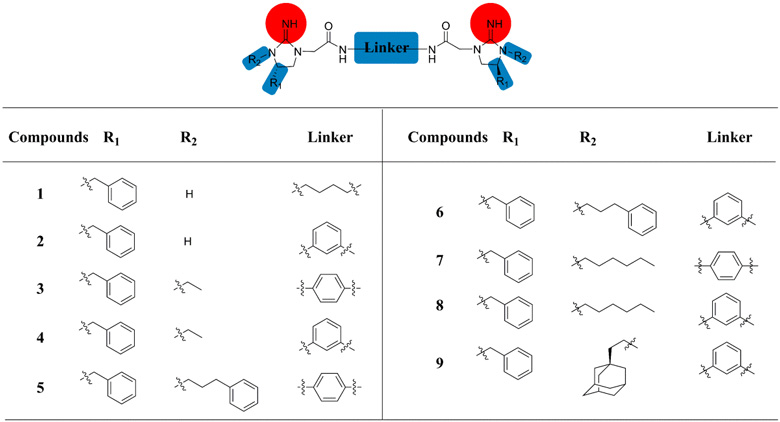
图 1. 环胍类二聚体结构。图片来源:Chem. Commun.
胍类化合物具有防腐和消毒的功效,最近有研究称环胍类化合物比胍类化合物具有更强的抗菌效果,胍基修饰的山酮类化合物具有类似HDPs的杀菌机理但是只对革兰氏阳性菌有效,结构对称的胍类化合物Brilacidin已经处在临床研究阶段等。基于此,作者设想结构对称的环胍类二聚体亦可模拟HDPs具有广谱杀菌效果。
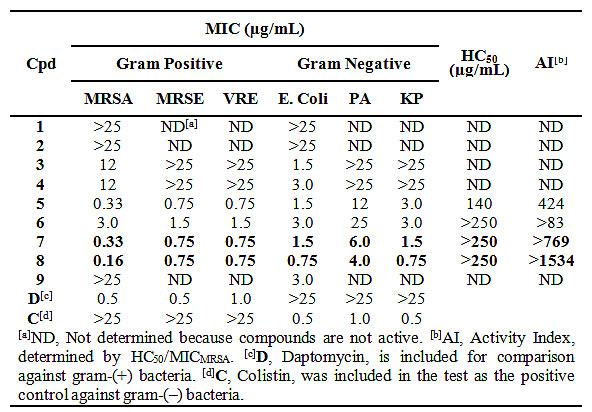
表1. 化合物1-9的抗菌活性
作者从最简单的天然氨基酸-苯丙氨酸出发,最终得到一系列结构对称的环胍类二聚体。从图1 和表1可见,此类化合物必须具备一定的两亲性结构,且其亲脂性/亲水性的比例必须经过精心调节才能有好的抗菌活性。其中,化合物7和8的体外活性最好,对所测三种革兰氏阳性菌的最小抑制浓度(MIC)都小于或等于0.75 μg/mL,跟阳性对照化合物Daptomycin的体外活性不相上下。更难得的是,7和8的对两种革兰氏阴性菌E. coli 和K. pneumoniae 的MIC也都小于等于1.5 μg/mL,只对P. aeruginosa 的活性略低,但是其MIC也好于绝大多数HDPs模拟物。
为了证明该类化合物具有类似HPDs的作用机制,作者利用荧光显微镜实验来观察加入化合物8之后细菌的变化。如图2 所示,由于细菌细胞壁被破坏进而发生细菌内DNA嵌入,化合物8处理过的细菌用碘化丙啶(PI)显色之后可以看到明显的红色,而不加化合物8的对照组(细菌仍然活着)无红色显示。作者还通过动力学实验发现,这类化合物可以快速杀死细菌。这些结果表明加入化合物8可以快速造成细菌细胞壁破坏进而导致细菌死亡,与HDPs 的作用机制吻合。
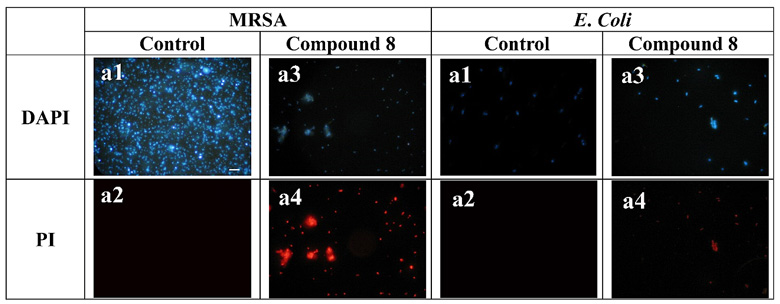
图2. 荧光显微镜实验表明化合物8可致MRSA和E. coli 的细胞壁破坏。图片来源:Chem. Commun.
细菌耐药性是作者考察的又一重要指标。图3表明,化合物8可以在14个连续考察期内MIC没有明显的升高,意味着MRSA和E. coli 对化合物在8不易产生耐药性。作者同时发现,化合物8还可以明显抑制E. coli 产生的生物膜(biofilms),而众所周知,细菌导致的生物膜比细菌更难杀死。最后,作者还考察了化合物7和8的体内实验效果,表明这类化合物可以明显抑制老鼠体内MRSA诱导的细菌感染,具有潜在的药用治疗效果。

图3. 化合物8的耐药性实验以及抑制E. coli 产生的biofilms实验结果。图片来源:Chem. Commun.
这一成果结果近期发表在Chemical Communications 上,文章的第一作者是南佛罗里达大学博士后滕鹏和博士研究生Alekhya Nimmagadda。
该论文作者为:Peng Teng, Alekhya Nimmagadda, Ma Su, Yuzhu Hong, Ning Shen, Chunpu Li, Ling-Yu Tsai, Jessica Cao, Qi Li, and Jianfeng Cai
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Novel bis-cyclic guanidines as potent membrane-active antibacterial agents with therapeutic potential
Chem. Commun., 2017, 53, 11948-11951, DOI:10.1039/C7CC07285F
蔡健峰教授课题组简介
蔡健峰,南佛罗里达大学副教授。2006年于Washington University in St. Louis获得博士学位,2007至2009年在耶鲁大学Andrew D. Hamilton(现任New York University校长)课题组做博士后。2009年起就职于南佛罗里达大学,于2015年获得终身教授名誉。
该组首次提出一种新型非天然多肽骨架AApeptide,研究工作主要集中于基于AApeptide的新型生物材料、人工蛋白质模拟结构(生物多聚体模拟结构)、活性药物分子和生物探针的研究,同时致力于新型蛋白结构的活性区域模拟以便得到具有独特催化功能。独立工作7年以来在J. Am. Chem. Soc., J. Med. Chem., Chem. Sci. Chem. Commun. 等杂志上已经发表了90篇文章,申请了12项专利,参与撰写了5本专业书籍,目前研究受到NSF、NIH等多项研究资助。
李琦教授课题组简介
李 琦,医学博士,教授、主任医师、博士生导师、博士后导师。现任上海中医药大学附属曙光医院肿瘤科主任。兼任世中联肿瘤经方研究专业委员会副会长,中国中医药研究促进会肿瘤专委会副主任委员,中华生物医学免疫学会常务理事,中华中医药学会肿瘤分会常委等。 先后入选“2017年国家百千万人才工程”、并获得“2017年国家卫计委突出贡献中青年专家”,国家重点学科带头人、全国百名杰出青年中医、上海市优秀学术带头人,上海市领军人才,上海市医学领军人才,上海市中医药领军人才等。获首届中国中西医结合优秀青年贡献奖、上海市银蛇奖、上海市科技创新标兵、明治生命科学奖等。
长期从事中西医结合肿瘤的医教研工作,主要进行中医药防治肿瘤转移的研究。主持国家重点学科1项、国家自然科学基金5项、重点国际合作项目1项,获省部级等项目30余项。研究成果获中华中医药科技奖、教育部科技奖、中华医学科技奖等科技奖等 1项,授权国家发明专利8项。发表论文252篇, SCI收录72篇;他引次数进入肿瘤学国际领域前1%。授权专利8项,主编医学专著3部。
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号