Nat. Chem.:大杀器?不,我只想安静地做个催化剂
谈到铀(Uranium),大多数人的第一反应可能就是原子弹这个大杀器。诚然,二战末期美军投到日本广岛的第一枚用于实战的原子弹“小男孩”,其巨大威力的源头就是U-235。自然界中天然存在的铀有三种同位素:U-238、U-235、U-234,其中U-238的含量最高,在99%以上。可用于核武器和核能的是U-235,提取浓缩U-235后的称为贫铀。由于核能的开发,大量的贫铀随之产生,这些贫铀储存以及可能导致的泄露均对环境造成威胁。寻求铀的其他利用方式,变废为宝,成为铀化学的重要方向。

“小男孩”爆炸之后产生的蘑菇云。图片来自网络
铀具有极大的原子半径和外层f轨道电子,铀配合物可以活化一些小分子化合物,如CO2、CO、N2和H2O[1]。但铀配合物在和小分子化合物作用时,大部分为典型的化学当量反应,而不是催化量反应。在还原H2O为H2时,低价态的铀配合物显示了很强的潜力,但反应过于剧烈和不可控制。2016年来自德国埃尔朗根-纽伦堡大学的Karsten Meyer等报道了第1个均相反应铀(III)催化剂[((Ad,MeArO)3mes)U](1),可电催化还原H2O为H2[2]。铀催化产氢,难点是催化剂的还原重生,即铀络合物含氧配体中U-O键的解离,催化还原的机理如下(图1):第1步,化合物1被H2O氧化生成2-OH并伴随着H2释放,在催化条件下(250eq H2O),2-OH的形成是瞬时的。第2步,化合物2-OH发生单电子电化学还原生成2-OH-,这一步的还原电势大约为-1.9 V。第3步,化合物2-OH-消除OH-,重新生成1进入下一个循环。
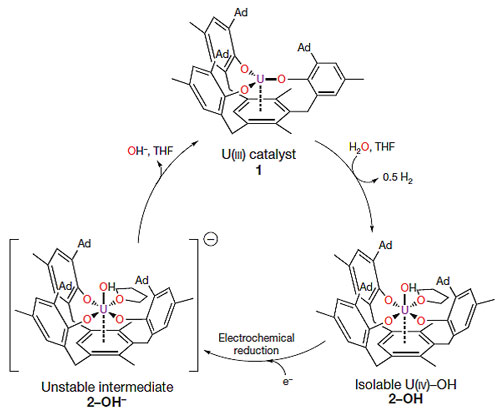
图1. 铀配合物催化还原H2O为H2的机理。图片来源:Nature
进一步,作者在分析机理时认为,催化循环过程可能经过了多种氧化态,如U(III)、U(IV)和U(V),这些氧化态通过配体中的氧稳定,其中的一些化合物已被分离表征,如化合物2-OH。化合物1电催化H2O还原反应时的价态变化如图2a所示,但其中的电子转移过程并不清楚。化合物3的结构与1类似,在H2O还原中却无催化活性。此外,在高价态的U(V)中间体中,铀与芳烃的相互作用也值得研究。

图2. 电催化还原时铀的价态变化,及化合物1和3的结构。图片来源:Nat. Chem.
近日,Karsten Meyer团队继续进行了这方面的理论研究,介绍了H2O还原催化循环中间体中铀-芳烃δ键的确切作用,以及H2O对三价铀催化剂的非典型双电子氧化加成的细节。相关论文发表在近期的Nature Chemistry 上。
作者合成和表征了U(V)和U(IV)氧配合物2和2-K(如图3所示),以分析催化循环中的细节,并且希望弄明白为什么化合物3的结构与1类似,但不像1一样具有H2O还原催化活性。N2O氧化1生成红色固体2,收率高达90%,继续用KC8还原2,生成棕-橙色粉末2-K,收率约为60%。这两个化合物的结构都经1H核磁结构确认,并适合低温单晶衍射,晶体结构见图4。
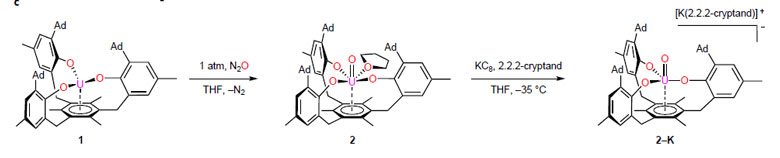
图3. 化合物2和2-K的结构及合成。图片来源:Nat. Chem.
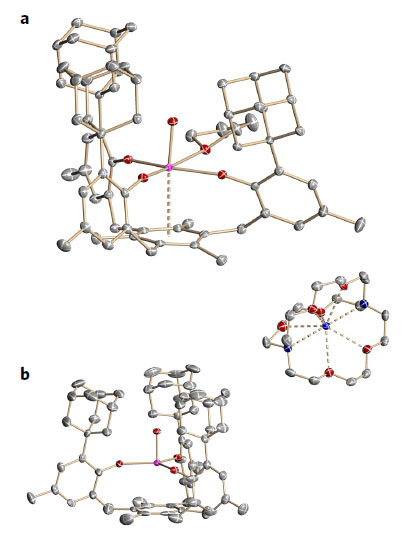
图 4. 铀配合物2(a)和2-K(b)的晶体结构。图片来源:Nat. Chem.
化合物2为C2/c单斜晶系,从化合物2的晶体结构中可以看到,U=O的键长为1.831(2) Å,符合文献上1.817-1.859 Å的范围。U=O、U-OAr的键长都在文献范围内,铀中心到三甲苯核的距离d(U-mescentr)为2.711(2) Å,比U(IV)卤素配合物稍长。这些数据也支持铀的价态越高,U-芳烃的距离越长的推测。化合物2-K属立方空间群P213,形成棕-黄色棱柱型晶体。因没有配位的THF,2-K为理想的C3v对称,所有的U-OAr的键长都相同为2.240(9) Å。2-K中铀中心到三甲苯核的距离d(U-mescentr)为2.810(6) Å,平均U-CAr的距离为3.136(6) Å,这些都比2长。作者进一步用EPR光谱研究了化合物2的电子结构,发现它表现出有机自由基和U(V)离子的信号峰。电化学和理论分析发现,U(V)中心与三甲苯形成了δ键(图5a),确定了2是第一个U(V)单芳烃配合物。三甲苯自由基呈正电性,为保持分子内电中性,大部分负电荷分布在一个螯合配体芳氧基手臂上。金属中心仅有9.6%的平衡电子密度(图5b)。三甲苯自由基部分占据了铀配合物2的最低未占分子轨道LUMO(图5c),可能直接参与了H2O还原循环。
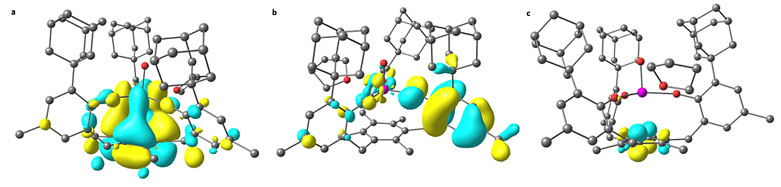
图5. 铀配合物2的电子结构计算分子轨道图。图片来源:Nat. Chem.
最后,为进一步理解铀催化剂1还原H2O的反应机理,作者对其进行了DFT水平上的计算研究,应用相对论有效原子实势(relativistic effective core potentials,RECPs)描述所有中间体的铀中心。以配合物1与水结合(结构A)开始,U(III)物种与H2O形成的O-U-mescentr键角推导为157.40°。从A开始,第1步是HO-H键的断裂,形成过渡态结构B,这时水分子通过η2-配位的O-H与铀结合,在铀金属中心形成一个扭曲的四方锥结构。与已知单电子转移不同,这步反应经历了双电子氧化加成。然后经过短暂的结构C,迅速释放两个氢到达过渡态D,最终生成U(V)氧配合物2(结构E)(图6)。

图6. 铀催化剂1还原H2O的计算反应概况。图片来源:Nat. Chem.
相对于其他风头正劲的过渡态金属,铀的催化反应才刚刚起步,但谁能知道它的潜力呢,毕竟用在催化上要比造贫铀弹好多了。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

The role of uranium–arene bonding in H2O reduction catalysis
Nat. Chem., 2017, DOI: 10.1038/nchem.2899
参考文献:
[1] Towards uranium catalysts. Nature, 2008, 455, 341-349, DOI: 10.1038/nature07372
[2] Uranium-mediated electrocatalytic dihydrogen production from water. Nature, 2016, 530, 317-321, DOI: 10.1038/nature16530.
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!











































 京公网安备 11010802027423号
京公网安备 11010802027423号