氧化脱氢[2+3]-环化反应构建咪唑啉类杂环化合物及其有趣的反应机理
转移一个电子是化学中最简单的基元反应之一。单电子氧化(OEO)反应,指的是从中性有机化合物分子中移走一个电子,生成的中间体称为自由基正离子。这样一个微小的变化,却会使有机分子的结构和反应性质产生巨大的改变。当一个分子被氧化成自由基正离子后,其α-位的碳氢键会显著变弱并酸性增强。利用这一原理,氧化脱氢碳氢官能团化反应近来已经成为一种重要有效的合成方法(Chem. Commun., 2016, 52, 13341)。
西北师范大学化学化工学院的霍聪德教授(点击查看介绍)课题组近年来通过单电子氧化活化反应底物,在有机化合物分子的碳氢键官能团化方面做了系统的工作。该小组在自氧化条件下实现了甘氨酸衍生物与吲哚的氧化偶联以及甘氨酸衍生物与烯烃之间的氧化波瓦罗夫芳构化串联反应(Angew. Chem. Int. Ed., 2014, 53, 13544)。还在自氧化条件下实现了苯硫酚与烯烃之间的双官能团化反应合成β-羟基硫醚衍生物(Chem. Commun., 2016, 52, 7233)。进一步通过苯硫酚与烯烃之间的一锅多步反应,制备了β-羟基砜衍生物。此反应优点如下:反应底物简单易得,反应试剂低价环保,溶剂毒性低,反应条件温和。并用此方法实现了抗癌药物康士得(Casodex)的克级制备(J. Org. Chem., 2017, 82, 10628)。
该小组也利用具有氧化还原活性的过渡金属铜、铁等做催化剂完成了一系列化学键的构造。例如:使用催化量的一价铜盐在氧气做末端氧化剂条件下实现了甘氨酸衍生物的芳基化反应(Adv. Synth. Catal., 2014, 356, 411)。实现了铜催化的有氧条件下甘氨酸衍生物和二氢呋喃、二氢吡咯之间的氧化环化串联反应,合成了系列的喹啉并内酯、喹啉并内酰胺衍生物。并将此新的反应方法应用于具有生物活性的骆驼宁碱类似物的合成(Adv. Synth. Catal., 2015, 357, 3648)。实现了铁催化的甘氨酸衍生物与四氢呋喃之间的双氧化脱氢偶联(DOD)串联环化反应,并同文提出了双氧化脱氢环化反应的概念(Org. Lett., 2015, 17, 5028)。实现了铜催化的有氧条件下甘氨酸衍生物与当归内酯之间的氧化脱氢[2+3]-环化反应,在温和简单的反应条件下制备了一系列复杂的吡咯烷酮类化合物(Org. Lett., 2015, 17, 4208)。在Fe/TBHP条件下,首次实现了苯并恶嗪酮3-位碳氢键的氧化脱氢官能团化。并利用此方法学,通过三步,克级规模制备了天然产物cephalandole A(Chem. Commun., 2016, 52, 13341)。在Fe/DDQ条件下,实现了苯并恶嗪酮与1,3-二羰基化合物或酮之间的氧化脱氢偶联反应。当使用磁性铁纳米颗粒做催化剂时,催化剂可以循环使用七次以上,催化活性无明显降低(Adv. Synth. Catal., 2017, 359, 3940)。
最近该小组在铜/氧气条件下实现了甘氨酸酯与氮杂环丙烷之间的氧化脱氢[2+3]-环化反应,构建咪唑啉类杂环骨架(Org. Lett., DOI: 10.1021/acs.orglett.7b03448)。这个反应是不是经历了经典的金属铜盐做催化剂,氧气做末端氧化剂的催化循环得到最终产物的呢?下面我们一起来了解一下。
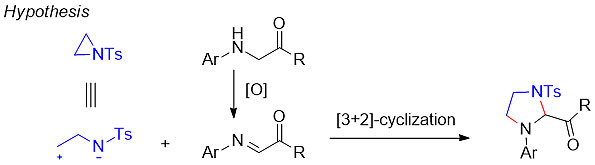
氮杂环丙烷是一类很容易得到的具有张力的三元环胺,它被广泛应用于制备各种各样的含氮杂环化合物。氮杂环丙烷被认为是一种1,3-偶极的前体化合物,可以与亲偶极化合物发生[3+2]-环化反应构建五元环。而甘氨酸衍生物可以被看作是亲偶极化合物的前体。在这些理论基础之上,作者设想以氧化脱氢方式实现甘氨酸衍生物与氮杂环丙烷之间的[3+2]-环化反应构建咪唑啉类杂环骨架。示意图如下:
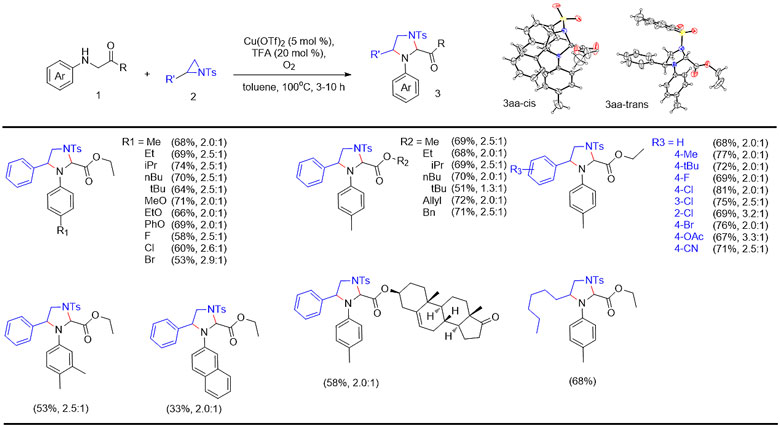
作者通过条件优化,确定了以Cu(OTf)2 (5 mol%)作催化剂,TFA (20mol%)作添加剂,甲苯作溶剂,温度100 ℃,氧气气氛为最优反应条件。以68%的收率得到了目标化合物3aa,并通过单晶衍射证实了结构的正确性。随后底物拓展顺利完成,30多个实例证实了反应的适用范围。
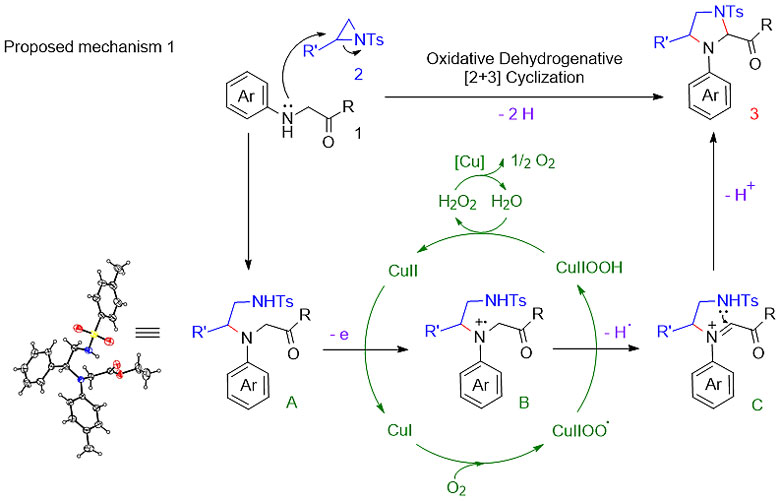
反应顺利实现,得到了设计的反应产物。然而反应机理是不是如前面所设想的那样呢?作者在反应研究过程中发现,会有一个明显的中间体的生成与消失,经过分离鉴定,中间体结构为A。由此可见,预想的反应途径不是真实的反应过程。此时,最容易想到的反应机理如下。即先发生分子间亲核开环后,再在铜/氧气的催化循环作用下氧化脱氢环化。
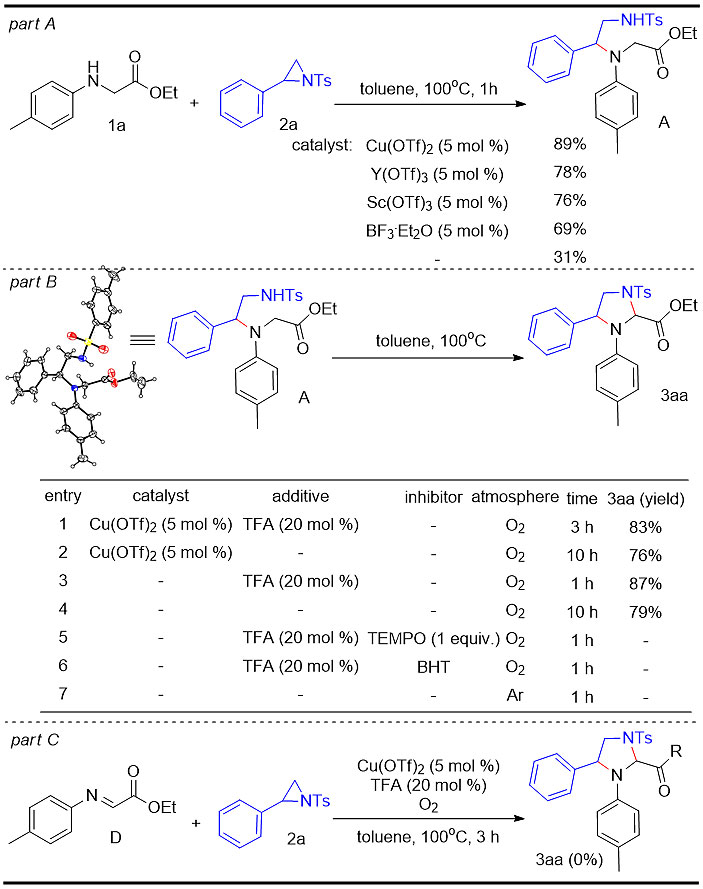
这一机理是否正确呢?作者随后又做了如下控制实验:
1、除Cu(OTf)2之外,一些常见的路易斯酸也可以促进产生中间体的亲核开环反应。
2、以中间体A为反应物,在标准条件下反应,产率83%;不加TFA,产率76%,反应速率变慢;不加Cu(OTf)2,产率87%,反应速率加快;既不加Cu(OTf)2,又不加TFA,产率依然可以达到79%,反应速率变慢。由此可见,这是一个质子酸促进的自氧化反应过程。而铜盐的作用只是作为路易斯酸促进前一步的亲核开环反应。
3、加入TEMPO、BHT等自由基抑制剂后,反应不能进行;惰气条件下,反应不能进行。由此可见,这是一个氧气参与的自由基反应过程。
4、亚胺中间体与氮杂环丙烷在标准条件下,不能得到目标产物。
5、在反应过程中,用HRMS检测到了氢过氧化物中间体B。
6、模板反应结束后,加入MnO2,有气体放出,间接证明了H2O2的存在。
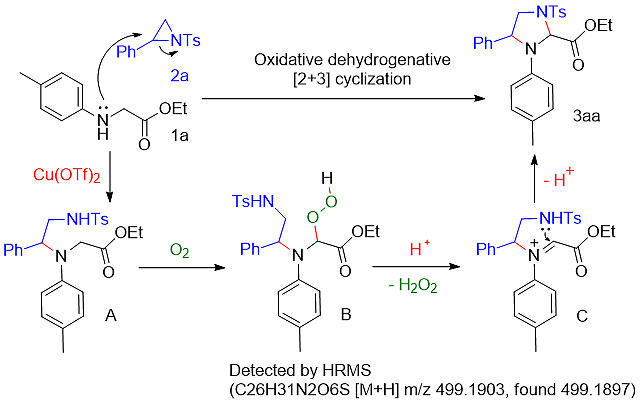
在这些控制实验基础上,作者给出了如下反应机理:氮杂环丙烷1a首先被甘氨酸衍生物2a亲核进攻开环得到中间体A;中间体A自氧化得到氢过氧化物B;B通过酸催化的SN1反应形成亚胺正离子中间体C;最后分子内构建C-N键得到目标化合物3aa。
这一成果近期发表在Org. Lett. 上,文章的第一作者是西北师范大学的硕士研究生李海涛。
该论文作者为:Haitao Li, Songhai Huang, Yajun Wang, Congde Huo
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Oxidative Dehydrogenative [2+3]-Cyclization of Glycine Esters with Aziridines Leading to Imidazolidines
Org. Lett., 2017, DOI: 10.1021/acs.orglett.7b03448
导师介绍
霍聪德
http://www.x-mol.com/university/faculty/13947
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号