Fe3+/Fe2+氧化还原电对调控阴极实现氯化氢电解回收氯气
氯气(Cl2)是一种重要的化工原料,广泛用于生产各种有机氯产品。大部分氯化反应是氯取代反应,每进行一个氯原子取代氢原子,就会有另一个氯原子同氢原子结合生成副产物氯化氢(HCl)。近年来,随着聚酯工业的急剧增长,氯气的需求量和氯化氢的产出量也随之迅速增长。因此,氯化氢中回收氯气的技术近年来成为科学研究的热点。
氯化氢中回收氯气可以采用催化氧化(Deacon)和电化学电解技术。催化氧化技术由于受到高腐蚀和缺乏高稳定催化剂的限制仍然处于实验室研发阶段,目前工业上从氯化氢中回收氯气仍然主要采用电解技术。在阳极一侧,HCl电解回收氯气可以采用盐酸水溶液或者HCl气体两种进料方式,相比于传统的盐酸进料方式,HCl气体进料的方式具有更低的阳极氧化电位(0.99 vs. 1.36 V,SHE,气相vs. 液相氯化氢标准电极电位)和更高的库仑效率,因而成为研究的主流。在阴极一侧,人们主要使用析氢阴极(HEC)或者氧气去极化阴极(ODC)。然而这两种阴极仍然导致阴极电位过低,从而需要更高的电解电压来运行,致使能量大量消耗。近日,美国特拉华大学的严玉山(点击查看介绍)团队采用Fe3+/Fe2+氧化还原电对调控阴极(IRC),设计了一种新的氯化氢电解回收氯气的过程。
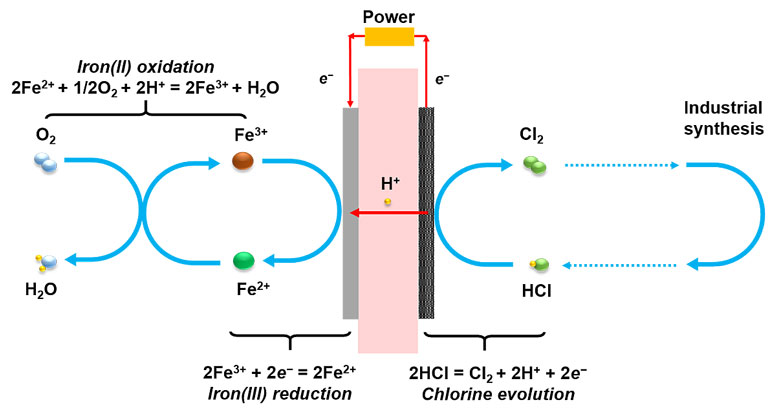
该团队设计的氯化氢电解回收氯气的过程主要包括电化学过程和化学过程(连接在电解池外的独立反应器)。电解过程如下:阳极一侧采用氯化氢气体阳极进料的方式,氯化氢气体直接氧化生成氯气、质子和电子;阴极一侧利用Fe3+还原反应生成Fe2+。化学过程如下:阴极一侧电解生成的Fe2+直接导入独立的Fe3+再生反应器,通入氧气或空气直接将Fe2+氧化为Fe3+,再将生成的Fe3+循环进入电解池,持续供给电解反应过程。Fe3+还原反应具有与生俱来的优势:(1)相对较高的标准氧化还原电位(0.77 vs. SHE);(2)使用碳材料即可具有较快的动力学,不像氧还原和析氢反应需要贵金属Pt基催化剂。因此,利用Fe3+/Fe2+氧化还原电对调控阴极,电解池的电压大幅度降低,大大减少了能耗。另外,阴极一侧仅需碳材料作为电极,相比于贵金属催化剂的HEC和ODC,IRC可以进一步降低成本。
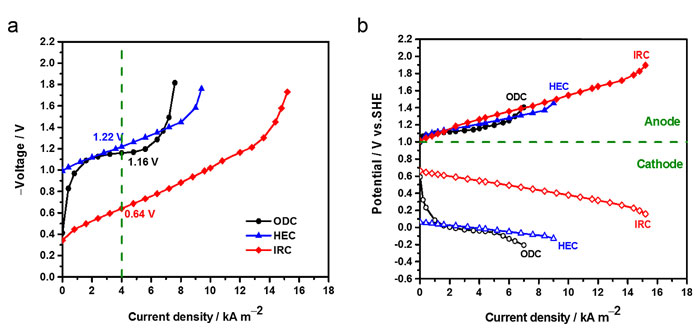
研究人员通过对阳极电极的优化以及设计制备了一种新的隔膜,最终使IRC电解过程的能耗降至当前核心氯化氢电解过程的50-55%左右。例如,反应在典型的4 kA•m-2电流密度下运行,IRC电解池的电解电压仅为0.64 V,而相应的HEC和ODC电解池分别需要1.22 V和1.16 V。同时,研究人员也进行了80小时的初步寿命试验,进一步证实了该设计的可行性。RC电解过程不需要使用昂贵的Nafion膜,阴极一侧不需要使用贵金属催化剂,因此,电解池的成本可降至当前核心氯化氢电解过程的一半左右。
这一成果近期发表在Angewandte Chemie International Edition 上,文章的第一作者是赵云博士。
该论文作者为:Yun Zhao, Shuang Gu, Ke Gong, Jie Zheng, Junhua Wang, Yushan Yan
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Low-Voltage Gaseous HCl Electrolysis with an Iron Redox-Mediated Cathode for Chlorine Regeneration
Angew. Chem. Int. Ed., 2017, 56, 10735, DOI: 10.1002/anie.201704749
导师介绍
严玉山
http://www.x-mol.com/university/faculty/47817
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!










































 京公网安备 11010802027423号
京公网安备 11010802027423号