Adv. Mater.:硒代半胱氨酸修饰的Bi2Se3纳米颗粒同步实现放疗增敏和防护
近年来,肿瘤的高发病率和高死亡率受到人们的普遍关注。放疗作为临床肿瘤治疗的三大基本疗法之一,在肿瘤治疗中占据较高的地位。据统计,70%左右的恶性肿瘤病人在疾病发展的不同阶段需要放疗控制,约有40%的恶性肿瘤可以通过放疗根治。但由于肿瘤组织内部分乏氧细胞的存在以及肿瘤细胞对潜在致死性损伤的修复,使部分肿瘤组织对放疗产生明显的抗性。传统的治疗只能通过进一步加大放疗剂量杀死更多的肿瘤细胞,而与此同时不可避免的会对正常组织产生辐射损伤。随着纳米技术和纳米医学的飞速发展,纳米放疗增敏剂在增强放射治疗效果领域表现出广阔的应用前景。但利用纳米放疗增敏剂在实现增强肿瘤放疗效果的同时,降低辐射对机体正常组织带来的毒副作用的研究尚无报道。
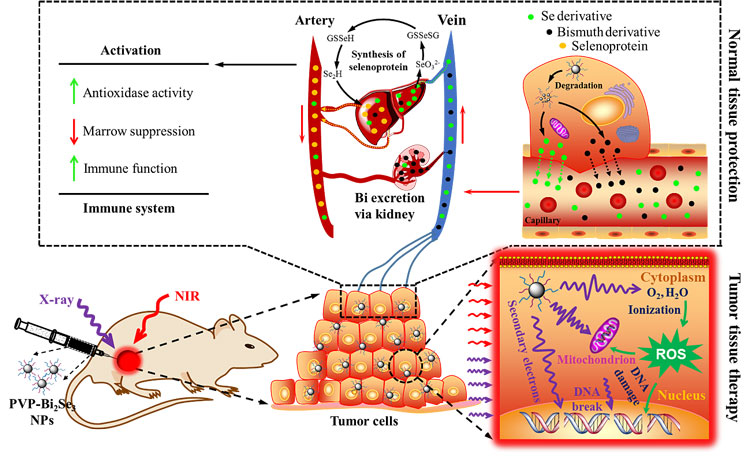
近日,苏州大学和中国科学院高能物理研究所纳米生物效应与安全性重点实验室的研究团队通过设计合成一种可生物降解的聚(乙烯基吡咯烷酮)和硒代半胱氨酸修饰的硒化铋(Bi2Se3)纳米材料,同步实现了对肿瘤放疗增敏和正常组织的放疗防护。一方面,Bi2Se3纳米颗粒的摩尔消光系数和X射线衰减系数分别为12.4 L•g-1和3.877 cm2•g-1(100 keV),表明该纳米颗粒具有优异的光热转化性能和X射线衰减能力,可以实现肿瘤光热治疗和放疗增敏;另一方面,该纳米颗粒体系的构建是以一种天然的硒代胱氨酸作为硒源,硒代半胱氨酸修饰的Bi2Se3具有良好的生物相容性,且可以生物降解并对正常组织起到放疗防护的作用。硒(Se)是一种人体必需的微量元素,适量地补硒可以提高机体的免疫力,维护心、肝、肺、胃等重要器官的正常功能。硒可以通过转化为硒代半胱氨酸参与硒蛋白的合成,进而催化一系列的电子转移反应,例如清除体内过多的自由基。研究发现,将硒代半胱氨酸包被的Bi2Se3纳米颗粒经原位注入小鼠肿瘤区域后,在热疗和放疗的协同作用下,肿瘤组织的大小得到了明显的抑制甚至消除。而肿瘤内的纳米颗粒通过在组织内缓慢降解,硒逐渐释放进入血液循环系统,通过在肝脏中合成硒酶或硒蛋白,提高机体的抗氧化活性、减少骨髓抑制并提高机体的免疫功能,最终增强机体正常组织对辐射的抵抗性,降低辐射带来的副作用。
相关工作发表在Advanced Materials 上,文章的第一作者是苏州大学的博士研究生杜江锋,共同通讯作者为赵宇亮研究员、谷战军研究员和陈春英研究员,共同通讯单位为苏州大学、中国科学院高能物理研究所、中国科学院大学和国家纳米科学中心。
该论文作者为:Jiangfeng Du, Zhanjun Gu, Liang Yan, Yuan Yong, Xuan Yi, Xiao Zhang, Jing Liu, Renfei Wu, Cuicui Ge, Chunying Chen, Yuliang Zhao
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Poly(Vinylpyrollidone)- and Selenocysteine-Modified Bi2Se3 Nanoparticles Enhance Radiotherapy Efficacy in Tumors and Promote Radioprotection in Normal Tissues
Adv. Mater., 2017, DOI: 10.1002/adma.201701268
导师介绍
赵宇亮
http://www.x-mol.com/university/faculty/23179
谷战军
http://www.x-mol.com/university/faculty/38291
谷战军课题组主页
陈春英
http://www.x-mol.com/university/faculty/23167
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号