当前位置:
X-MOL 学术
›
Nat. Rev. Nephrol.
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
Mechanisms of haemolysis-induced kidney injury.
Nature Reviews Nephrology ( IF 28.6 ) Pub Date : 2019-08-27 , DOI: 10.1038/s41581-019-0181-0 Kristof Van Avondt 1, 2 , Erfan Nur 3 , Sacha Zeerleder 1, 4, 5
Nature Reviews Nephrology ( IF 28.6 ) Pub Date : 2019-08-27 , DOI: 10.1038/s41581-019-0181-0 Kristof Van Avondt 1, 2 , Erfan Nur 3 , Sacha Zeerleder 1, 4, 5
Affiliation
|
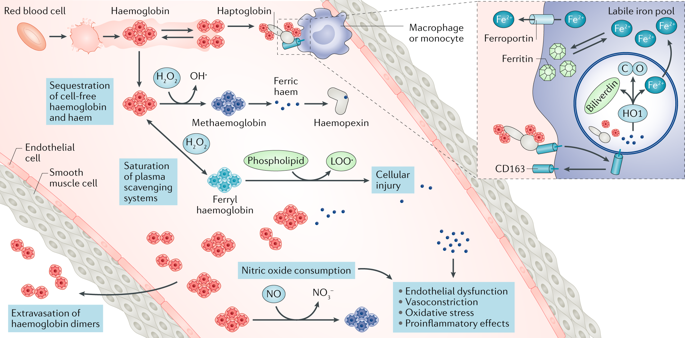
Intravascular haemolysis is a fundamental feature of chronic hereditary and acquired haemolytic anaemias, including those associated with haemoglobinopathies, complement disorders and infectious diseases such as malaria. Destabilization of red blood cells (RBCs) within the vasculature results in systemic inflammation, vasomotor dysfunction, thrombophilia and proliferative vasculopathy. The haemoprotein scavengers haptoglobin and haemopexin act to limit circulating levels of free haemoglobin, haem and iron - potentially toxic species that are released from injured RBCs. However, these adaptive defence systems can fail owing to ongoing intravascular disintegration of RBCs. Induction of the haem-degrading enzyme haem oxygenase 1 (HO1) - and potentially HO2 - represents a response to, and endogenous defence against, large amounts of cellular haem; however, this system can also become saturated. A frequent adverse consequence of massive and/or chronic haemolysis is kidney injury, which contributes to the morbidity and mortality of chronic haemolytic diseases. Intravascular destruction of RBCs and the resulting accumulation of haemoproteins can induce kidney injury via a number of mechanisms, including oxidative stress and cytotoxicity pathways, through the formation of intratubular casts and through direct as well as indirect proinflammatory effects, the latter via the activation of neutrophils and monocytes. Understanding of the detailed pathophysiology of haemolysis-induced kidney injury offers opportunities for the design and implementation of new therapeutic strategies to counteract the unfavourable and potentially fatal effects of haemolysis on the kidney.
中文翻译:

溶血性肾损伤的机制。
血管内溶血是慢性遗传性和获得性溶血性贫血的基本特征,包括与血红蛋白病、补体疾病和疟疾等传染病相关的贫血。脉管系统内红细胞 (RBC) 的不稳定会导致全身炎症、血管舒缩功能障碍、血栓形成倾向和增殖性血管病变。血红蛋白清除剂触珠蛋白和血红素结合蛋白可限制游离血红蛋白、血红素和铁的循环水平——这些物质从受伤的红细胞中释放出来,具有潜在的毒性。然而,这些适应性防御系统可能会由于红细胞的持续血管内分解而失效。血红素降解酶血红素加氧酶 1 (HO1) 以及潜在的 HO2 的诱导代表了对大量细胞血红素的反应和内源性防御;然而,这个系统也可能变得饱和。大量和/或慢性溶血的常见不良后果是肾损伤,这导致慢性溶血疾病的发病率和死亡率。红细胞的血管内破坏和由此产生的血红蛋白积累可通过多种机制诱导肾损伤,包括氧化应激和细胞毒性途径,通过管内管型的形成以及通过直接和间接的促炎作用,后者通过激活嗜中性粒细胞和单核细胞。了解溶血性肾损伤的详细病理生理学为设计和实施新的治疗策略以抵消溶血对肾脏的不利和潜在致命影响提供了机会。这个系统也可能变得饱和。大量和/或慢性溶血的常见不良后果是肾损伤,这导致慢性溶血疾病的发病率和死亡率。红细胞的血管内破坏和由此产生的血红蛋白积累可通过多种机制诱导肾损伤,包括氧化应激和细胞毒性途径,通过管内管型的形成以及通过直接和间接的促炎作用,后者通过激活嗜中性粒细胞和单核细胞。了解溶血性肾损伤的详细病理生理学为设计和实施新的治疗策略以抵消溶血对肾脏的不利和潜在致命影响提供了机会。这个系统也可能变得饱和。大量和/或慢性溶血的常见不良后果是肾损伤,这导致慢性溶血疾病的发病率和死亡率。红细胞的血管内破坏和由此产生的血红蛋白积累可通过多种机制诱导肾损伤,包括氧化应激和细胞毒性途径,通过管内管型的形成以及通过直接和间接的促炎作用,后者通过激活嗜中性粒细胞和单核细胞。了解溶血性肾损伤的详细病理生理学为设计和实施新的治疗策略以抵消溶血对肾脏的不利和潜在致命影响提供了机会。大量和/或慢性溶血的常见不良后果是肾损伤,这导致慢性溶血疾病的发病率和死亡率。红细胞的血管内破坏和由此产生的血红蛋白积累可通过多种机制诱导肾损伤,包括氧化应激和细胞毒性途径,通过管内管型的形成以及通过直接和间接的促炎作用,后者通过激活嗜中性粒细胞和单核细胞。了解溶血性肾损伤的详细病理生理学为设计和实施新的治疗策略以抵消溶血对肾脏的不利和潜在致命影响提供了机会。大量和/或慢性溶血的常见不良后果是肾损伤,这导致慢性溶血疾病的发病率和死亡率。红细胞的血管内破坏和由此产生的血红蛋白积累可通过多种机制诱导肾损伤,包括氧化应激和细胞毒性途径,通过管内管型的形成以及通过直接和间接的促炎作用,后者通过激活嗜中性粒细胞和单核细胞。了解溶血性肾损伤的详细病理生理学为设计和实施新的治疗策略以抵消溶血对肾脏的不利和潜在致命影响提供了机会。这有助于慢性溶血性疾病的发病率和死亡率。红细胞的血管内破坏和由此产生的血红蛋白积累可通过多种机制诱导肾损伤,包括氧化应激和细胞毒性途径,通过管内管型的形成以及通过直接和间接的促炎作用,后者通过激活嗜中性粒细胞和单核细胞。了解溶血性肾损伤的详细病理生理学为设计和实施新的治疗策略以抵消溶血对肾脏的不利和潜在致命影响提供了机会。这有助于慢性溶血性疾病的发病率和死亡率。红细胞的血管内破坏和由此产生的血红蛋白积累可通过多种机制诱导肾损伤,包括氧化应激和细胞毒性途径,通过管内管型的形成以及通过直接和间接的促炎作用,后者通过激活嗜中性粒细胞和单核细胞。了解溶血性肾损伤的详细病理生理学为设计和实施新的治疗策略以抵消溶血对肾脏的不利和潜在致命影响提供了机会。红细胞的血管内破坏和由此产生的血红蛋白积累可通过多种机制诱导肾损伤,包括氧化应激和细胞毒性途径,通过管内管型的形成以及通过直接和间接的促炎作用,后者通过激活嗜中性粒细胞和单核细胞。了解溶血性肾损伤的详细病理生理学为设计和实施新的治疗策略以抵消溶血对肾脏的不利和潜在致命影响提供了机会。红细胞的血管内破坏和由此产生的血红蛋白积累可通过多种机制诱导肾损伤,包括氧化应激和细胞毒性途径,通过管内管型的形成以及通过直接和间接的促炎作用,后者通过激活嗜中性粒细胞和单核细胞。了解溶血性肾损伤的详细病理生理学为设计和实施新的治疗策略以抵消溶血对肾脏的不利和潜在致命影响提供了机会。后者通过中性粒细胞和单核细胞的激活。了解溶血性肾损伤的详细病理生理学为设计和实施新的治疗策略以抵消溶血对肾脏的不利和潜在致命影响提供了机会。后者通过中性粒细胞和单核细胞的激活。了解溶血性肾损伤的详细病理生理学为设计和实施新的治疗策略以抵消溶血对肾脏的不利和潜在致命影响提供了机会。
更新日期:2019-08-28
中文翻译:

溶血性肾损伤的机制。
血管内溶血是慢性遗传性和获得性溶血性贫血的基本特征,包括与血红蛋白病、补体疾病和疟疾等传染病相关的贫血。脉管系统内红细胞 (RBC) 的不稳定会导致全身炎症、血管舒缩功能障碍、血栓形成倾向和增殖性血管病变。血红蛋白清除剂触珠蛋白和血红素结合蛋白可限制游离血红蛋白、血红素和铁的循环水平——这些物质从受伤的红细胞中释放出来,具有潜在的毒性。然而,这些适应性防御系统可能会由于红细胞的持续血管内分解而失效。血红素降解酶血红素加氧酶 1 (HO1) 以及潜在的 HO2 的诱导代表了对大量细胞血红素的反应和内源性防御;然而,这个系统也可能变得饱和。大量和/或慢性溶血的常见不良后果是肾损伤,这导致慢性溶血疾病的发病率和死亡率。红细胞的血管内破坏和由此产生的血红蛋白积累可通过多种机制诱导肾损伤,包括氧化应激和细胞毒性途径,通过管内管型的形成以及通过直接和间接的促炎作用,后者通过激活嗜中性粒细胞和单核细胞。了解溶血性肾损伤的详细病理生理学为设计和实施新的治疗策略以抵消溶血对肾脏的不利和潜在致命影响提供了机会。这个系统也可能变得饱和。大量和/或慢性溶血的常见不良后果是肾损伤,这导致慢性溶血疾病的发病率和死亡率。红细胞的血管内破坏和由此产生的血红蛋白积累可通过多种机制诱导肾损伤,包括氧化应激和细胞毒性途径,通过管内管型的形成以及通过直接和间接的促炎作用,后者通过激活嗜中性粒细胞和单核细胞。了解溶血性肾损伤的详细病理生理学为设计和实施新的治疗策略以抵消溶血对肾脏的不利和潜在致命影响提供了机会。这个系统也可能变得饱和。大量和/或慢性溶血的常见不良后果是肾损伤,这导致慢性溶血疾病的发病率和死亡率。红细胞的血管内破坏和由此产生的血红蛋白积累可通过多种机制诱导肾损伤,包括氧化应激和细胞毒性途径,通过管内管型的形成以及通过直接和间接的促炎作用,后者通过激活嗜中性粒细胞和单核细胞。了解溶血性肾损伤的详细病理生理学为设计和实施新的治疗策略以抵消溶血对肾脏的不利和潜在致命影响提供了机会。大量和/或慢性溶血的常见不良后果是肾损伤,这导致慢性溶血疾病的发病率和死亡率。红细胞的血管内破坏和由此产生的血红蛋白积累可通过多种机制诱导肾损伤,包括氧化应激和细胞毒性途径,通过管内管型的形成以及通过直接和间接的促炎作用,后者通过激活嗜中性粒细胞和单核细胞。了解溶血性肾损伤的详细病理生理学为设计和实施新的治疗策略以抵消溶血对肾脏的不利和潜在致命影响提供了机会。大量和/或慢性溶血的常见不良后果是肾损伤,这导致慢性溶血疾病的发病率和死亡率。红细胞的血管内破坏和由此产生的血红蛋白积累可通过多种机制诱导肾损伤,包括氧化应激和细胞毒性途径,通过管内管型的形成以及通过直接和间接的促炎作用,后者通过激活嗜中性粒细胞和单核细胞。了解溶血性肾损伤的详细病理生理学为设计和实施新的治疗策略以抵消溶血对肾脏的不利和潜在致命影响提供了机会。这有助于慢性溶血性疾病的发病率和死亡率。红细胞的血管内破坏和由此产生的血红蛋白积累可通过多种机制诱导肾损伤,包括氧化应激和细胞毒性途径,通过管内管型的形成以及通过直接和间接的促炎作用,后者通过激活嗜中性粒细胞和单核细胞。了解溶血性肾损伤的详细病理生理学为设计和实施新的治疗策略以抵消溶血对肾脏的不利和潜在致命影响提供了机会。这有助于慢性溶血性疾病的发病率和死亡率。红细胞的血管内破坏和由此产生的血红蛋白积累可通过多种机制诱导肾损伤,包括氧化应激和细胞毒性途径,通过管内管型的形成以及通过直接和间接的促炎作用,后者通过激活嗜中性粒细胞和单核细胞。了解溶血性肾损伤的详细病理生理学为设计和实施新的治疗策略以抵消溶血对肾脏的不利和潜在致命影响提供了机会。红细胞的血管内破坏和由此产生的血红蛋白积累可通过多种机制诱导肾损伤,包括氧化应激和细胞毒性途径,通过管内管型的形成以及通过直接和间接的促炎作用,后者通过激活嗜中性粒细胞和单核细胞。了解溶血性肾损伤的详细病理生理学为设计和实施新的治疗策略以抵消溶血对肾脏的不利和潜在致命影响提供了机会。红细胞的血管内破坏和由此产生的血红蛋白积累可通过多种机制诱导肾损伤,包括氧化应激和细胞毒性途径,通过管内管型的形成以及通过直接和间接的促炎作用,后者通过激活嗜中性粒细胞和单核细胞。了解溶血性肾损伤的详细病理生理学为设计和实施新的治疗策略以抵消溶血对肾脏的不利和潜在致命影响提供了机会。后者通过中性粒细胞和单核细胞的激活。了解溶血性肾损伤的详细病理生理学为设计和实施新的治疗策略以抵消溶血对肾脏的不利和潜在致命影响提供了机会。后者通过中性粒细胞和单核细胞的激活。了解溶血性肾损伤的详细病理生理学为设计和实施新的治疗策略以抵消溶血对肾脏的不利和潜在致命影响提供了机会。







































 京公网安备 11010802027423号
京公网安备 11010802027423号