当前位置:
X-MOL 学术
›
Nat. Rev. Urol.
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
Epigenetic drugs and their molecular targets in testicular germ cell tumours.
Nature Reviews Urology ( IF 12.1 ) Pub Date : 2019-04-01 , DOI: 10.1038/s41585-019-0154-x Sina Jostes 1 , Daniel Nettersheim 2 , Hubert Schorle 1
Nature Reviews Urology ( IF 12.1 ) Pub Date : 2019-04-01 , DOI: 10.1038/s41585-019-0154-x Sina Jostes 1 , Daniel Nettersheim 2 , Hubert Schorle 1
Affiliation
|
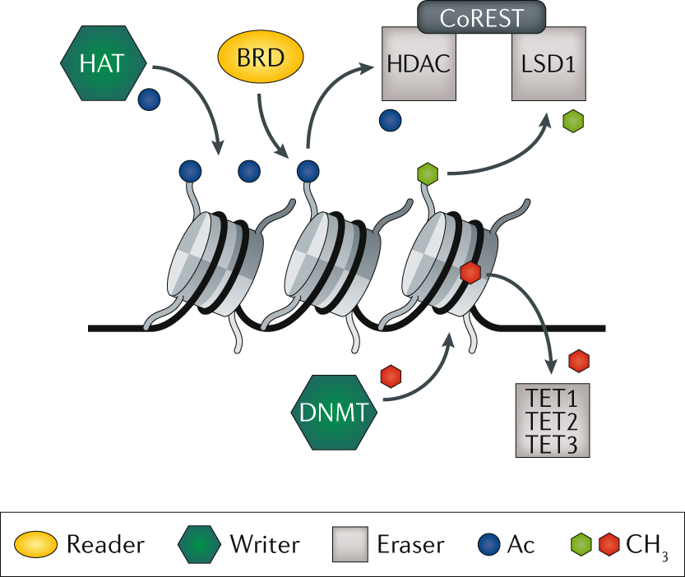
Current treatment regimens for type II testicular germ cell tumours (TGCTs) achieve cure rates of ≥95%; however, 1-5% of TGCTs develop resistance to standard platinum-based chemotherapy. Patients with recurrent TGCT typically receive high-dose chemotherapy, but this treatment results in severe adverse effects and cytotoxicity. Thus, alternative treatment options should be considered to improve patient well-being and quality of life. Epigenetic drugs could be feasible options for TGCT treatment. Several compounds have already been tested in TGCT cell lines and xenograft models with promising results. These compounds include DNA demethylating agents (such as SGI-110), histone demethylase inhibitors (such as the lysine-specific histone demethylase 1A (LSD1) inhibitor CBB3001), histone deacetylase (HDAC) inhibitors (such as romidepsin) and bromodomain inhibitors (such as JQ1). Despite the diversity in their molecular effects, most epigenetic compounds show strong overlap in their genetic response. The use of epigenetic drugs in TGCTs triggers a cellular stress response, induction of differentiation and downregulation of genes associated with pluripotency, leading to growth arrest and apoptosis. Additive effects are seen using a combination of JQ1 and romidepsin. The availability of dual drugs (such as LSD1-HDAC1 hybrid inhibitors) could additionally take advantage of drug synergy effects. Thus, epigenetic drugs are novel tools that could be combined with standard therapy approaches to improve treatment of TGCTs.
中文翻译:

睾丸生殖细胞肿瘤中的表观遗传药物及其分子靶点。
目前针对 II 型睾丸生殖细胞肿瘤 (TGCT) 的治疗方案可实现≥95% 的治愈率;然而,1-5% 的 TGCT 对标准的铂类化疗产生耐药性。复发性 TGCT 患者通常接受大剂量化疗,但这种治疗会导致严重的副作用和细胞毒性。因此,应考虑替代治疗方案以改善患者的幸福感和生活质量。表观遗传药物可能是 TGCT 治疗的可行选择。几种化合物已经在 TGCT 细胞系和异种移植模型中进行了测试,结果令人鼓舞。这些化合物包括 DNA 去甲基化剂(如 SGI-110)、组蛋白去甲基化酶抑制剂(如赖氨酸特异性组蛋白去甲基化酶 1A (LSD1) 抑制剂 CBB3001)、组蛋白去乙酰化酶 (HDAC) 抑制剂(如罗米地辛)和溴结构域抑制剂(如 JQ1)。尽管它们的分子效应存在多样性,但大多数表观遗传化合物在其遗传反应中表现出强烈的重叠。在 TGCT 中使用表观遗传药物会引发细胞应激反应、诱导分化和与多能性相关的基因下调,从而导致生长停滞和细胞凋亡。使用 JQ1 和 romidepsin 的组合可以看到附加效应。双重药物(如 LSD1-HDAC1 混合抑制剂)的可用性可以另外利用药物协同效应。因此,表观遗传药物是可以与标准治疗方法相结合以改善 TGCT 治疗的新型工具。大多数表观遗传化合物在其遗传反应中表现出强烈的重叠。在 TGCT 中使用表观遗传药物会引发细胞应激反应、诱导分化和与多能性相关的基因下调,从而导致生长停滞和细胞凋亡。使用 JQ1 和 romidepsin 的组合可以看到附加效应。双重药物(如 LSD1-HDAC1 混合抑制剂)的可用性可以另外利用药物协同效应。因此,表观遗传药物是可以与标准治疗方法相结合以改善 TGCT 治疗的新型工具。大多数表观遗传化合物在其遗传反应中表现出强烈的重叠。在 TGCT 中使用表观遗传药物会引发细胞应激反应、诱导分化和与多能性相关的基因下调,从而导致生长停滞和细胞凋亡。使用 JQ1 和 romidepsin 的组合可以看到附加效应。双重药物(如 LSD1-HDAC1 混合抑制剂)的可用性可以另外利用药物协同效应。因此,表观遗传药物是可以与标准治疗方法相结合以改善 TGCT 治疗的新型工具。使用 JQ1 和 romidepsin 的组合可以看到附加效应。双重药物(如 LSD1-HDAC1 混合抑制剂)的可用性可以另外利用药物协同效应。因此,表观遗传药物是可以与标准治疗方法相结合以改善 TGCT 治疗的新型工具。使用 JQ1 和 romidepsin 的组合可以看到附加效应。双重药物(如 LSD1-HDAC1 混合抑制剂)的可用性可以另外利用药物协同效应。因此,表观遗传药物是可以与标准治疗方法相结合以改善 TGCT 治疗的新型工具。
更新日期:2019-07-05
中文翻译:

睾丸生殖细胞肿瘤中的表观遗传药物及其分子靶点。
目前针对 II 型睾丸生殖细胞肿瘤 (TGCT) 的治疗方案可实现≥95% 的治愈率;然而,1-5% 的 TGCT 对标准的铂类化疗产生耐药性。复发性 TGCT 患者通常接受大剂量化疗,但这种治疗会导致严重的副作用和细胞毒性。因此,应考虑替代治疗方案以改善患者的幸福感和生活质量。表观遗传药物可能是 TGCT 治疗的可行选择。几种化合物已经在 TGCT 细胞系和异种移植模型中进行了测试,结果令人鼓舞。这些化合物包括 DNA 去甲基化剂(如 SGI-110)、组蛋白去甲基化酶抑制剂(如赖氨酸特异性组蛋白去甲基化酶 1A (LSD1) 抑制剂 CBB3001)、组蛋白去乙酰化酶 (HDAC) 抑制剂(如罗米地辛)和溴结构域抑制剂(如 JQ1)。尽管它们的分子效应存在多样性,但大多数表观遗传化合物在其遗传反应中表现出强烈的重叠。在 TGCT 中使用表观遗传药物会引发细胞应激反应、诱导分化和与多能性相关的基因下调,从而导致生长停滞和细胞凋亡。使用 JQ1 和 romidepsin 的组合可以看到附加效应。双重药物(如 LSD1-HDAC1 混合抑制剂)的可用性可以另外利用药物协同效应。因此,表观遗传药物是可以与标准治疗方法相结合以改善 TGCT 治疗的新型工具。大多数表观遗传化合物在其遗传反应中表现出强烈的重叠。在 TGCT 中使用表观遗传药物会引发细胞应激反应、诱导分化和与多能性相关的基因下调,从而导致生长停滞和细胞凋亡。使用 JQ1 和 romidepsin 的组合可以看到附加效应。双重药物(如 LSD1-HDAC1 混合抑制剂)的可用性可以另外利用药物协同效应。因此,表观遗传药物是可以与标准治疗方法相结合以改善 TGCT 治疗的新型工具。大多数表观遗传化合物在其遗传反应中表现出强烈的重叠。在 TGCT 中使用表观遗传药物会引发细胞应激反应、诱导分化和与多能性相关的基因下调,从而导致生长停滞和细胞凋亡。使用 JQ1 和 romidepsin 的组合可以看到附加效应。双重药物(如 LSD1-HDAC1 混合抑制剂)的可用性可以另外利用药物协同效应。因此,表观遗传药物是可以与标准治疗方法相结合以改善 TGCT 治疗的新型工具。使用 JQ1 和 romidepsin 的组合可以看到附加效应。双重药物(如 LSD1-HDAC1 混合抑制剂)的可用性可以另外利用药物协同效应。因此,表观遗传药物是可以与标准治疗方法相结合以改善 TGCT 治疗的新型工具。使用 JQ1 和 romidepsin 的组合可以看到附加效应。双重药物(如 LSD1-HDAC1 混合抑制剂)的可用性可以另外利用药物协同效应。因此,表观遗传药物是可以与标准治疗方法相结合以改善 TGCT 治疗的新型工具。











































 京公网安备 11010802027423号
京公网安备 11010802027423号