当前位置:
X-MOL 学术
›
ACS Biomater. Sci. Eng.
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
Endothelial Cell Migration Regulated by Surface Topography of Poly(ε-caprolactone) Nanofibers
ACS Biomaterials Science & Engineering ( IF 5.4 ) Pub Date : 2021-09-20 , DOI: 10.1021/acsbiomaterials.1c00951 Yang Zhang 1 , Xiaofeng Wang 1 , Yan Zhang 1 , Yajing Liu 1 , Dongfang Wang 1 , Xueke Yu 2 , Haonan Wang 1 , Zhiyuan Bai 1 , Yong-Chao Jiang 2 , Xiaomeng Li 1 , Wei Zheng 3 , Qian Li 1
ACS Biomaterials Science & Engineering ( IF 5.4 ) Pub Date : 2021-09-20 , DOI: 10.1021/acsbiomaterials.1c00951 Yang Zhang 1 , Xiaofeng Wang 1 , Yan Zhang 1 , Yajing Liu 1 , Dongfang Wang 1 , Xueke Yu 2 , Haonan Wang 1 , Zhiyuan Bai 1 , Yong-Chao Jiang 2 , Xiaomeng Li 1 , Wei Zheng 3 , Qian Li 1
Affiliation
|
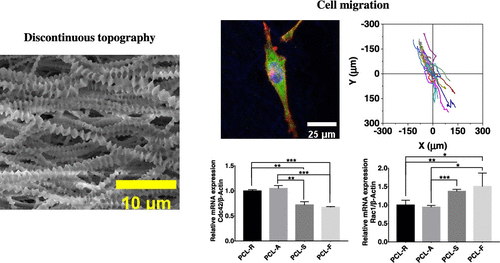
The study of cell migration on biomaterials is of great significance in tissue engineering and regenerative medicine. In recent years, there has been increasing evidence that the physical properties of the extracellular matrix (ECM), such as surface topography, affect various cellular behaviors such as proliferation, adhesion, and migration. However, the biological mechanism of surface topography influencing cellular behavior is still unclear. In this study, we prepared polycaprolactone (PCL) fibrous materials with different surface microstructures by solvent casting, electrospinning, and self-induced crystallization. The corresponding topographical structure obtained is a two-dimensional (2D) flat surface, 2.5-dimensional (2.5D) fibers, and three-dimensional (3D) fibers with a multilevel microstructure. We then investigated the effects of the complex topographical structure on endothelial cell migration. Our study demonstrates that cells can sense the changes of micro- and nanomorphology on the surface of materials, adapt to the physical environment through biochemical reactions, and regulate actin polymerization and directional migration through Rac1 and Cdc42. The cells on the nanofibers are elongated spindles, and the positive feedback of cell adhesion and actin polymerization along the fiber direction makes the plasma membrane continue to protrude, promoting cell polarization and directional migration. This study might provide new insights into the biomaterial design, especially those used for artificial vascular grafts.
中文翻译:

聚(ε-己内酯)纳米纤维表面形貌调控内皮细胞迁移
细胞在生物材料上的迁移研究在组织工程和再生医学中具有重要意义。近年来,越来越多的证据表明细胞外基质 (ECM) 的物理特性,如表面形貌,会影响各种细胞行为,如增殖、粘附和迁移。然而,表面形貌影响细胞行为的生物学机制仍不清楚。在这项研究中,我们通过溶剂浇铸、静电纺丝和自诱导结晶制备了具有不同表面微观结构的聚己内酯 (PCL) 纤维材料。获得的相应地形结构是二维 (2D) 平面、2.5 维 (2.5D) 纤维和具有多级微结构的三维 (3D) 纤维。然后我们研究了复杂的地形结构对内皮细胞迁移的影响。我们的研究表明,细胞可以感知材料表面微观和纳米形态的变化,通过生化反应适应物理环境,并通过 Rac1 和 Cdc42 调节肌动蛋白聚合和定向迁移。纳米纤维上的细胞为拉长的纺锤体,沿纤维方向的细胞粘附和肌动蛋白聚合的正反馈使质膜不断突出,促进细胞极化和定向迁移。这项研究可能会为生物材料设计提供新的见解,尤其是那些用于人工血管移植的材料。我们的研究表明,细胞可以感知材料表面微观和纳米形态的变化,通过生化反应适应物理环境,并通过 Rac1 和 Cdc42 调节肌动蛋白聚合和定向迁移。纳米纤维上的细胞为拉长的纺锤体,沿纤维方向的细胞粘附和肌动蛋白聚合的正反馈使质膜不断突出,促进细胞极化和定向迁移。这项研究可能会为生物材料设计提供新的见解,尤其是那些用于人工血管移植的材料。我们的研究表明,细胞可以感知材料表面微观和纳米形态的变化,通过生化反应适应物理环境,并通过 Rac1 和 Cdc42 调节肌动蛋白聚合和定向迁移。纳米纤维上的细胞为拉长的纺锤体,沿纤维方向的细胞粘附和肌动蛋白聚合的正反馈使质膜不断突出,促进细胞极化和定向迁移。这项研究可能会为生物材料设计提供新的见解,尤其是那些用于人工血管移植的材料。纳米纤维上的细胞为拉长的纺锤体,沿纤维方向的细胞粘附和肌动蛋白聚合的正反馈使质膜不断突出,促进细胞极化和定向迁移。这项研究可能会为生物材料设计提供新的见解,尤其是那些用于人工血管移植的材料。纳米纤维上的细胞为拉长的纺锤体,沿纤维方向的细胞粘附和肌动蛋白聚合的正反馈使质膜不断突出,促进细胞极化和定向迁移。这项研究可能会为生物材料设计提供新的见解,尤其是那些用于人工血管移植的材料。
更新日期:2021-10-12
中文翻译:

聚(ε-己内酯)纳米纤维表面形貌调控内皮细胞迁移
细胞在生物材料上的迁移研究在组织工程和再生医学中具有重要意义。近年来,越来越多的证据表明细胞外基质 (ECM) 的物理特性,如表面形貌,会影响各种细胞行为,如增殖、粘附和迁移。然而,表面形貌影响细胞行为的生物学机制仍不清楚。在这项研究中,我们通过溶剂浇铸、静电纺丝和自诱导结晶制备了具有不同表面微观结构的聚己内酯 (PCL) 纤维材料。获得的相应地形结构是二维 (2D) 平面、2.5 维 (2.5D) 纤维和具有多级微结构的三维 (3D) 纤维。然后我们研究了复杂的地形结构对内皮细胞迁移的影响。我们的研究表明,细胞可以感知材料表面微观和纳米形态的变化,通过生化反应适应物理环境,并通过 Rac1 和 Cdc42 调节肌动蛋白聚合和定向迁移。纳米纤维上的细胞为拉长的纺锤体,沿纤维方向的细胞粘附和肌动蛋白聚合的正反馈使质膜不断突出,促进细胞极化和定向迁移。这项研究可能会为生物材料设计提供新的见解,尤其是那些用于人工血管移植的材料。我们的研究表明,细胞可以感知材料表面微观和纳米形态的变化,通过生化反应适应物理环境,并通过 Rac1 和 Cdc42 调节肌动蛋白聚合和定向迁移。纳米纤维上的细胞为拉长的纺锤体,沿纤维方向的细胞粘附和肌动蛋白聚合的正反馈使质膜不断突出,促进细胞极化和定向迁移。这项研究可能会为生物材料设计提供新的见解,尤其是那些用于人工血管移植的材料。我们的研究表明,细胞可以感知材料表面微观和纳米形态的变化,通过生化反应适应物理环境,并通过 Rac1 和 Cdc42 调节肌动蛋白聚合和定向迁移。纳米纤维上的细胞为拉长的纺锤体,沿纤维方向的细胞粘附和肌动蛋白聚合的正反馈使质膜不断突出,促进细胞极化和定向迁移。这项研究可能会为生物材料设计提供新的见解,尤其是那些用于人工血管移植的材料。纳米纤维上的细胞为拉长的纺锤体,沿纤维方向的细胞粘附和肌动蛋白聚合的正反馈使质膜不断突出,促进细胞极化和定向迁移。这项研究可能会为生物材料设计提供新的见解,尤其是那些用于人工血管移植的材料。纳米纤维上的细胞为拉长的纺锤体,沿纤维方向的细胞粘附和肌动蛋白聚合的正反馈使质膜不断突出,促进细胞极化和定向迁移。这项研究可能会为生物材料设计提供新的见解,尤其是那些用于人工血管移植的材料。











































 京公网安备 11010802027423号
京公网安备 11010802027423号