Nitric Oxide ( IF 3.2 ) Pub Date : 2021-04-20 , DOI: 10.1016/j.niox.2021.04.004 Kefa Li 1 , Tingting You 1 , Panqi Zhao 1 , Yanhong Luo 1 , Danting Zhang 1 , Huan Wei 1 , Yuhui Wang 1 , Jinjin Yang 1 , Xueyan Guan 1 , Zhihe Kuang 1
|
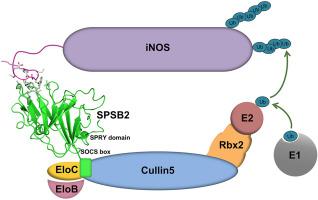
Relatively high concentration of nitric oxide (NO) produced by inducible nitric oxide synthase (iNOS) in response to a variety of stimuli is a source of reactive nitrogen species, an important weapon of host innate immune defense. The SPRY domain-containing SOCS box protein 2 (SPSB2) is an E3 ubiquitin ligase that regulates the lifetime of iNOS. SPSB2 interacts with the N-terminal region of iNOS via a binding site on the SPRY domain of SPSB2, and recruits an E3 ubiquitin ligase complex to polyubiquitinate iNOS, leading to its proteasomal degradation. Although critical residues for the SPSB2-iNOS interaction have been identified, structural basis for the interaction remains to be explicitly determined. In this study, we have determined a crystal structure of the N-terminal region of iNOS in complex with the SPRY domain of SPSB2 at 1.24 Å resolution. We have resolved the roles of some flanking residues, whose contribution to the SPSB2-iNOS interaction was structurally unclear previously. Furthermore, we have evaluated the effects of SPSB2 inhibitors on NO production using transient transfection and cell-penetrating peptide approaches, and found that such inhibitors can elevate NO production in RAW264.7 macrophages. These results thus provide a useful basis for the development of potent SPSB2 inhibitors as well as recruiting ligands for proteolysis targeting chimera (PROTAC) design.
中文翻译:

含 SPRY 结构域的 SOCS 盒蛋白 SPSB2 调节诱导型一氧化氮合酶的结构基础,一种 E3 泛素连接酶
诱导型一氧化氮合酶 (iNOS) 响应各种刺激而产生的相对高浓度的一氧化氮 (NO) 是活性氮的来源,是宿主先天免疫防御的重要武器。含有 SPRY 结构域的 SOCS 盒蛋白 2 (SPSB2) 是一种 E3 泛素连接酶,可调节 iNOS 的寿命。SPSB2 通过 SPSB2 的 SPRY 结构域上的结合位点与 iNOS 的 N 末端区域相互作用,并募集 E3 泛素连接酶复合物以多泛素化 iNOS,导致其蛋白酶体降解。尽管已经确定了 SPSB2-iNOS 相互作用的关键残基,但相互作用的结构基础仍有待明确确定。在这项研究中,我们以 1.24 Å 的分辨率确定了 iNOS 的 N 端区域与 SPSB2 的 SPRY 结构域复合的晶体结构。我们已经解决了一些侧翼残基的作用,它们对 SPSB2-iNOS 相互作用的贡献以前在结构上尚不清楚。此外,我们使用瞬时转染和细胞穿透肽方法评估了 SPSB2 抑制剂对 NO 产生的影响,发现此类抑制剂可以提高 RAW264.7 巨噬细胞中 NO 的产生。因此,这些结果为开发有效的 SPSB2 抑制剂以及为蛋白水解靶向嵌合体 (PROTAC) 设计招募配体提供了有用的基础。并发现此类抑制剂可以提高 RAW264.7 巨噬细胞中 NO 的产生。因此,这些结果为开发有效的 SPSB2 抑制剂以及为蛋白水解靶向嵌合体 (PROTAC) 设计招募配体提供了有用的基础。并发现此类抑制剂可以提高 RAW264.7 巨噬细胞中 NO 的产生。因此,这些结果为开发有效的 SPSB2 抑制剂以及为蛋白水解靶向嵌合体 (PROTAC) 设计招募配体提供了有用的基础。











































 京公网安备 11010802027423号
京公网安备 11010802027423号