Acta Biomaterialia ( IF 9.4 ) Pub Date : 2020-09-13 , DOI: 10.1016/j.actbio.2020.09.021 Sophie Le Cann 1 , Elin Törnquist 2 , Isabella Silva Barreto 2 , Manon Fraulob 1 , Hugues Albini Lomami 1 , Mariana Verezhak 3 , Manuel Guizar-Sicairos 3 , Hanna Isaksson 2 , Guillaume Haïat 1
|
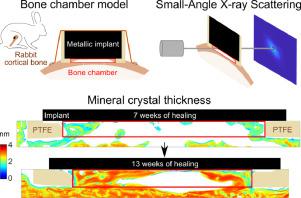
A better understanding of bone nanostructure around the bone-implant interface is essential to improve longevity of clinical implants and decrease failure risks. This study investigates the spatio-temporal evolution of mineral crystal thickness and plate orientation in newly formed bone around the surface of a metallic implant. Standardized coin-shaped titanium implants designed with a bone chamber were inserted into rabbit tibiae for 7 and 13 weeks. Scanning measurements with micro-focused small-angle X-ray scattering (SAXS) were carried out on newly formed bone close to the implant and in control mature cortical bone. Mineral crystals were thinner close to the implant (1.8 ± 0.45 nm at 7 weeks and 2.4 ± 0.57 nm at 13 weeks) than in the control mature bone tissue (2.5 ± 0.21 nm at 7 weeks and 2.8 ± 0.35 nm at 13 weeks), with increasing thickness over healing time (+30 % in 6 weeks). These results are explained by younger bone close to the implant, which matures during osseointegration. Thinner mineral crystals parallel to the implant surface within the first 100 µm indicate that the implant affects the ultrastructure of neighbouring bone , potentially due to heterogeneous interfacial stresses, and suggest a longer maturation process of bone tissue and difficulty in binding to the metal. The bone growth kinetics within the bone chamber was derived from the spatio-temporal evolution of bone tissue's nanostructure, coupled with microtomographic imaging. The findings indicate that understanding mineral crystal thickness or plate orientation can improve our knowledge of osseointegration.
中文翻译:

骨-植入物界面处羟基磷灰石晶体厚度的时空演化。
更好地了解骨-植入物界面周围的骨纳米结构对于提高临床植入物的寿命并降低失败风险至关重要。这项研究调查了金属植入物表面周围新形成的骨骼中矿物晶体厚度和板取向的时空演化。将设计有骨腔的标准硬币形钛植入物插入兔胫骨中7到13周。使用微聚焦小角X射线散射(SAXS)扫描测量是在靠近植入物的新形成的骨上以及在对照成熟的皮质骨上进行的。靠近植入物的矿物晶体(在第7周为1.8±0.45 nm,在第13周为2.4±0.57 nm)比在对照成熟骨组织中(在第7周为2.5±0.21 nm和在第13周为2.8±0.35 nm)更薄,随着愈合时间厚度的增加(6周内增加30%)。这些结果可以通过靠近植入物的年轻骨骼来解释,该骨骼在骨整合过程中会成熟。在最初的100 µm内与植入物表面平行的较薄的矿物晶体表明,植入物可能影响相邻骨骼的超微结构,这可能是由于界面应力不均匀所致,并且提示骨骼组织的成熟过程更长,并且难以与金属结合。骨腔内的骨生长动力学源自骨组织纳米结构的时空演变以及显微断层成像。研究结果表明,了解矿物晶体的厚度或板的取向可以提高我们的骨整合知识。这些结果可以通过靠近植入物的年轻骨骼来解释,该骨骼在骨整合过程中会成熟。在最初的100 µm内与植入物表面平行的较薄的矿物晶体表明,植入物可能影响相邻骨骼的超微结构,这可能是由于界面应力不均匀所致,并且提示骨骼组织的成熟过程更长,并且难以与金属结合。骨腔内的骨生长动力学源自骨组织纳米结构的时空演化以及显微断层成像。研究结果表明,了解矿物晶体的厚度或板的取向可以提高我们的骨整合知识。这些结果可以通过靠近植入物的年轻骨骼来解释,该骨骼在骨整合过程中会成熟。在最初的100 µm内与植入物表面平行的较薄的矿物晶体表明,植入物可能影响相邻骨骼的超微结构,这可能是由于界面应力不均匀所致,并且提示骨骼组织的成熟过程更长,并且难以与金属结合。骨腔内的骨生长动力学源自骨组织纳米结构的时空演化以及显微断层成像。研究结果表明,了解矿物晶体的厚度或板的取向可以提高我们的骨整合知识。在最初的100 µm内与植入物表面平行的较薄的矿物晶体表明,植入物可能影响相邻骨骼的超微结构,这可能是由于界面应力不均匀所致,并且提示骨骼组织的成熟过程更长,并且难以与金属结合。骨腔内的骨生长动力学源自骨组织纳米结构的时空演化以及显微断层成像。研究结果表明,了解矿物晶体的厚度或板的取向可以提高我们的骨整合知识。在最初的100 µm内与植入物表面平行的较薄的矿物晶体表明,植入物可能影响相邻骨骼的超微结构,这可能是由于界面应力不均匀所致,并且提示骨骼组织的成熟过程更长,并且难以与金属结合。骨腔内的骨生长动力学源自骨组织纳米结构的时空演化以及显微断层成像。研究结果表明,了解矿物晶体的厚度或板的取向可以提高我们的骨整合知识。骨腔内的骨生长动力学源自骨组织纳米结构的时空演化以及显微断层成像。研究结果表明,了解矿物晶体的厚度或板的取向可以提高我们的骨整合知识。骨腔内的骨生长动力学源自骨组织纳米结构的时空演化以及显微断层成像。研究结果表明,了解矿物晶体的厚度或板的取向可以提高我们的骨整合知识。











































 京公网安备 11010802027423号
京公网安备 11010802027423号