当前位置:
X-MOL 学术
›
Chem. Biodivers.
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
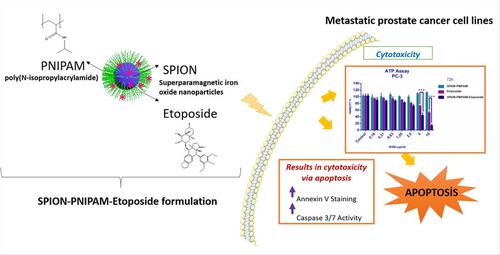
Etoposide Loaded SPION‐PNIPAM Nanoparticles Improve the in vitro Therapeutic Outcome on Metastatic Prostate Cancer Cells via Enhanced Apoptosis
Chemistry & Biodiversity ( IF 2.3 ) Pub Date : 2020-10-15 , DOI: 10.1002/cbdv.202000607 Merve Erkisa 1, 2 , Ferda Ari 1 , Irem Ulku 3 , Rouhollah Khodadust 3 , Yasemin Yar 4 , Havva Yagci Acar 3, 4 , Engin Ulukaya 5
Chemistry & Biodiversity ( IF 2.3 ) Pub Date : 2020-10-15 , DOI: 10.1002/cbdv.202000607 Merve Erkisa 1, 2 , Ferda Ari 1 , Irem Ulku 3 , Rouhollah Khodadust 3 , Yasemin Yar 4 , Havva Yagci Acar 3, 4 , Engin Ulukaya 5
Affiliation
|
Prostate cancer is among the leading causes of death worldwide because its metastatic form is a deadly disease. Therefore, the development of new chemotherapeutics is of immense importance. Nanoparticle technology seems to provide diverse options in this regard. Therefore, poly(N‐isopropylacrylamide) (PNIPAM) coated superparamagnetic iron oxide nanoparticles (SPION) loaded with Etoposide were prepared in small sizes (57 nm) and with 3.5 % drug content to improve the efficiency of Etoposide in prostate cancer therapy. Sustained release of the drug was achieved, which found to be sensitive to low pH and high temperature. The anti‐growth activity of SPION‐PNIPAM‐Etoposide formulation against metastatic prostate cancer cells (PC‐3, LNCaP) were investigated by SRB assay, then, confirmed by ATP assay. Mode of cell death was evaluated by using flow cytometry analyses. A significant improvement of nanoformulated drug was observed at 5–10 μg/ml doses of the drug in both cell lines. More importantly, this formulation enhanced the cytotoxic effect of Etoposide on PC‐3 cells, which is considered more resistant to Etoposide than LNCaP and reduced the IC50 value by 55 % reaching to 4.5 μg drug/ml, which is a very significant improvement in the literature. It was clearly shown that nanoformulated drug provided about 3‐fold increases in caspase‐dependent early apoptotic cells in PC‐3 cells. The novel formulation seems to successfully cause cell death of especially PC‐3 metastatic prostate cancer cells. It should therefore be taken into consideration for further animal studies as a novel potent anticancer agent.
中文翻译:

负载依托泊苷的 SPION-PNIPAM 纳米颗粒通过增强细胞凋亡改善转移性前列腺癌细胞的体外治疗结果
前列腺癌是全球主要的死亡原因之一,因为它的转移形式是一种致命的疾病。因此,开发新的化疗药物具有十分重要的意义。纳米粒子技术似乎在这方面提供了多种选择。因此,聚(N-异丙基丙烯酰胺)(PNIPAM)包被的超顺磁性氧化铁纳米粒子(SPION)被制备成小尺寸(57 nm)和3.5%的药物含量,以提高依托泊苷在前列腺癌治疗中的效率。实现了药物的持续释放,发现它对低 pH 值和高温敏感。通过 SRB 测定研究 SPION-PNIPAM-依托泊苷制剂对转移性前列腺癌细胞 (PC-3, LNCaP) 的抗生长活性,然后通过 ATP 测定证实。通过使用流式细胞术分析评估细胞死亡的方式。在两种细胞系中观察到纳米制剂药物在 5-10 μg/ml 剂量下的显着改善。更重要的是,该制剂增强了依托泊苷对 PC-3 细胞的细胞毒作用,PC-3 细胞被认为比 LNCaP 对依托泊苷具有更强的抗药性,并使 IC50 值降低 55%,达到 4.5 μg 药物/ml,这是一个非常显着的改善。文学。清楚地表明,纳米制剂药物使 PC-3 细胞中半胱天冬酶依赖性早期凋亡细胞增加了约 3 倍。这种新配方似乎成功地导致了 PC-3 转移性前列腺癌细胞的细胞死亡。因此,在进一步的动物研究中应考虑将其作为一种新型强效抗癌剂。在两种细胞系中观察到纳米制剂药物在 5-10 μg/ml 剂量下的显着改善。更重要的是,该制剂增强了依托泊苷对 PC-3 细胞的细胞毒作用,PC-3 细胞被认为比 LNCaP 对依托泊苷具有更强的抗药性,并使 IC50 值降低 55%,达到 4.5 μg 药物/ml,这是一个非常显着的改善。文学。清楚地表明,纳米制剂药物使 PC-3 细胞中半胱天冬酶依赖性早期凋亡细胞增加了约 3 倍。这种新配方似乎成功地导致了 PC-3 转移性前列腺癌细胞的细胞死亡。因此,在进一步的动物研究中应考虑将其作为一种新型强效抗癌剂。在两种细胞系中观察到纳米制剂药物在 5-10 μg/ml 剂量下的显着改善。更重要的是,该制剂增强了依托泊苷对 PC-3 细胞的细胞毒作用,PC-3 细胞被认为比 LNCaP 对依托泊苷具有更强的抗药性,并使 IC50 值降低 55%,达到 4.5 μg 药物/ml,这是一个非常显着的改善。文学。清楚地表明,纳米制剂药物使 PC-3 细胞中半胱天冬酶依赖性早期凋亡细胞增加了约 3 倍。这种新配方似乎成功地导致了 PC-3 转移性前列腺癌细胞的细胞死亡。因此,在进一步的动物研究中应考虑将其作为一种新型强效抗癌剂。该制剂增强了依托泊苷对 PC-3 细胞的细胞毒作用,PC-3 细胞被认为比 LNCaP 对依托泊苷具有更强的抗性,并将 IC50 值降低 55%,达到 4.5 μg 药物/毫升,这是文献中非常显着的改进。清楚地表明,纳米制剂药物使 PC-3 细胞中半胱天冬酶依赖性早期凋亡细胞增加了约 3 倍。这种新配方似乎成功地导致了 PC-3 转移性前列腺癌细胞的细胞死亡。因此,在进一步的动物研究中应考虑将其作为一种新型强效抗癌剂。该制剂增强了依托泊苷对 PC-3 细胞的细胞毒作用,PC-3 细胞被认为比 LNCaP 对依托泊苷具有更强的抗性,并将 IC50 值降低 55%,达到 4.5 μg 药物/毫升,这是文献中非常显着的改进。清楚地表明,纳米制剂药物使 PC-3 细胞中半胱天冬酶依赖性早期凋亡细胞增加了约 3 倍。这种新配方似乎成功地导致了 PC-3 转移性前列腺癌细胞的细胞死亡。因此,在进一步的动物研究中应考虑将其作为一种新型强效抗癌剂。这是文献中非常显着的改进。清楚地表明,纳米制剂药物使 PC-3 细胞中半胱天冬酶依赖性早期凋亡细胞增加了约 3 倍。这种新配方似乎成功地导致了 PC-3 转移性前列腺癌细胞的细胞死亡。因此,在进一步的动物研究中应考虑将其作为一种新型强效抗癌剂。这是文献中非常显着的改进。清楚地表明,纳米制剂药物使 PC-3 细胞中半胱天冬酶依赖性早期凋亡细胞增加了约 3 倍。这种新配方似乎成功地导致了 PC-3 转移性前列腺癌细胞的细胞死亡。因此,在进一步的动物研究中应考虑将其作为一种新型强效抗癌剂。
更新日期:2020-10-15
中文翻译:

负载依托泊苷的 SPION-PNIPAM 纳米颗粒通过增强细胞凋亡改善转移性前列腺癌细胞的体外治疗结果
前列腺癌是全球主要的死亡原因之一,因为它的转移形式是一种致命的疾病。因此,开发新的化疗药物具有十分重要的意义。纳米粒子技术似乎在这方面提供了多种选择。因此,聚(N-异丙基丙烯酰胺)(PNIPAM)包被的超顺磁性氧化铁纳米粒子(SPION)被制备成小尺寸(57 nm)和3.5%的药物含量,以提高依托泊苷在前列腺癌治疗中的效率。实现了药物的持续释放,发现它对低 pH 值和高温敏感。通过 SRB 测定研究 SPION-PNIPAM-依托泊苷制剂对转移性前列腺癌细胞 (PC-3, LNCaP) 的抗生长活性,然后通过 ATP 测定证实。通过使用流式细胞术分析评估细胞死亡的方式。在两种细胞系中观察到纳米制剂药物在 5-10 μg/ml 剂量下的显着改善。更重要的是,该制剂增强了依托泊苷对 PC-3 细胞的细胞毒作用,PC-3 细胞被认为比 LNCaP 对依托泊苷具有更强的抗药性,并使 IC50 值降低 55%,达到 4.5 μg 药物/ml,这是一个非常显着的改善。文学。清楚地表明,纳米制剂药物使 PC-3 细胞中半胱天冬酶依赖性早期凋亡细胞增加了约 3 倍。这种新配方似乎成功地导致了 PC-3 转移性前列腺癌细胞的细胞死亡。因此,在进一步的动物研究中应考虑将其作为一种新型强效抗癌剂。在两种细胞系中观察到纳米制剂药物在 5-10 μg/ml 剂量下的显着改善。更重要的是,该制剂增强了依托泊苷对 PC-3 细胞的细胞毒作用,PC-3 细胞被认为比 LNCaP 对依托泊苷具有更强的抗药性,并使 IC50 值降低 55%,达到 4.5 μg 药物/ml,这是一个非常显着的改善。文学。清楚地表明,纳米制剂药物使 PC-3 细胞中半胱天冬酶依赖性早期凋亡细胞增加了约 3 倍。这种新配方似乎成功地导致了 PC-3 转移性前列腺癌细胞的细胞死亡。因此,在进一步的动物研究中应考虑将其作为一种新型强效抗癌剂。在两种细胞系中观察到纳米制剂药物在 5-10 μg/ml 剂量下的显着改善。更重要的是,该制剂增强了依托泊苷对 PC-3 细胞的细胞毒作用,PC-3 细胞被认为比 LNCaP 对依托泊苷具有更强的抗药性,并使 IC50 值降低 55%,达到 4.5 μg 药物/ml,这是一个非常显着的改善。文学。清楚地表明,纳米制剂药物使 PC-3 细胞中半胱天冬酶依赖性早期凋亡细胞增加了约 3 倍。这种新配方似乎成功地导致了 PC-3 转移性前列腺癌细胞的细胞死亡。因此,在进一步的动物研究中应考虑将其作为一种新型强效抗癌剂。该制剂增强了依托泊苷对 PC-3 细胞的细胞毒作用,PC-3 细胞被认为比 LNCaP 对依托泊苷具有更强的抗性,并将 IC50 值降低 55%,达到 4.5 μg 药物/毫升,这是文献中非常显着的改进。清楚地表明,纳米制剂药物使 PC-3 细胞中半胱天冬酶依赖性早期凋亡细胞增加了约 3 倍。这种新配方似乎成功地导致了 PC-3 转移性前列腺癌细胞的细胞死亡。因此,在进一步的动物研究中应考虑将其作为一种新型强效抗癌剂。该制剂增强了依托泊苷对 PC-3 细胞的细胞毒作用,PC-3 细胞被认为比 LNCaP 对依托泊苷具有更强的抗性,并将 IC50 值降低 55%,达到 4.5 μg 药物/毫升,这是文献中非常显着的改进。清楚地表明,纳米制剂药物使 PC-3 细胞中半胱天冬酶依赖性早期凋亡细胞增加了约 3 倍。这种新配方似乎成功地导致了 PC-3 转移性前列腺癌细胞的细胞死亡。因此,在进一步的动物研究中应考虑将其作为一种新型强效抗癌剂。这是文献中非常显着的改进。清楚地表明,纳米制剂药物使 PC-3 细胞中半胱天冬酶依赖性早期凋亡细胞增加了约 3 倍。这种新配方似乎成功地导致了 PC-3 转移性前列腺癌细胞的细胞死亡。因此,在进一步的动物研究中应考虑将其作为一种新型强效抗癌剂。这是文献中非常显着的改进。清楚地表明,纳米制剂药物使 PC-3 细胞中半胱天冬酶依赖性早期凋亡细胞增加了约 3 倍。这种新配方似乎成功地导致了 PC-3 转移性前列腺癌细胞的细胞死亡。因此,在进一步的动物研究中应考虑将其作为一种新型强效抗癌剂。











































 京公网安备 11010802027423号
京公网安备 11010802027423号