当前位置:
X-MOL 学术
›
FEBS Open Bio
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
MiR-642a-5p partially mediates the effects of lipopolysaccharide on human pulmonary microvascular endothelial cells via eEF2.
FEBS Open Bio ( IF 2.8 ) Pub Date : 2020-09-03 , DOI: 10.1002/2211-5463.12969 Liming Fei 1 , Gengyun Sun 1 , Qinghai You 1
FEBS Open Bio ( IF 2.8 ) Pub Date : 2020-09-03 , DOI: 10.1002/2211-5463.12969 Liming Fei 1 , Gengyun Sun 1 , Qinghai You 1
Affiliation
|
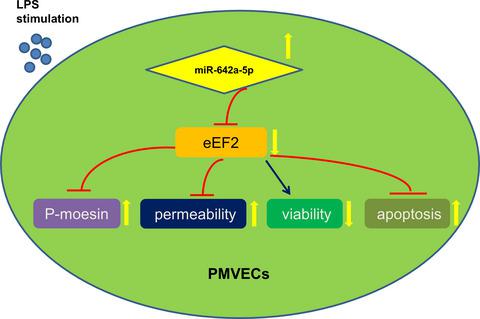
Inhalation or systemic administration of lipopolysaccharide (LPS) can induce acute pulmonary inflammation and lung injury. The pulmonary vasculature is composed of pulmonary microvascular endothelial cells (PMVECs), which form a semiselective membrane for gas exchange. The miRNA miR‐642a‐5p has previously been reported to be up‐regulated in patients with acute respiratory distress syndrome; thus, here, we examined whether this miRNA is involved in the effects of LPS on PMVECs. The levels of miR‐642a‐5p and mRNA encoding eukaryotic elongation factor 2 (eEF2) were detected by quantitative RT‐PCR. Moesin and eEF2 protein levels were tested by western blot assay. Dual‐luciferase reporter assay was used to examine the relationship between miR‐642a‐5p and eEF2. Cell viability was assessed using the 3‐(4,5‐dimethylthiazol‐2‐yl)‐2,5‐diphenyltetrazolium bromide assay, and cell permeability was analyzed using the transendothelial electrical resistance assay. We report that miR‐642a‐5p levels are significantly up‐regulated in LPS‐stimulated PMVECs, and miR‐642a‐5p contributes to LPS‐induced hyperpermeability and apoptosis of PMVECs. LPS treatment results in down‐regulation of eEF2 in PMVECs. Overexpression of eEF2, a direct target of miR‐642a‐5p, inhibited the effect of LPS on PMVECs. miR‐642a‐5p promoted LPS‐induced hyperpermeability and apoptosis by targeting eEF2. Thus, miR‐642a‐5p and eEF2 may serve as potential targets for acute lung injury/acute respiratory distress syndrome diagnosis or treatment.
中文翻译:

MiR-642a-5p 通过 eEF2 部分介导脂多糖对人肺微血管内皮细胞的影响。
吸入或全身给药脂多糖 (LPS) 可诱发急性肺部炎症和肺损伤。肺血管系统由肺微血管内皮细胞 (PMVECs) 组成,它们形成用于气体交换的半选择性膜。先前已报道 miRNA miR-642a-5p 在急性呼吸窘迫综合征患者中上调;因此,在这里,我们检查了这种 miRNA 是否参与 LPS 对 PMVECs 的影响。通过定量 RT-PCR 检测 miR-642a-5p 和编码真核延伸因子 2 (eEF2) 的 mRNA 水平。通过蛋白质印迹法测试 Moesin 和 eEF2 蛋白水平。双荧光素酶报告基因检测用于检测 miR-642a-5p 和 eEF2 之间的关系。使用 3-(4,5-二甲基噻唑-2-基)-2 评估细胞活力,5-二苯基溴化四唑测定,并使用跨内皮电阻测定分析细胞通透性。我们报道了 miR-642a-5p 水平在 LPS 刺激的 PMVECs 中显着上调,并且 miR-642a-5p 有助于 LPS 诱导的 PMVECs 高通透性和凋亡。LPS 处理导致 PMVECs 中 eEF2 的下调。eEF2(miR-642a-5p 的直接靶标)的过表达抑制了 LPS 对 PMVECs 的影响。miR-642a-5p 通过靶向 eEF2 促进 LPS 诱导的高通透性和细胞凋亡。因此,miR-642a-5p 和 eEF2 可作为急性肺损伤/急性呼吸窘迫综合征诊断或治疗的潜在靶点。我们报道了 miR-642a-5p 水平在 LPS 刺激的 PMVECs 中显着上调,并且 miR-642a-5p 有助于 LPS 诱导的 PMVECs 高通透性和凋亡。LPS 处理导致 PMVECs 中 eEF2 的下调。eEF2(miR-642a-5p 的直接靶标)的过表达抑制了 LPS 对 PMVECs 的影响。miR-642a-5p 通过靶向 eEF2 促进 LPS 诱导的高通透性和细胞凋亡。因此,miR-642a-5p 和 eEF2 可作为急性肺损伤/急性呼吸窘迫综合征诊断或治疗的潜在靶点。我们报道了 miR-642a-5p 水平在 LPS 刺激的 PMVECs 中显着上调,并且 miR-642a-5p 有助于 LPS 诱导的 PMVECs 高通透性和凋亡。LPS 处理导致 PMVECs 中 eEF2 的下调。eEF2(miR-642a-5p 的直接靶标)的过表达抑制了 LPS 对 PMVECs 的影响。miR-642a-5p 通过靶向 eEF2 促进 LPS 诱导的高通透性和细胞凋亡。因此,miR-642a-5p 和 eEF2 可作为急性肺损伤/急性呼吸窘迫综合征诊断或治疗的潜在靶点。miR-642a-5p 通过靶向 eEF2 促进 LPS 诱导的高通透性和细胞凋亡。因此,miR-642a-5p 和 eEF2 可作为急性肺损伤/急性呼吸窘迫综合征诊断或治疗的潜在靶点。miR-642a-5p 通过靶向 eEF2 促进 LPS 诱导的高通透性和细胞凋亡。因此,miR-642a-5p 和 eEF2 可作为急性肺损伤/急性呼吸窘迫综合征诊断或治疗的潜在靶点。
更新日期:2020-11-04
中文翻译:

MiR-642a-5p 通过 eEF2 部分介导脂多糖对人肺微血管内皮细胞的影响。
吸入或全身给药脂多糖 (LPS) 可诱发急性肺部炎症和肺损伤。肺血管系统由肺微血管内皮细胞 (PMVECs) 组成,它们形成用于气体交换的半选择性膜。先前已报道 miRNA miR-642a-5p 在急性呼吸窘迫综合征患者中上调;因此,在这里,我们检查了这种 miRNA 是否参与 LPS 对 PMVECs 的影响。通过定量 RT-PCR 检测 miR-642a-5p 和编码真核延伸因子 2 (eEF2) 的 mRNA 水平。通过蛋白质印迹法测试 Moesin 和 eEF2 蛋白水平。双荧光素酶报告基因检测用于检测 miR-642a-5p 和 eEF2 之间的关系。使用 3-(4,5-二甲基噻唑-2-基)-2 评估细胞活力,5-二苯基溴化四唑测定,并使用跨内皮电阻测定分析细胞通透性。我们报道了 miR-642a-5p 水平在 LPS 刺激的 PMVECs 中显着上调,并且 miR-642a-5p 有助于 LPS 诱导的 PMVECs 高通透性和凋亡。LPS 处理导致 PMVECs 中 eEF2 的下调。eEF2(miR-642a-5p 的直接靶标)的过表达抑制了 LPS 对 PMVECs 的影响。miR-642a-5p 通过靶向 eEF2 促进 LPS 诱导的高通透性和细胞凋亡。因此,miR-642a-5p 和 eEF2 可作为急性肺损伤/急性呼吸窘迫综合征诊断或治疗的潜在靶点。我们报道了 miR-642a-5p 水平在 LPS 刺激的 PMVECs 中显着上调,并且 miR-642a-5p 有助于 LPS 诱导的 PMVECs 高通透性和凋亡。LPS 处理导致 PMVECs 中 eEF2 的下调。eEF2(miR-642a-5p 的直接靶标)的过表达抑制了 LPS 对 PMVECs 的影响。miR-642a-5p 通过靶向 eEF2 促进 LPS 诱导的高通透性和细胞凋亡。因此,miR-642a-5p 和 eEF2 可作为急性肺损伤/急性呼吸窘迫综合征诊断或治疗的潜在靶点。我们报道了 miR-642a-5p 水平在 LPS 刺激的 PMVECs 中显着上调,并且 miR-642a-5p 有助于 LPS 诱导的 PMVECs 高通透性和凋亡。LPS 处理导致 PMVECs 中 eEF2 的下调。eEF2(miR-642a-5p 的直接靶标)的过表达抑制了 LPS 对 PMVECs 的影响。miR-642a-5p 通过靶向 eEF2 促进 LPS 诱导的高通透性和细胞凋亡。因此,miR-642a-5p 和 eEF2 可作为急性肺损伤/急性呼吸窘迫综合征诊断或治疗的潜在靶点。miR-642a-5p 通过靶向 eEF2 促进 LPS 诱导的高通透性和细胞凋亡。因此,miR-642a-5p 和 eEF2 可作为急性肺损伤/急性呼吸窘迫综合征诊断或治疗的潜在靶点。miR-642a-5p 通过靶向 eEF2 促进 LPS 诱导的高通透性和细胞凋亡。因此,miR-642a-5p 和 eEF2 可作为急性肺损伤/急性呼吸窘迫综合征诊断或治疗的潜在靶点。











































 京公网安备 11010802027423号
京公网安备 11010802027423号