Rh催化硫叶立德与(杂)芳香烃C-H键的交叉偶联反应
迄今为止,硫叶立德参与的过渡金属催化反应较为有限,发展尚不完善。目前比较成熟的方法包括Ir催化α-羰基硫叶立德形成C-N和C-C键的反应,该反应可以有效地避免使用安全隐患高的重氮化合物,在药物后期修饰的大规模合成中具有重要的意义,已应用于呼吸系统疾病的候选治疗药物MK-7246的工业化合成中。此外,α-羰基硫叶立德可经由Ir催化剂的作用得到Ir卡宾,与α,β-不饱和β-氨基酯反应得到取代吡咯化合物。
最近,英国利物浦大学的Christophe Aϊssa博士(点击查看介绍)等研究者首次报道了Rh催化α-羰基硫叶立德与芳香烃及杂芳香烃C(sp2)-H键的交叉偶联反应。该反应通过连续的C-H键活化、叶立德迁移插入碳-金属键并发生质子解离得到目标偶联产物,与Ir催化的脱水环化反应结合还可用于合成苯并[c]吖啶,由此开拓了过渡金属催化硫叶立德与亲核性较差的底物发生的反应。相关工作发表在Angew. Chem. Int. Ed. 上。
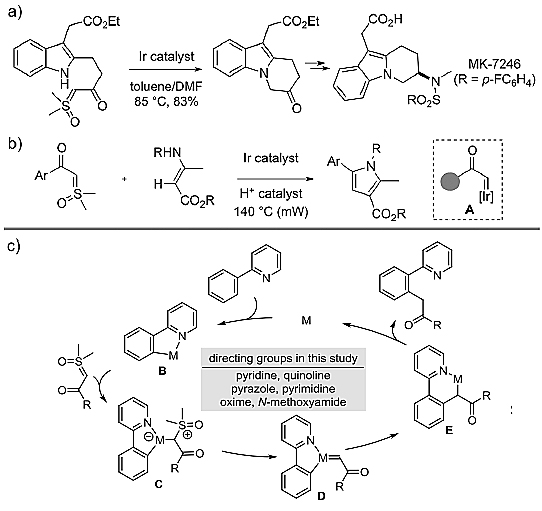
图1. 硫叶立德参与的反应。图片来源:Angew. Chem. Int. Ed.
他们设想通过导向基团引导的金属活化C-H键活化反应可以形成环金属中间体B,B与α-羰基硫叶立德反应,经由中间体C和D得到中间体E,最终质子解离得到产物。如果以上途径能够成功实现,则可以避免Rh催化C-H键的官能化反应中使用重氮化合物以及三氮唑、腙等重氮化合物前体,由此消除反应带来的安全隐患,还可以拓展Rh催化的环化反应以及其他金属卡宾中间体参与的C-H键活化反应的适用范围。

Christophe Aϊssa博士。图片来源:University of Liverpool
中间体B到E的迁移插入过程之前尚无报道。作者首先尝试用已知的Rh中间体1与叶立德2a反应,可以良好的收率得到迁移插入的非对映异构体产物3和4。两种中间体在快速柱层析的过程中会发生互相转化,其比例在2.8:1到5:1之间。3和4在室温条件下较为稳定,并通过X射线单晶衍射确定了环Rh中间体结构。随后他们发现,1,1,1,3,3,3-六氟-2-丙醇(HFIP)可以促进环Rh中间体3和4的原位质子解离,得到最终产物并完成催化剂循环。反应中使用1.7当量的2b可以接近化学计量的收率得到6b,使用2.0当量位阻较大的2a作为底物也可以77%的收率得到产物6a。其他催化剂,如[(Cp*IrCl2)]2、[(Cp*IrI2)]2、[Cp*Ir(CO)I2]、[Ru(p-cymene)Cl2]2等无法催化反应进行。
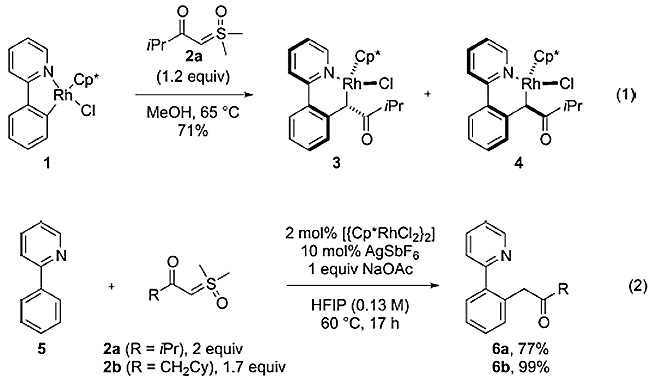
图2. 反应条件的优化。图片来源:Angew. Chem. Int. Ed.
得到最优条件之后,他们对底物的普适性进行了考察。首先对于硫叶立德底物,不同芳香酮叶立德参与反应都具有良好的收率,其中苯环电子云密度高的底物反应更为理想(6c-6f);噻吩、呋喃等芳香杂环修饰的底物也具有很好的底物适用性(6g-6h);环丙烷、Boc保护的哌啶、金刚烷等官能团也可以很好地兼容(6i-6k)。对于含有吡啶导向基的底物,芳香酮对位含有取代基时,反应的收率有所下降(6l-6m);吲哚、吡咯、呋喃、吡啶酮等芳香杂环修饰的底物参与反应也能够得到中等以上的收率(6n-6r)。而将吡啶导向基换为吡唑、嘧啶、甲基肟等官能团时,反应也能够得到中等到良好的收率(6s-6w)。需要特别指出的是,2w使用8 mol%的[Cp*Rh(MeCN)3][SbF6]2作为催化剂时,可以90%的收率得到6w。
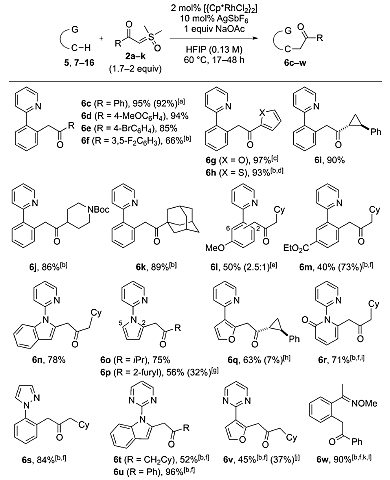
图3. 底物普适性的考察。图片来源:Angew. Chem. Int. Ed.
接下来,他们以底物17为例对硫叶立德的取代基效应进行研究,体系加热至90 ℃反应48 h,仅得到50%的中等NMR收率,作者分析可能是因为位阻效应导致反应的产率降低。
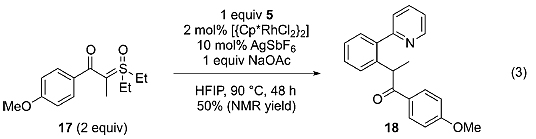
图4. 硫叶立德取代基效应的研究。图片来源:Angew. Chem. Int. Ed.
作者还对产物进行了衍生化,得到一系列有应用价值的杂环类化合物。底物19与2b反应可以进一步环化得到N-甲氧基取代的内酰胺。产物6u的嘧啶取代基在碱性条件下可以消除得到21。含有喹啉导向基团的产物22也可以通过Ir催化的环化芳构化反应得到苯并[c]吖啶化合物。
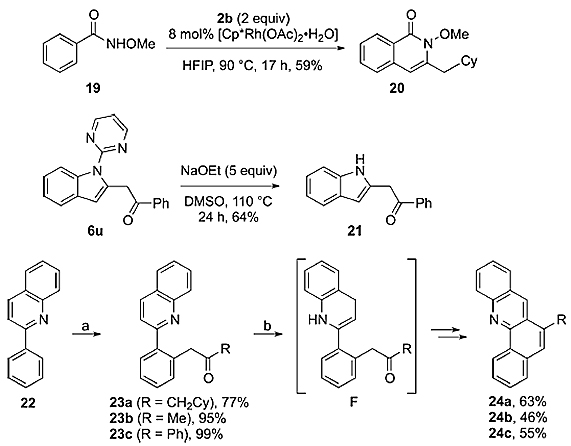
图5. 产物的衍生化。图片来源:Angew. Chem. Int. Ed.
最后,他们对反应机理进行了研究,通过设计同位素氘代实验,以5作为底物,使用1,2-二氯苯与(CF3)2CHOD以1:1混合作为溶剂,可以得到底物C(sp2)-H键发生氘代的产物[Dn]5以及通过烯醇-酮互变异构作用得到的氘代产物[Dn]6b;作者通过进一步的研究发现,C-H键的断裂不仅是可逆的,其速率也快于总反应的速率。他们继续设计了动力学同位素效应实验,反应使用底物5时kH/kD = 2.6;而使用已发生C-H键活化的Rh络合物3时kH/kD = 1.9。此外,5与3的HFIP溶液混合可分别以83%和70%的收率得到6a与1。以上的实验结果与作者提出的反应机理都能够很好地吻合,其中质子解离为决速步骤。
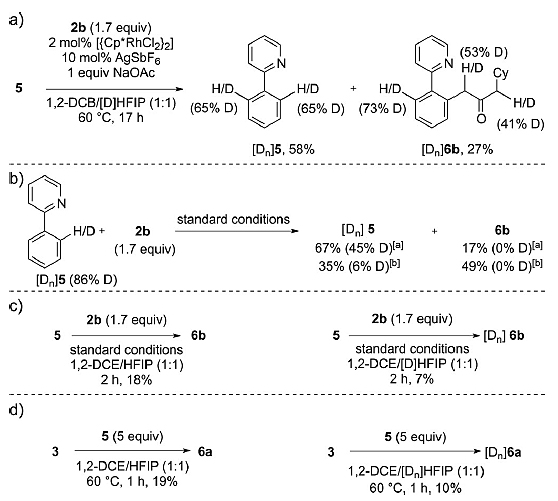
图6. 机理验证实验。图片来源:Angew. Chem. Int. Ed.
——小结——
Christophe Aϊssa教授首次报道了Rh催化硫叶立德与芳香烃及杂芳香烃C-H键的交叉偶联反应,该反应具有良好的底物适用性,有效避免了Rh卡宾参与的反应中需要使用重氮化合物所带来的安全隐患。他们还通过设计同位素实验和控制实验,验证了环Rh中间体与硫叶立德迁移插入的反应机理,由此大大拓展了硫叶立德参与的过渡金属催化反应。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Cross-Coupling of a-Carbonyl Sulfoxonium Ylides with C-H Bonds
Angew. Chem. Int. Ed., 2017, DOI: 10.1002/anie.201706804
导师介绍
Christophe Aϊssa
http://www.x-mol.com/university/faculty/39318
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!



































 京公网安备 11010802027423号
京公网安备 11010802027423号