华中师大徐浩/武汉大学戚孝天JACS:远程手性控制的[4+1]环化反应
末端炔烃作为一种廉价易得且用途多样的化合物,广泛应用于有机合成中,在医药、农药及天然产物的合成中发挥着重要作用。由于末端炔氢具有一定的酸性 (pKa~25),可以与金属形成炔基金属中间体,该活泼中间体能与含有C=O、C=N和C=C双键的亲核试剂发生不对称亲核加成反应或与自由基、金属卡宾物种发生不对称偶联反应(图1a),这些反应模式的反应位点离金属中心相隔一根化学键。
炔丙醇及其衍生物,则能与金属形成亚丙二烯基金属中间体。该类中间体能与多种亲核试剂发生不对称炔丙基取代或环加成反应。反应往往发生在γ位,与金属中心相隔三根化学键。该领域得到了广泛的关注,国内侯雪龙、胡向平、肖文精、龚流柱、游书力、吴小余、张新刚、陆良秋、钮大文、郭昌、郭武生等课题组做出了杰出的贡献。华中师范大学徐浩课题组近年来在该领域也取得了一些进展,实现了催化不对称炔丙基胺化(RSC Adv. 2020, 10, 38478−38483)、烷基化反应(Chin. Chem. Lett. 2022, 33, 867−870)以及催化不对称插烯与双插烯炔丙基取代反应(J. Am. Chem. Soc. 2022, 144, 15779–15785,点击阅读详细)。
当在炔丙醇化合物中引入烯基,则能形成烯基-亚丙二烯基金属中间体。然而,烯基-亚丙二烯基金属中间体介导的不对称反应鲜有报道,主要归因于烯基-亚丙二烯基金属中间体具有多个反应位点,存在多种竞争反应,特别是其ε位离金属中心有五根化学键的距离,该位点的立体选择性控制极具挑战性(图1b)。因此,亟待发展新的方法及策略,实现烯基-亚丙二烯基金属中间体参与的不对称转化反应。Haak课题组利用钌催化剂(Angew. Chem., Int. Ed. 2015, 54, 4097−4101)实现了该中间体参与的环化反应,但是没有实现催化不对称的合成。最近,房新强课题组利用铜催化剂(ACS Catal. 2022, 12, 6840−6850),实现了该中间体参与的烯丙基取代反应及环化反应,初步远程不对称催化的尝试得到了中等ee值的产物。近日,何智涛课题组报道了一例新颖的铜催化的不对称炔烯丙基取代反应(Nat. Synth., 2022, DOI: 10.1038/s44160-022-00176-4,点击阅读详细),实现了其γ位优秀的对映选择性控制。

图1. 金属催化末端炔的不对称转化
为了解决ε位远程手性控制的难题,作者设想采用顺式构象的金属中间体来缩短ε位与金属中心的距离,并利用亲核试剂与铜催化剂阴阳离子对相互作用,可能是解决此问题的关键(图1c)。这样的设计一方面可以减少反应过程中可能的过渡态数量,一方面增强烯基-亚丙二烯基金属中间体ε位的对映选择性控制能力。近日,该课题组通过发展新型炔基烯丙醇酯试剂,采用新型的手性PyBox配体与铜盐作为催化剂(5 mol %),成功实现了烯基-亚丙二烯基铜中间体远程不对称的[4+1]环化反应,该反应是首例铜催化ε位不对称炔基-烯丙基取代反应。相关研究成果发表在J. Am. Chem. Soc.上(图2)。
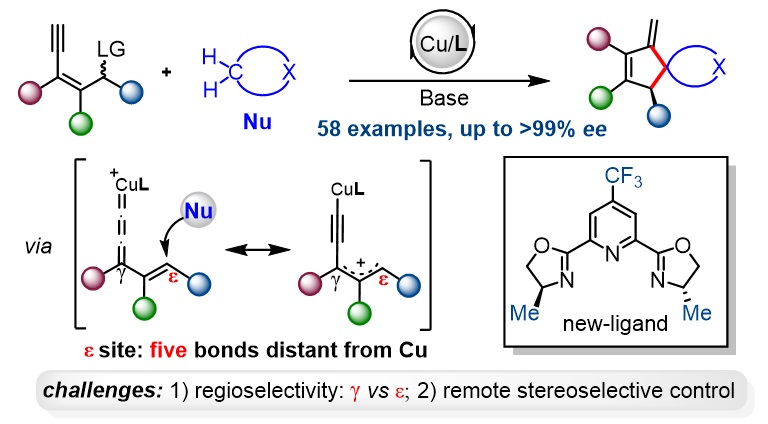
图2. 远程对映选择性的[4+1]环化反应
首先作者以炔基烯丙醇酯1和1,3-环己二酮作为模板底物,对离去基、配体、温度、催化剂当量、底物比例等条件进行了筛选(表1)。实验结果表明,以Cu(CH3CN)4BF4(5 mol%)与CF3-PyBOX配体L11(6 mol%)为催化剂,MeOH作为反应溶剂,DIPEA(1.5 equiv)作为碱,-20 ℃下反应,以99%的产率和96%的ee值得到螺环产物3。
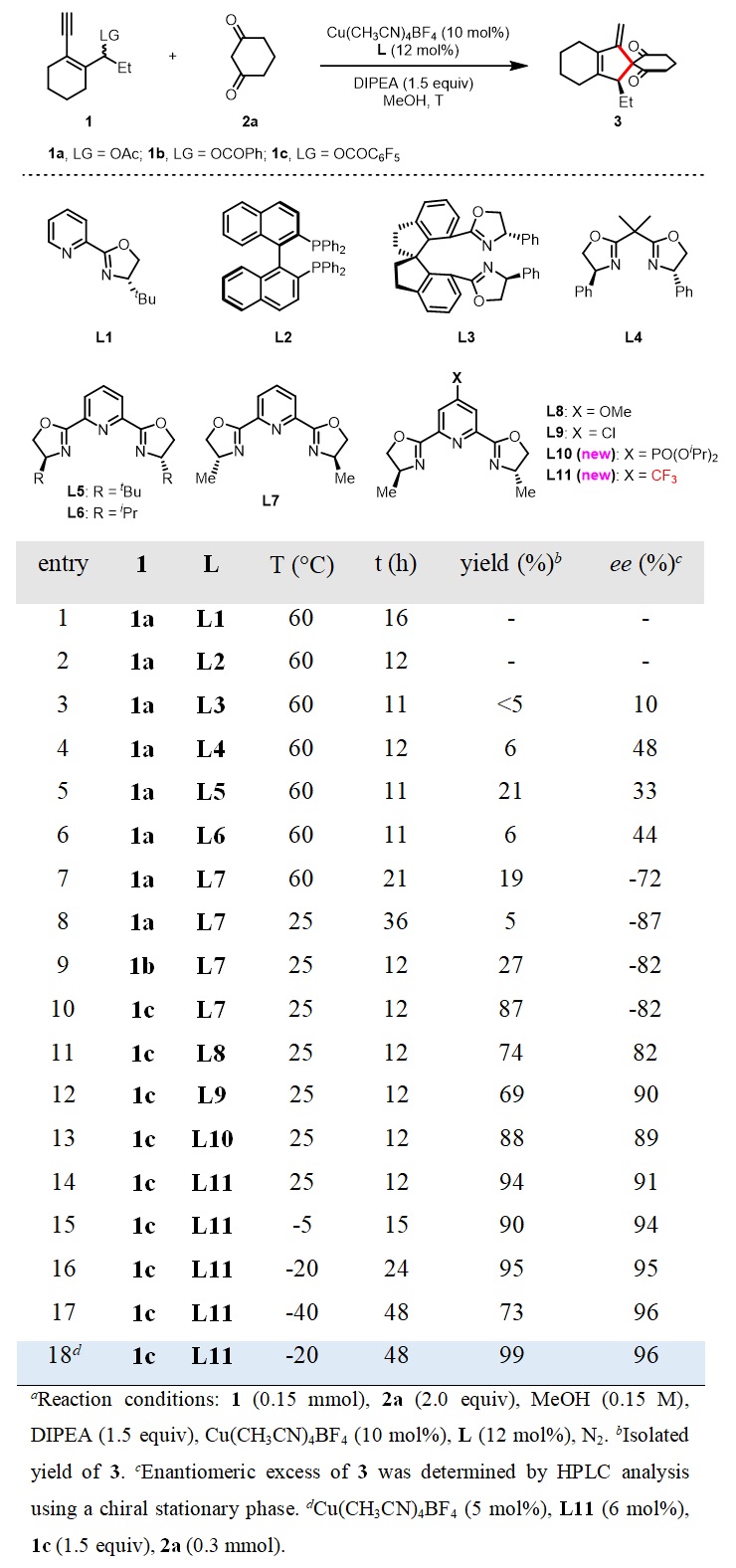
表1. 反应条件的筛选
随后,在最优反应条件下作者对底物的适用范围进行了探索(图3)。首先考察了不同的1,3-二羰基化合物对反应的影响,四元、五元、六元以及含杂原子环状1,3-二羰基化合物均能顺利的得到螺环化合物。含药物相关骨架的1,3-二羰基化合物(巴比妥酸、米氏酸、吡唑二酮等)同样适用于该反应,链状1,3-二羰基化合物也能以中等的产率和对映选择性得到目标化合物。此外,5-取代的1,3-环己二酮和非对称的1,3-二羰基化合物也能应用到此反应中,以优秀的对映选择性和较好的非对映选择性得到目标化合物。接下来,对炔基烯丙醇酯进行拓展,各类烷基、烯丙基、烯基、芳基取代的底物均能以中等到优秀的产率和优秀的对映选择性得到目标化合物。其它环状的炔基烯丙醇酯,如哌啶、1,2,3,4-四氢萘官能化的炔基烯丙醇酯以及五元、七元环状炔基烯丙醇酯及链状炔基烯丙醇酯均能顺利地得到目标螺环产物。
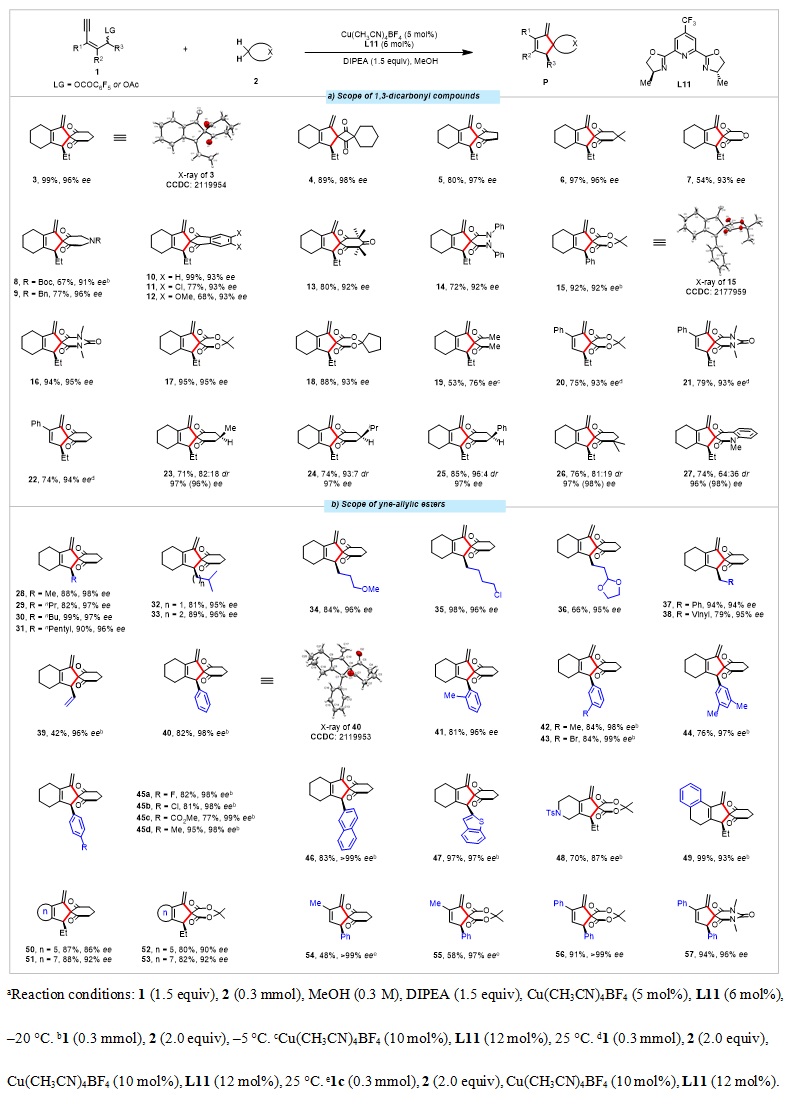
图3. 底物拓展
为了提升该反应的应用价值,作者进行了克量级规模合成及衍生化研究,均能取得很好的效果(图4a和4b)。为了探究该[4+1]环化反应的反应机理,作者进行了控制实验和机理探究。首先以苯乙炔基烯丙醇酯62作为双亲电试剂进行实验,并没有得到目标化合物63,证明了末端炔烃对反应活性至关重要(图4c-1);随后,作者分别利用异构化的炔丙醇酯1af和炔基烯丙醇酯1ai进行反应,以相似的结果得到了螺环产物,说明反应可能经历了相同的中间体Int. a(图4c-2)。为了探究反应对映选择性控制步骤,作者利用甲基取代的米氏酸2v与炔基烯丙醇酯1c进行反应,能以良好的对映选择性得到化合物64,说明ε位亲核进攻过程产生了手性(图4c-3)。随后作者以可能的中间体65为原料,可以顺利的得到Conia-ene 产物(图4c-4),说明[4+1]环化可能经历了亲核取代/ Conia-ene环化的反应历程。接着,作者利用手性的炔基烯丙醇酯为底物,使用不同构型的手性配体,得到不同的手性构型产物,说明产物的绝对构型是由手性配体决定的(图4c-5)。 欣喜的是,作者培养得到双铜/双配体络合物的单晶,利用此单晶作为催化剂,催化效率和对映选择性不变(图4d-e)。作者还进行了非线性效应研究,产物的ee值与配体的ee值存在较好的线性关系,说明反应过程中活性物种可能是单铜/单配体络合物(图4f)。基于以上机理研究,作者推断了如图4g所示的可能的反应机理。
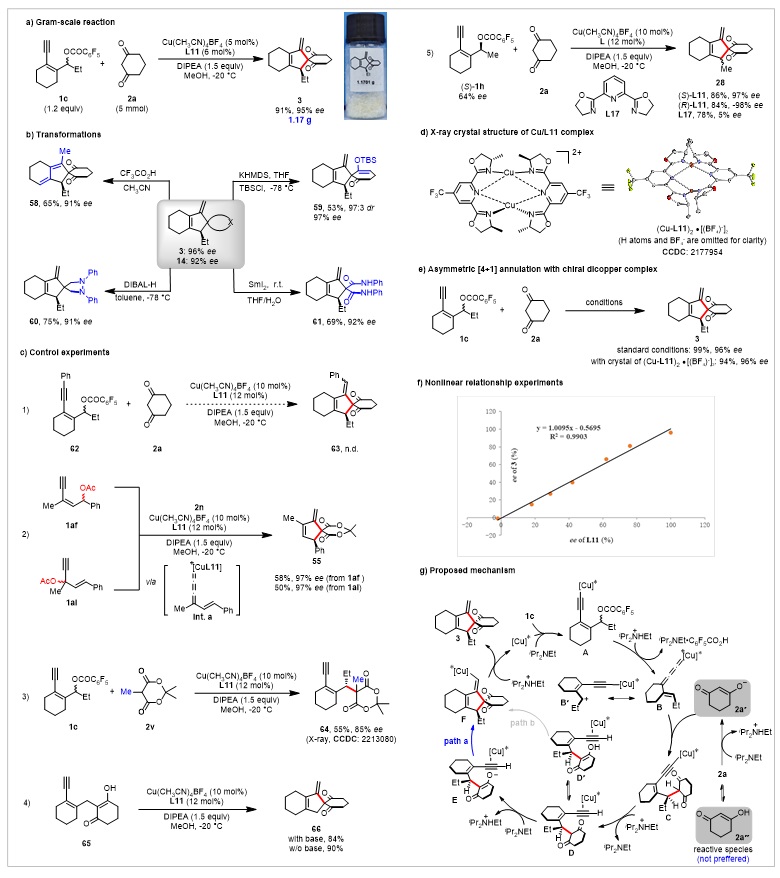
图4. 合成应用、控制实验和机理研究
武汉大学戚孝天教授课题组通过DFT计算,深入探究了烯基-亚丙二烯基铜参与的不对称[4+1]环化反应机理及ε位远程手性控制的起源。如图5所示,理论计算表明该反应先后经历Cu(I)催化的炔基碳氢键CMD去质子化(69-TS)、DIPEA-H+促进的C–O键解离(71-TS)、1,3-二羰基碳负离子2a'对烯基-亚丙二烯基铜中间体72的亲核加成(74A-TS vs 74B-TS),以及DIPEA-H+和DIPEA协助的环化过程。计算结果论证了亲核加成为不可逆过程,是整个反应的对映选择性决定步。该过程中亲核试剂Si-面进攻过渡态74A-TS的活化能 (ΔG‡= 15.4 kcal/mol) 比Re-面进攻过渡态74B-TS (ΔG‡= 16.7 kcal/mol) 低1.3 kcal/mol,表明Si-面进攻在动力学上更加有利。
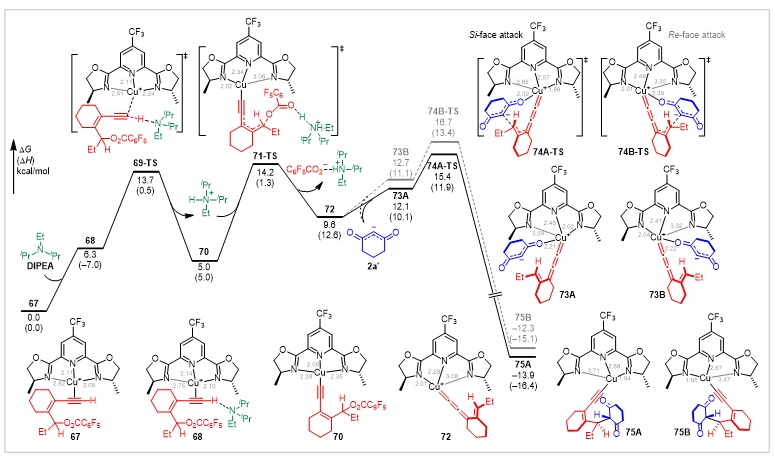
图5. DFT计算
为了揭示对映选择性的决定因素,作者对碳碳成键过渡态74A-TS和 74B-TS中的非共价键相互作用进行了IGMH分析,结果表明两个过渡态中均存在C•••C和Cu•••O相互作用(图6)。作者进一步使用Atoms-in-Molecules (AIM) 理论量化两组相互作用的差异大小,分析结果表明,两个过渡态中C–C键的键临界点电子密度非常接近,而74A-TS中Cu–O键的键临界点电子密度(0.037 a.u.)明显大于74B-TS(0.032 a.u.),意味着74A-TS中存在较强的Cu•••O相互作用,增强了过渡态的稳定性,这与其较短的Cu–O键长(2.32 Å)相互印证。综上所述,74A-TS中较强的Cu•••O相互作用显著促进了Si-面亲核进攻,从而决定了[4+1]环化反应的对映选择性。
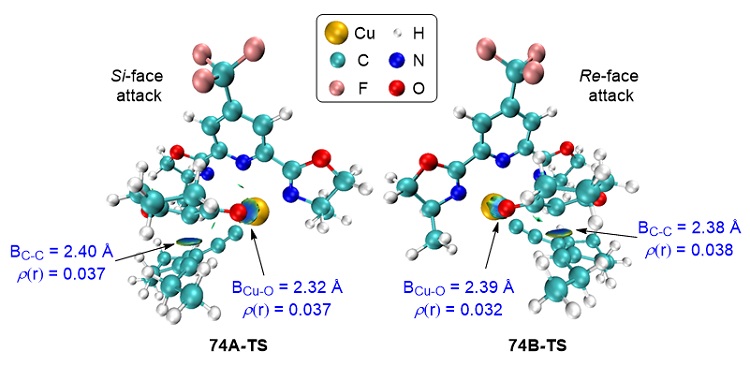
图6. 亲核进攻过渡态中的关键键长和键临界点电子密度
总结
作者报道了首例基于铜催化烯基-亚丙二烯基铜中间体的远程不对称[4+1]环化反应,该反应具有优异的区域选择性、优异的对映选择性、广泛的官能团耐受性及反应条件温和等特点。同时,详尽的机理研究以及理论计算对反应机理以及对映选择性的控制机制提供了有力的支撑。该策略大大拓展末端炔参与的不对称转化反应的范围。华中师范大学孔晗晗博士、朱翠菊副研究员与武汉大学博士生邓双为本论文的共同第一作者,华中师范大学徐浩教授和武汉大学戚孝天教授为通讯作者。该项研究得到了国家自然科学基金、华中师范大学“桂子学者”计划、华中师范大学博士后B类岗位计划及武汉大学中央高校基本科研业务费的支持。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Remote Enantioselective [4+1] Annulation with Copper-Vinylvinylidene Intermediates
Han-Han Kong,# Cuiju Zhu,# Shuang Deng,# Guang Xu, Ruinan Zhao, Chaochao Yao, Hua-Ming Xiang, Chunhui Zhao, Xiaotian Qi*, and Hao Xu*
J. Am. Chem. Soc., 2022, DOI: 10.1021/jacs.2c09572
进一步了解徐浩课题组,请查看课题组网站:
https://www.x-mol.com/groups/Xu_Hao
进一步了解戚孝天课题组,请查看课题组网站:
https://www.x-mol.com/groups/qi
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!



































 京公网安备 11010802027423号
京公网安备 11010802027423号