Nature:仿生合成的金属硫簇能结合N₂但不能还原?
氮是地球上所有已知生命的基本组成元素,也是大气中含量最多的元素。不过,要将大气中惰性的N2转化为生物可利用的形式(如氨和氮氧化物)却并非易事,自然界中只有固氮生物或闪电才有这种能力。事实上,生物固氮过程中的关键角色是能将N2还原为NH3的固氮酶(nitrogenase),其中研究最多的钼-固氮酶可在常温常压下进行N2催化还原。这种酶具有独特的金属-硫-碳辅因子,即[(R-高柠檬酸盐)MoFe7S9C](FeMoco,图1),其中硫环绕的铁原子被认为是捕获和还原N2的关键。由于FeMoco仅存在于固氮酶中,因此化学家对其物化性质以及N2还原活性产生了极大的兴趣。近50年的研究历史中,几例报道的人工合成金属硫簇作为FeMoco类似物可以与N2结合,但让人疑惑的是,任何合成的金属硫簇或提取的FeMoco都无法实现N2还原。尽管详细的N2还原机制仍不明确,但越来越多的研究表明FeMoco消除了其中一个µ2-桥联硫原子,并在铁原子上产生的空配位点捕获底物。类似地,产生小分子N2配合物的常用方法是在还原条件下去除金属结合的配体。然而,将这种方法应用于合成FeMoco的类似物(即金属硫簇)却存在挑战性,这是因为这些簇的无机核中含有配位硫原子,因此空置的金属位点通常会吸引M-S簇的核心硫原子而非N2,从而导致聚集。

图1. FeMoco的N2结合态和N2结合的Mo-Fe-S簇。图片来源:Nature
近日,日本京都大学的Yasuhiro Ohki等研究者在Nature 上报道了人工合成的[Mo3S4Fe]立方体(图1),其中顶点的Fe原子可以捕获N2,并在过量钠和三甲基氯硅烷的存在下催化N2的甲硅烷基化,形成相应的N(SiMe3)3。这些结果不仅证实了合成的金属硫簇能够催化N2的甲硅烷基化,而且证明了Fe原子在富硫环境中的N2还原能力。这对于进一步研究固氮酶FeMoco结合和活化N2的机理有一定启发。

图2. N2结合[Mo3S4Fe]簇的合成和化学修饰。图片来源:Nature
首先,作者从[Mo3S4Fe]簇[CpR3Mo3S4FeCl](CpR = Cp* (1a), CpR = CpL (1b) 和 CpR = CpXL (1c))出发,在强还原剂(KC8用于1a;萘钠用于1b和1c)和N2气氛下于THF中进行反应形成相应的N2簇(图2a)。由于N2配位模式取决于CpR配体的体积,因此得到了N2-桥联的[Mo3S4Fe]二聚体(即[{Cp*3Mo3S4Fe}2(µ-N2)]2- (2a))或者带有末端N2配体的单体(即[CpR3Mo3S4Fe(N2)]-(CpR = CpL (2b)和CpR = CpXL (2c)))。需要指出的是,2a-2c的N2键合模式主要是通过15N2标记簇的15N NMR谱证实的,其中2a在δ = -40.9 ppm处有单峰,而2b(δ = 22.0 ppm和δ =-5.3 ppm)和2c(δ = 22.6 ppm和δ = -5.7 ppm)则分别存在两个峰。另外,在1896 cm-1和1902 cm-1处观察到N-N键的伸缩振动,这进一步证实了2b和2c中存在末端N2键合,并且两者在15N2标记时都表现出红移。然而,共振拉曼或红外光谱却无法检测到2a的N-N键伸缩振动,这可能是由于N2键合模式的对称性略有破坏。如图2b、2c所示,作者还通过X-射线衍射分析揭示了2a和2c的结构,其中2a是N2-桥联的[Mo3S4Fe]二聚体,而2c是带有末端N2键合的单体簇。此外,两者的N-N键距离(2a:1.151(4) Å,2c:1.136(5) Å)均介于游离N2(1.098(1) Å)和N2H2(1.252 Å)之间,这表明N-N键减弱。接下来,作者尝试使用[Mo3S4Fe]立方体进行N2的催化还原。尽管观察到NH3,但没有催化作用,在经典条件下最多生成1.6±0.1 equiv.的NH3(每2c)。作者推测该反应中可能发生S原子的质子化,这会削弱Fe-S键并从[Mo3S4Fe]中释放出顶点Fe原子,这与电化学氧化下立方体的降解有关。值得一提的是,作者发现氯化物簇1a-1c和N2簇2b和2c在过量钠和三甲基氯硅烷的存在下都能将N2催化还原为N(SiMe3)3。如图3所示,在室温和N2(1 atm.)气氛下反应100 h后,至少能生成122.9 ± 3.0 当量(每1c)和248.0 ± 15.6 当量(每1b)的N(SiMe3)3。尽管此时这些配合物活性差异的原因尚未确定,但作者认为是CpR配体的空间位阻效应起主要作用而非电子效应,这是因为在循环伏安法中观察到CpR取代基不会显著影响1a-1c的氧化还原行为或2b和2c的氧化还原特征。
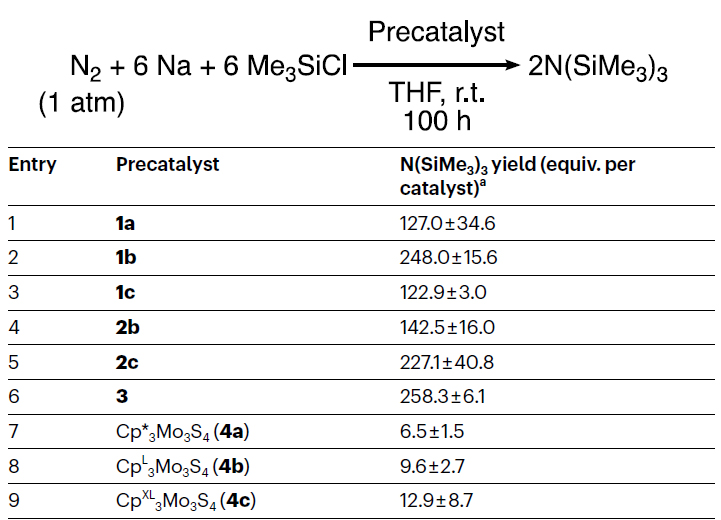
图3. [Mo3S4Fe]簇促进N2催化还原为N(SiMe3)3。图片来源:Nature
值得一提的是,以1b和2c产生的单位活性金属为基础,N(SiMe3)3的产率大约是迄今为止报道的其它Fe催化剂的三倍,并且与Mo和Co催化剂的最高产率相当。另外,在THF中进行的反应会伴随着副产物Me3SiSiMe3、Me3SiOC4H9和 Me3SiOC4H8SiMe3的生成,它们源于三甲基甲硅烷基自由基(•SiMe3)与自身或THF溶剂之间的反应。尽管THF溶剂要比N2反应性高,但在1b的存在下N(SiMe3)3的选择性高达37.2%(图3)。相反,[CpR3Mo3S4](CpR = Cp* (4a)、CpR = CpL (4b) 和CpR = CpXL (4c))、几个相关的FeS簇或FeCl2在相同条件下却得到少量的N(SiMe3)3。在使用1a进行催化反应后,反应混合物的质谱显示[Mo3S4Fe]立方体键合了THF的开环产物,这表明立方核在催化过程中具有足够的稳定性。此外,CO捕获实验表明1c、Na和ClSiMe3(各200 equiv.)在N2存在下进行反应时仅形成11%的[CpXL3Mo3S4Fe(CO)] (5),这意味着在Fe上生成了带有不稳定配体(如THF或N2)的[Mo3S4Fe]物种。也就是说,每个[Mo3S4Fe]立方体的Fe中心是N2还原的位点。基于此,作者提出了[Mo3S4Fe]立方体催化N2甲硅烷基化的可能机理。首先,Fe上的Cl原子被•SiMe3攫取,产生一个与N2键合的空Fe位点(即Fe-N2物种),其中远端N原子经甲硅烷基化生成Fe-NNSiMe3物种。随后,再经甲硅烷基化和还原解离一个肼阴离子[Me3SiN-N(SiMe3)2]-,从而为下一个催化循环再生一个空的Fe位点。N2配体的初始甲硅烷基化可以说是N2还原中最重要的步骤。为了验证这一过程,作者将原位生成的2c(由1c和2.3 equiv. KC8制备而成)与1.1 equiv. ClSiPh3进行反应(图2a),以20%的产率得到单甲硅烷基化的N2物种([CpXL3Mo3S4Fe(N2SiPh3)],3),X-射线衍射分析显示与2c相比(N-N键长为1.136(5) Å),3中的N-N键距离变长(1.193(7) Å,图2d),这些结果与先前报道的[N2SiR3]-Fe配合物的值很接近。尽管3上的SiPh3取代基与催化过程中使用的SiMe3不同,但3的分离证实了在催化循环中可能生成2c的Fe-NNSiMe3类似物。事实上,当用3来催化N2的甲硅烷基化时,得到了258.3±6.1 equiv.的N(SiMe3)3,这表明末端Fe-N2部分对于N2的还原至关重要。
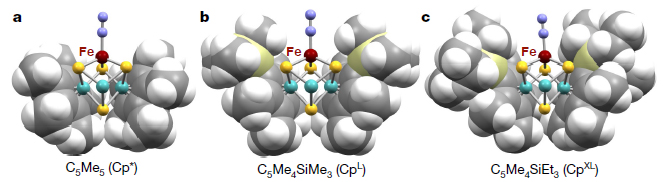
图4. N2结合[Mo3S4Fe]簇的结构模型。图片来源:Nature
如图4所示,N2结合簇的结构模型表明CpR配体围绕着N2配体和[Mo3S4Fe]核心,而CpR配体上的-SiMe3和-SiEt3则是被迫进入[Mo3S4Fe]立方体中Fe位点周围的空间(图4b、4c),以最小化CpR配体之间的空间排斥作用。因此,-SiR3基团就能有效地为[Fe-N2]部分提供空间保护,并通过Fe-N2-Fe桥或立方体间Fe-S相互作用防止立方体的二聚化。相比之下,体积较小的Cp*配体会暴露出更多的Fe位点(图4a),并允许接近另一个[Mo3S4Fe]立方体的Fe位点以生成Fe-N2-Fe二聚体。另一方面,CpR配体的体积也会影响催化活性,这是因为第一个N-Si键是在远端N原子上形成的。在Fe-N2-Fe二聚体中,两个N原子都受到保护,直到其中一个Fe-N键相互作用断裂以产生单体。在使用Fe-Cl立方体的催化反应中,氯化物攫取可能会因体积较大的CpR配体变慢。
总结
本文合成金属硫簇[Mo3S4Fe]立方体催化N2的甲硅烷基化,并提出了金属硫簇成功还原N2的一些关键要素。其中,金属硫核在还原条件下具有足够的稳定性才可使Fe中心足够富电子以活化N2。这些结果表明,抑制金属硫核的分子间聚集是稳定末端N2-键合物种和保持远端N原子反应性的关键。尽管将N2还原为NH3与N(SiMe3)3的机制差异显著,但本文结果对于进一步研究固氮酶FeMoco结合和活化N2的机理来说还是大有帮助的。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Nitrogen reduction by the Fe sites of synthetic [Mo3S4Fe] cubes
Yasuhiro Ohki, Kenichiro Munakata, Yuto Matsuoka, Ryota Hara, Mami Kachi, Keisuke Uchida, Mizuki Tada, Roger E. Cramer, W. M. C. Sameera, Tsutomu Takayama, Yoichi Sakai, Shogo Kuriyama, Yoshiaki Nishibayashi, Kazuki Tanifuji
Nature, 2022, 607, 86-90, DOI: 10.1038/s41586-022-04848-1
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!













































 京公网安备 11010802027423号
京公网安备 11010802027423号