JACS:光促进的PEDA反应和C-H差向异构化合成Pleurotin
Pleurotin,中文名灰侧耳素,是Robbins、Kavanagh和Hervey于1947年从担子菌真菌Pleurotus griseus 的培养液提取物中分离得到的一种琥珀色晶体。此天然产物具有良好的生物活性,对革兰氏阳性菌(如金黄色葡萄球菌)和多种癌症细胞(乳腺癌和结肠癌等)都具有一定的抑制活性。
结构分析表明,Pleurotin拥有独特的六环骨架,含有苯醌结构、两个含氧杂环,一个四取代的反式-六氢茚满骨架、8个连续的立体中心 (其中一个为全碳季碳中心) (图1)。拥挤的环系和密集的立体中心给合成带来了很大的挑战。
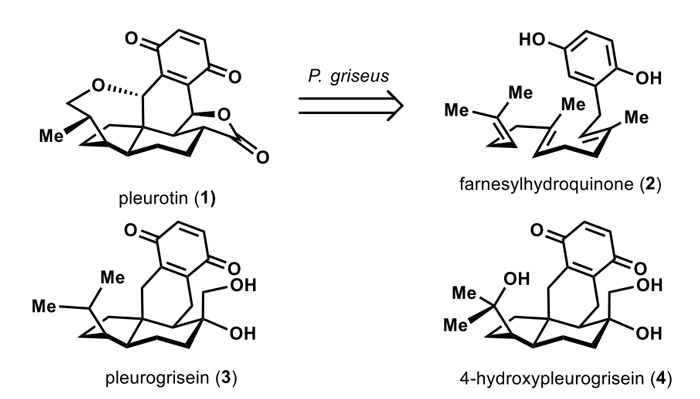
图1
活性天然产物研究一直是新药开发的重要来源。然而由于天然分离Pleurotin的缺乏,阻碍了它作为抗癌先导化合物的持续研究。Shipley和Newman等人利用Hohenbuehelia atrocaerulea 发酵的工艺来获取此天然产物。而实验室的首次合成可以追溯到1988年,Hart等人采用非对映选择性的自由基环化以26步实现该分子的合成。近期,普林斯顿大学的Erik J. Sorensen课题组采用钛酸四异丙酯促进的photoenolization/Diels−Alder (PEDA) 反应和烷氧自由基诱导的HAT介导的C-H差向异构化实现了Pleurotin的简短形式合成。其中,钛酸四异丙酯促进的PEDA反应是国内华东师范大学高栓虎课题组发展的方法,目前已成功解决了其反应性、非对映选择性和对映选择性控制问题 (Nat. Commun. 2017, 8, 622; Chem. Sci. 2021, 12, 7575-7582; J. Am. Chem. Soc. 2021, 143, 6370-6375; Angew. Chem. Int. Ed. 2021, 60, 16655-16660)。
作者从商业可得的溴丙酸正丁酯和5-甲氧基茚酮10出发,经Reformatsky反应得到茚酯11,利用Pearlman催化剂催化氢化,以6:1 的dr值得到烷基茚满12。接着氢化铝锂还原酯成醇盐,再进行无氨气参与的Koide-Birch还原,6 M 盐酸后处理反应液即可将烯醇醚水解并异构化成α,β-不饱和环己烯酮5。为便于产生所需的烷氧自由基,发生HAT介导的差向异构化,作者在化合物5的伯醇处引入烷氧基邻苯二甲酰亚胺基片段得到烯酮亲双烯体15,此片段在下一步的光反应中还起到羟基保护基的作用 (图2)。
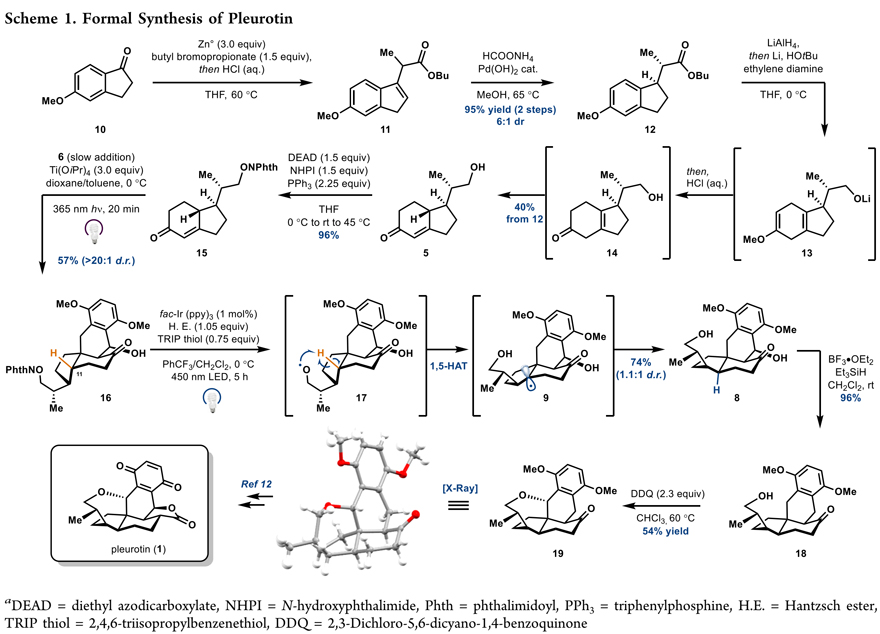
图2
立体选择性的构建含一个或连续季碳中心的多环蒽醇化合物一直是有机合成领域的难点。作者采用高栓虎课题组发展的钛酸四异丙酯促进的PEDA反应,醛6和烯酮15在365 nm光照下发生环化反应,立体专一性地构建了含季碳中心的四环蒽醇骨架。紧接着是另一个关键反应,烷氧自由基诱导的HAT介导的 C-H差向异构化反应,通过广泛而系统的条件筛选,最终作者发现使用75 mol% 的 TRIP 硫醇 (T4) 作为 HAT 试剂,在0 °C的α,α,α-三氟甲苯中可以实现中等的立体控制(74%, 1.1:1 dr),从而顺利将顺式氢化茚满转变成天然产物所需的反式氢化茚满结构。化合物8在BF3•OEt2/Et3SiH下选择性还原苄位羟基得到四环酮醇骨架18,最后DDQ氧化构建氧杂七元环。
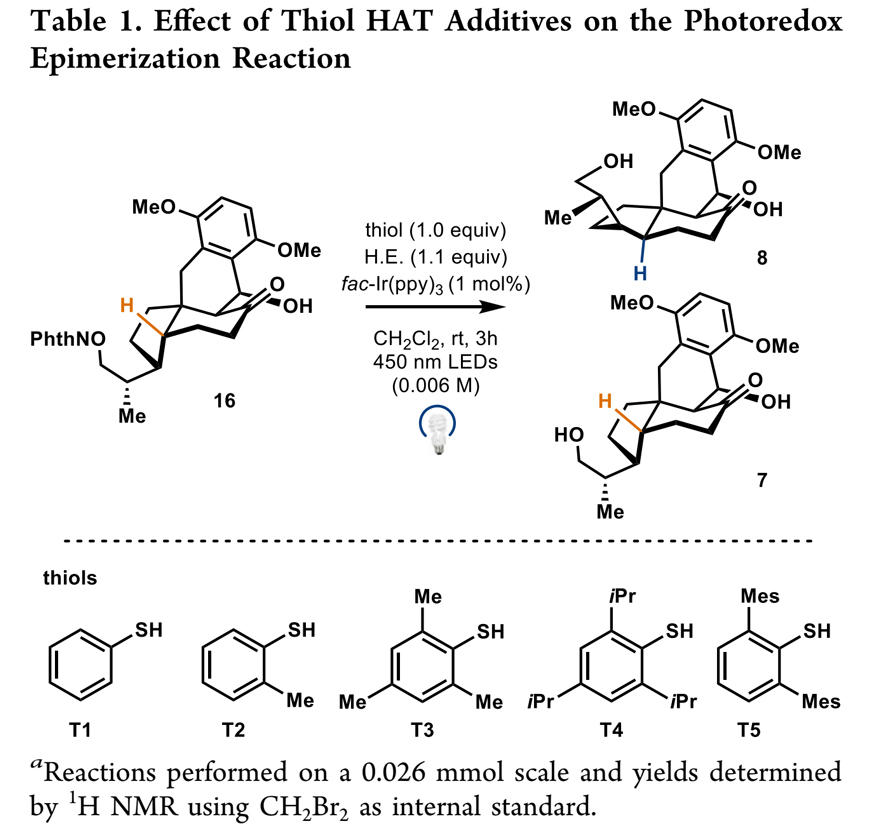
图3
综上,Erik J. Sorensen课题组利用两次光反应实现了Pleurotin的13步简短形式合成工作,包括钛酸四异丙酯促进的PEDA反应构建含季碳四环骨架和1,5-HAT介导的C-H差向异构化。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

A Concise Synthesis of Pleurotin Enabled by a Nontraditional C−H Epimerization
John F. Hoskin and Erik J. Sorensen
J. Am. Chem. Soc. 2021, DOI: 10.1021/jacs.2c06504
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号