Science:亲电金属催化的烯丙基C-H键胺化
胺类化合物不仅是非常重要的有机合成原料及中间体,也是药物小分子中最常见的结构之一。据统计,全球43%的候选药物中都含有脂肪胺,而其中叔胺占60%。迄今为止,化学家已经发展了多种经典的合成方法,例如:卤代烷的亲核取代、相应醛或酮的还原胺化以及E-烯丙醇、乙酸酯或碳酸酯的Tsuji-Trost 烯丙基胺化等。尽管这些方法可方便地构建简单叔胺(如:肉桂醛衍生的烯丙基胺),但要想合成更复杂的胺却需要预氧化、不稳定的试剂以及繁琐的合成步骤(图1A,中部右侧)。对于线性脂肪胺(药物和农用化学品中的主要结构)而言,预官能团化的偶联体(如:醛)通常衍生自末端烯烃,而将胺添加到末端烯烃上无疑是合成此类化合物的简单直接方法。金属介导的烯丙基C-H键胺化反应是很受关注的方法,能够更好地控制反应性、选择性以及官能团兼容性。
2018年,美国伊利诺伊大学厄巴纳-香槟分校(UIUC)的M. Christina White教授(点击查看介绍)团队证实了亚砜-噁唑啉-钯(II) [SOX•Pd(OAc)2] 通过形成π-烯丙基-Pd(SOX)中间体,成功地实现了未活化末端烯烃和N-Tf伯烷基胺的烯丙基C-H键胺化反应(J. Am. Chem. Soc., 2018, 140, 3202)(图1A,中部左侧)。不过,这种胺化反应受限于具有一个或多个与氮共价结合的吸电子基团的胺源,并且需要进一步的合成操作才能生成叔胺。在高浓度下,未受保护的碱性脂肪胺会与亲电子金属结合,并可能抑制其催化循环中的关键步骤(如:分子间C-H键活化)(图1A,底部左侧)。为解决这些问题,M. Christina White教授团队近日提出胺类亲核试剂释放与催化剂循环相结合的自动调节机制,实现了钯(II)催化的烯丙基C-H键胺化交叉偶联反应(图1A,底部中间),并以高区域选择性(>20:1 L:B)和立体选择性(>20:1 E:Z)合成了一系列烯丙基叔胺(多达81种)。该反应不仅条件温和、底物范围广,而且还能实现药物分子及其衍生物的合成和后期修饰。相关成果发表在Science 上。
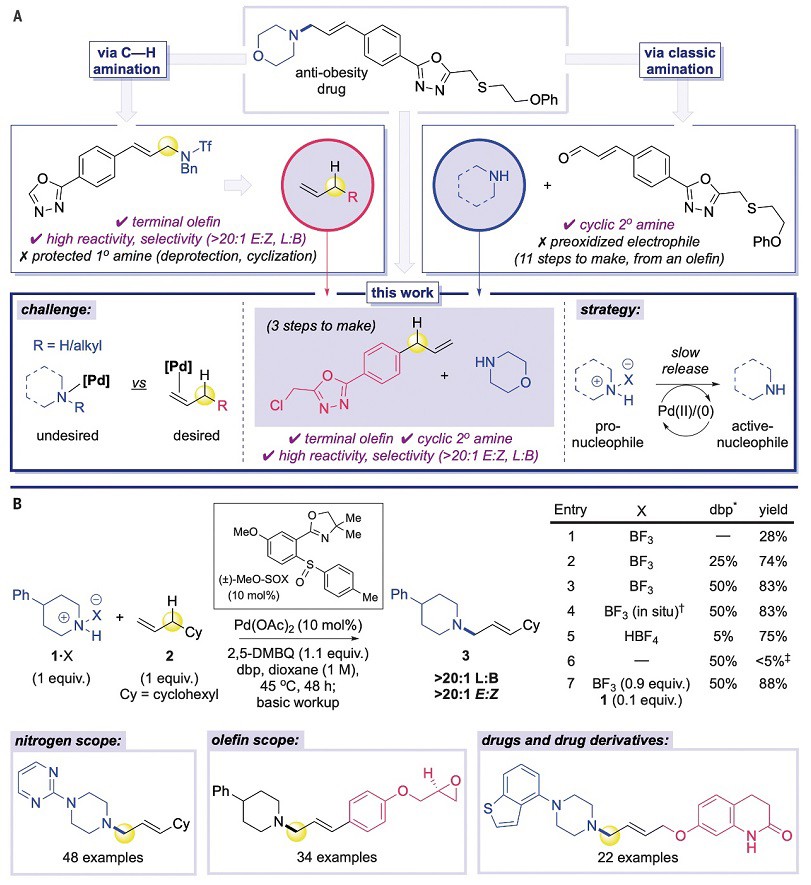
图1. 反应设计和发展。图片来源:Science
首先,作者选择4-苯基哌啶为胺-BF3络合物(1)、烯丙基环己烷(2)为模型底物对反应条件进行了筛选(图1B),结果显示(±)-MeO-SOX•Pd(OAc)2能以28%的收率获得叔胺(3)。进一步对添加剂及其用量、胺-X盐(X=TFA、Ts、Cl及HBF4)、游离胺和胺-X盐比例以及溶剂进行筛选后,最终以83%的收率、>20:1 L:B支链选择性和>20:1 E:Z立体选择性获得所需的叔胺产物3,并且反应无需无水无氧条件。
在最优条件下,以药物化学中最常见的5种脂肪族叔胺结构为合成目标,作者考察了环仲胺和非环仲胺的兼容性。如图2A所示,多种环仲胺都能与未活化末端烯烃2发生烯丙基C-H键胺化交叉偶联(AACC)反应,以中等至较好的收率获得相应的胺化产物(5-10、12-29),不过未取代的四氢吡咯和哌啶(4和11)因过度烷基化而效果较差。α-取代的哌啶和四氢吡咯(8、9和13-15)也能兼容该反应,尽管苯基比甲基体积更大,但是2-苯基吡咯烷比2-甲基吡咯烷的反应效果更好(13a-13b vs 15a-15b)。此外,链状仲胺(30-36)也能实现这一转化,以中等至良好的收率得到所需的胺化产物。特别是,伯胺-BF3亲核试剂经AACC催化还能实现对称叔胺的合成,从而获得相应的二烷基化产物(37),该化合物是选择性平滑肌松弛药阿尔维林的合成前体。
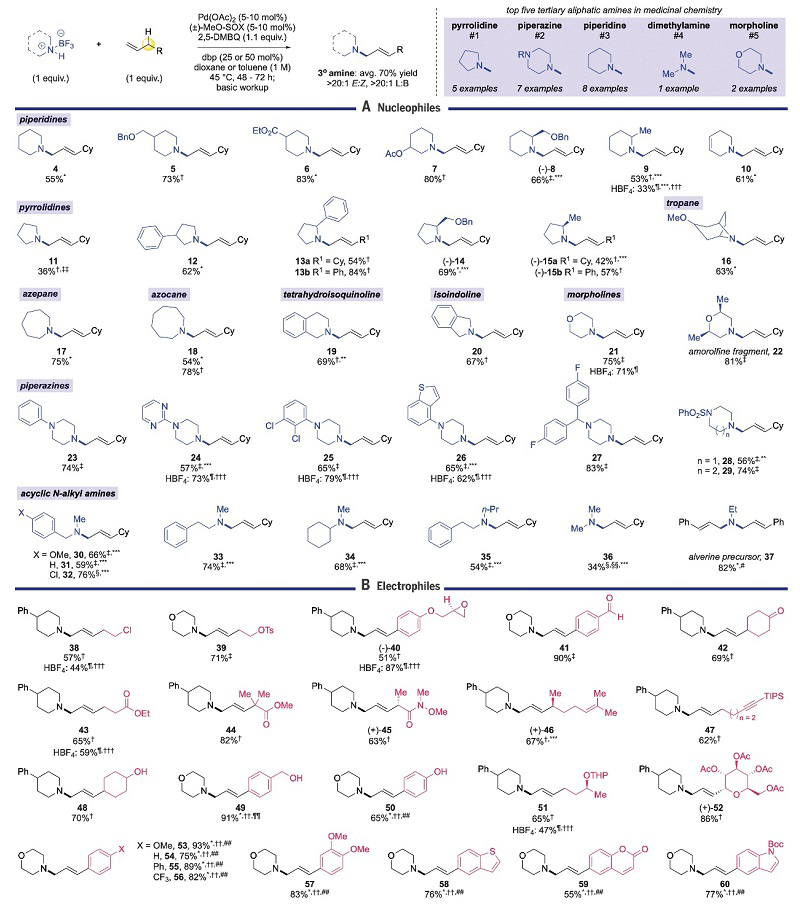
图2. AACC反应底物拓展。图片来源:Science
接下来,作者利用哌啶和吗啉对烯烃的底物范围进行了探索(图2B)。尽管碱性仲胺易与Csp3中心含有离去基团(如:卤素原子、OTs和环氧基团)的底物进行亲核取代反应,但是在AACC催化下却选择性地在烯丙基末端进行胺化反应(38-40),特别是降低dbp负载量并使用胺-HBF4 盐能以87%的收率获得产物40,同时避免了环氧化物开环。此外,该反应还能耐受多种官能团,例如:醛羰基(41)、酮羰基(42)、乙酯(43)、偕二甲基酯(44)、带有α-立体中心的Weinreb 酰胺(45)、烯基(46)、炔基(47)、游离醇(48-50)、四氢吡喃醚(52)、不同基团取代的苯基(53-57)、苯并噻吩(58)、香豆素(59)以及吲哚(60),同时没有观察到羟基氧化以及酸解等副反应。需要指出的是,胺-HBF4 盐的产率通常与胺-BF3底物相似或降低(9、21、26、38、43、51、69、71),但底物24和25的胺-HBF4 盐则能获得更好的收率并抑制二烯的形成。总的来说,该方法为Hofmann烷基化、还原胺化、烯烃官能团化和烯丙基取代合成提供了一种正交方法。
随后,作者将该反应用于合成含叔胺结构的药物分子。如图3A所示,市售可得的cyclizine与烯丙基苯经AACC催化能以优异的收率得到钙拮抗剂桂利嗪(61)和氟桂利嗪(62)。类似地,N-甲基苄胺衍生物与烯丙基芳烃进行反应时,以中等至较好的收率得到抗真菌药物萘替芬及其类似物(63-65)。值得一提的是,从吗啉和带有苄基氯的末端烯烃出发,经AACC催化和亲核取代便可得到抗肥胖化合物(67),这比先前的还原胺化路线减少一半步骤(5步 vs 12步)且总产率近乎翻倍(8.5% vs 5.0%)。另外,嘧啶基哌嗪-BF3与烯烃经AACC催化和加氢两步即可合成抗焦虑药物,如丁螺环酮(68)、伊沙匹降(69)、坦度螺酮(70),以及临床抗精神病药物,如阿立哌唑及其类似物(71-72)。此外,该方法还能实现药物分子的后期修饰以及药物类似物的合成(图3B),例如5-羟色胺再摄取抑制剂帕罗西汀、氟西汀和去甲基喹硫平(74-76)、止咳药右美沙芬(77)、氯吡格雷(78)、Boc-deoxydebio-1452类似物(79)以及广谱抗生素特地唑胺衍生物(82)。

图3. 复杂脂肪族叔胺类药物及其衍生物的合成。图片来源:Science
作者进行了一系列实验来阐述AACC催化的反应机理(图4)。1)利用1H NMR来监测反应中胺-BF3 (1•BF3)、胺-HBF4 (1•HBF4) 和烯丙基C-H键 胺化产物 (3•HX) 三者随时间的变化曲线(图4A),结果显示在反应的初始阶段1•BF3稳定消耗、1•HBF4迅速形成,等到1•HBF4形成~20-30%时才开始出现3•HX,并且反应结束后以3•HBF4形式存在,这可能是有助于抑制产物的过烷基化等副反应;2)气相色谱-质谱 (GC-MS) 分析反应早期的体系可观察到痕量的甲基酮,这与Pd(II)还原为Pd(0)的Wacker烯烃氧化反应相一致(图4C);3)醌对Pd(0)氧化提供一个羟基酚碱,能使1•HBF4 去质子化以引发胺官能团化,并将质子从1•HBF4 转移到碱性更强的叔胺产物 3;4)向反应体系中添加游离胺亲核试剂 1 或叔胺产物 3,可将反应初始速率分别增加 10 倍和 7 倍,若以催化量1或3a (10 mol %) 参与反应时,24 h后的产率明显提高(图4B);5)催化量的仲胺有利于提高反应速率,并且降低催化剂负载量(10 → 5 mol%)也能保持收率,若1的量大于 20 mol % 时,则观察到产物收率显著下降。上述实验进一步说明,AACC 催化的关键是催化剂循环与游离胺的生成有关,并且任意时间内催化循环中游离胺的上限约为 10% -20%。
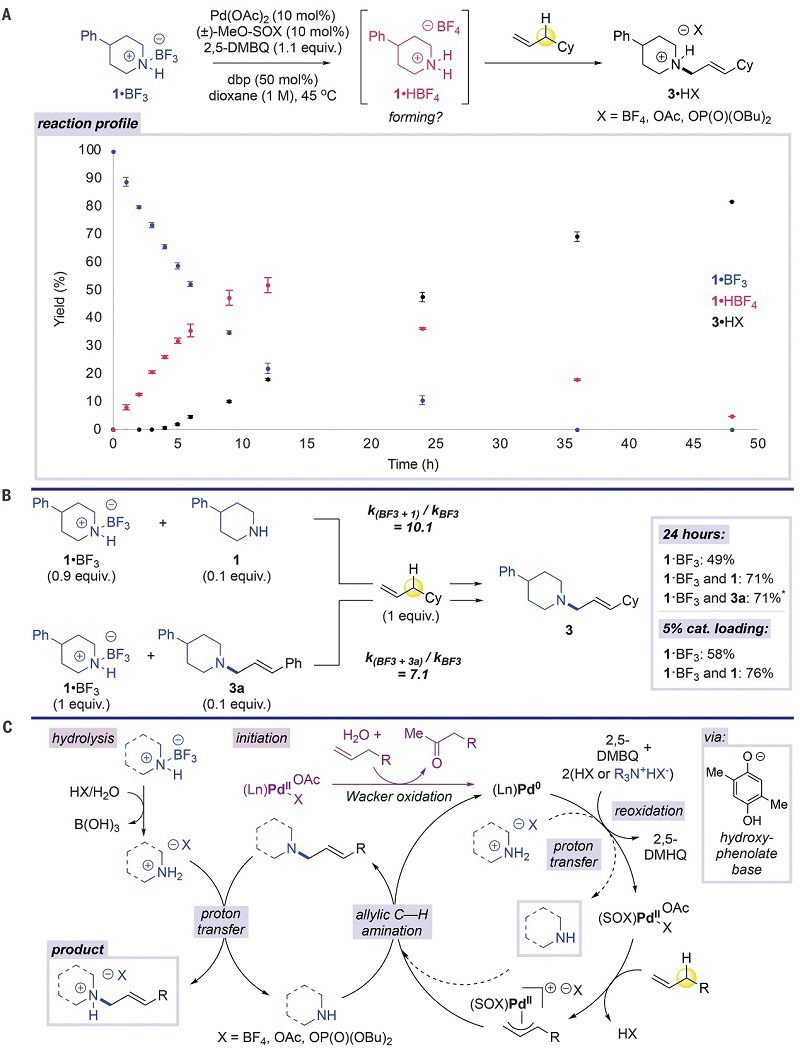
图4. 机理研究和可能机理。图片来源:Science
作者随后提出了可能的反应机理(图4C)。在反应的初始阶段,体系中的二价钯通过Wacker烯烃氧化反应被还原为零价钯,再被体系中的二甲基苯醌重新氧化为SOX-Pd(II)物种,随后经Pd(II)介导的C-H键异裂得到阳离子π-烯丙基-Pd(SOX)络合物。此时,醌介导的Pd(0)氧化过程中产生的羟基酚盐和/或叔胺产物作为碱,使得仲胺-HBF4盐原位去质子化以产生受催化剂用量调节的低浓度的游离胺亲核试剂。接着,游离仲胺与π-烯丙基-Pd(SOX)络合物发生烯丙基C-H键胺化反应,接着经还原消除得到叔胺,同时再生零价钯参与催化循环。
总结
M. Christina White教授团队成功地实现了钯(II)催化的烯丙基C-H键胺化交叉偶联反应,并以高区域选择性(>20:1 L:B)和立体选择性(>20:1 E:Z)合成了一系列烯丙基叔胺,包括12种药物化合物和10种复杂药物衍生物。该方法条件温和、底物适应性强,对于药物分子合成以及后期修饰都有很好的效果。此外,该方法为霍夫曼烷基化、还原胺化、烯烃官能团化和烯丙基取代合成提供了一种正交方法,并为高通量、基于片段的药物研发提供了强大的工具。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Allylic C–H amination cross-coupling furnishes tertiary amines by electrophilic metal catalysis
Siraj Z. Ali, Brenna G. Budaitis, Devon F. A. Fontaine, Andria L. Pace, Jacob A. Garwin, M. Christina White
Science, 2022, 376, 276-283, DOI: 10.1126/science.abn8382
导师介绍
M. Christina White
https://www.x-mol.com/university/faculty/212
(本文由吡哆醛供稿)
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!




























 京公网安备 11010802027423号
京公网安备 11010802027423号