基于氮杂对亚甲基苯醌的1,6-共轭加成策略实现吲哚及咔唑的催化不对称氮烷基化反应
吲哚和咔唑的骨架广泛存在于天然产物与活性药物分子之中,其中氮烷基化的吲哚与咔唑更是具有独特的生物活性,因此发展直接高效的不对称催化吲哚及咔唑的氮烷基化反应一直以来受到广泛的关注。然而,吲哚N-H键较弱的亲核性导致目前该不对称催化反应的研究相当受限,大多数分子间的反应局限于特殊的底物(如烯丙基化)、取代基或采用迂回的策略增强N-H键的亲核性。另一方面,对咔唑不对称氮烷基化反应的系统研究十分少见。最近,香港科技大学的孙建伟教授(点击查看介绍)课题组基于氮杂对亚甲基苯醌的1,6-共轭加成策略,实现了吲哚及咔唑的催化不对称氮烷基化反应。
作者设想氮杂对亚甲基苯醌(aza-p-quinone methides,aza-p-QMs)具有极高的反应活性,将其作为烷基化试剂可能会弥补N-H键较低的化学反应性,并获得较好的立体选择性。
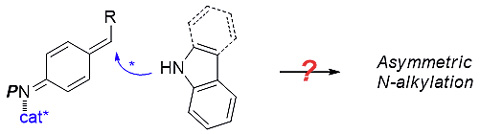
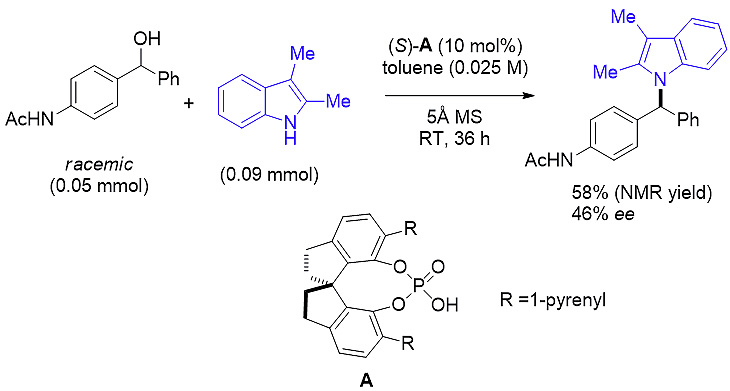
作者以乙酰基保护的对氨基苄醇作为aza-p-QMs的前体,在多种手性磷酸的作用下能与2,3-二甲基吲哚反应得到预期产物,但对映选择性均为中等水平。接着他们对氮保护基进行系统调控,最终可得到产率和对映选择性都极高的目标产物。
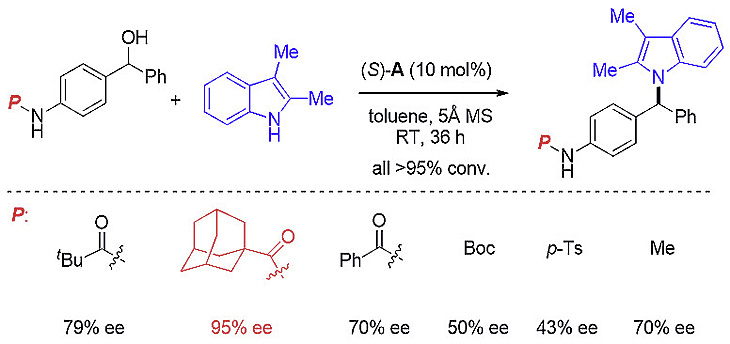
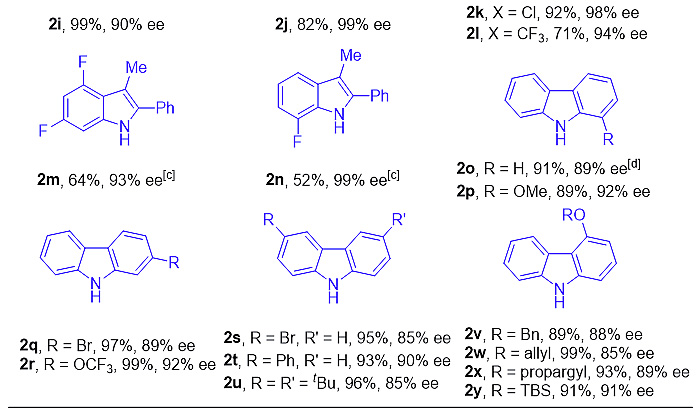
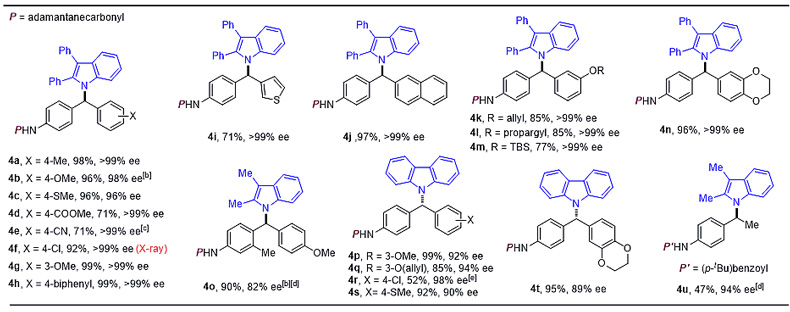
在最优反应条件下,作者对吲哚和咔唑的适用范围进行了考察,无论是供电子还是吸电子取代基底物,均可得到较高的产率和对映选择性。同时,反应也表现出良好的官能团兼容性,烯基、硅醚基、酯基、氰基等都不受反应影响。随后作者还考察了aza-p-QMs底物范围的适用性。
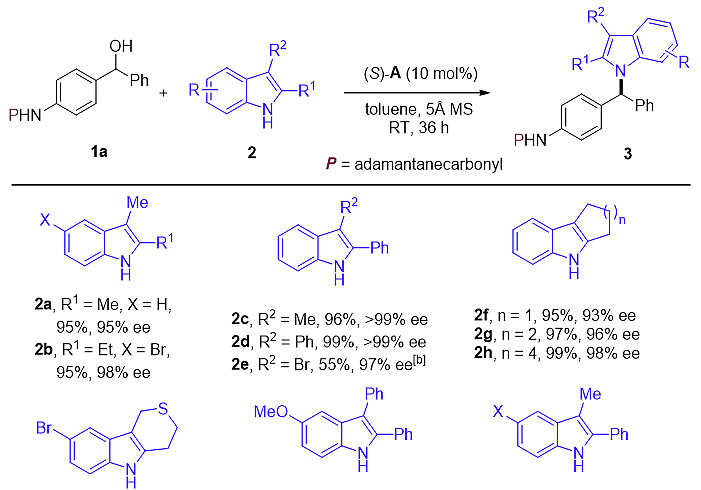
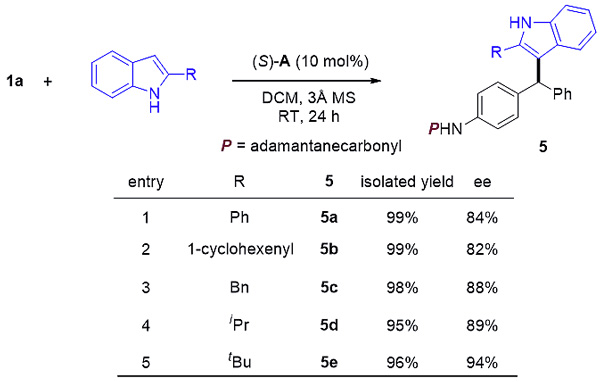
另外,作者还考察了吲哚3位未发生取代的反应情况。经过简单的条件筛选,作者发现2位烷基、烯基及芳基取代的吲哚均可与aza-p-QMs反应,高产率地得到3位烷基化的产物,对映选择性良好到优秀。
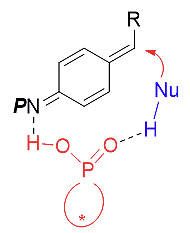
最后,通过相关的控制实验,作者提出反应的可能过渡态,手性磷酸作为双功能催化剂,布朗斯特酸位点活化底物原位生成aza-p-QMs的酰胺键,磷酰键则作为路易斯碱位点活化吲哚或咔唑的N-H键。
这一成果近期发表在《德国应用化学》上,文章的第一作者是香港科技大学的博士后陈敏。
该论文作者为:Dr. Min Chen, Prof. Jianwei Sun
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Catalytic Asymmetric N-Alkylation of Indoles and Carbazoles through 1,6-Conjugate Addition of Aza-para-quinone Methides
Angew. Chem. Int. Ed., 2017, 56, 4583, DOI: 10.1002/anie.201701947
导师介绍
孙建伟
http://www.x-mol.com/university/faculty/7073
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号